
����Ŀ��A��E�dz��л�ѧ�г�����5�������Ҷ�����һ����ͬԪ�ء�B���ж����壬��ɫ����E��ˮ�е��ܽ��С��0.01g��20�棩������֮���ת����ϵ��ͼ��ʾ������������ʾ���˵������ܷ�����ѧ��Ӧ����������ʾ���ʼ���һ�������´���ת����ϵ���������ʵķ�Ӧ��������ȥ����
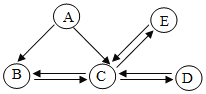
(1)д����صĻ�ѧ����ʽ����A+C��_____����C��E��_____��
(2)����C�л�����������Bʱ���ɽ������ͨ��_____��ȥ����B��
(3)д�������£�����C�����������ƣ�Na2O2����Ӧ����̼���ƺ������Ļ�ѧ����ʽ_____��
��Դ�ͻ������������Ϊ���ǹ�ע�Ľ��㡣
(4)�����Ļ�ʯȼ����ú��______����Ȼ���ȡ���Ȼ������Ҫ�ɷ���CH4���ڿ�������ȫȼ�յĻ�ѧ����ʽ��____________________________________��
(5)ȼú��Ӱ�컷�������л���������ȼúû��ֱ�ӹ�ϵ����______������ţ���ͬ����
A ���� B ����ЧӦ C �������ƻ� D ���������������
(6)CO2�����������ߣ�ʹȫ�����������������ء���ͼΪCO2�����һ�֡�̼ת������
![]()
����������������������______��
A CaCO3 B C2H5OH C CO
��CO2��H2�ڴ����ͼ��������£�����ת��Ϊ����ԭ����ϩ��C2H4�����뽫�÷�Ӧ�Ļ�ѧ����ʽ����������2CO2+ 6H2  C2H4+_______________��
C2H4+_______________��
�۽�CO2ͨ��Na2CO3��Һ�У�ֻ����NaHCO3���÷�Ӧ�Ļ�ѧ����ʽ��_______��
���𰸡�CO2+C![]() 2CO CO2+Ca��OH��2�TCaCO3��+H2O ���ȵ�����ͭ 2CO2+2Na2O2��2Na2CO3+O2 ʯ�� CH4+O2
2CO CO2+Ca��OH��2�TCaCO3��+H2O ���ȵ�����ͭ 2CO2+2Na2O2��2Na2CO3+O2 ʯ�� CH4+O2![]() CO2+ 2H2O C B 8H2O CO2+ Na2CO3+ H2O��2NaHCO3
CO2+ 2H2O C B 8H2O CO2+ Na2CO3+ H2O��2NaHCO3
��������
B���ж�����һ����̼��һ����̼��C�ת������C�Ƕ�����̼��A�ܷ�Ӧ����һ����̼�������̼����A��̼��������̼����E�ת�����Ұ�ɫ����E��ˮ�е��ܽ��С��0.01g��20�棩����E��̼��ƣ�������̼����D�ת��,��D��̼���ƻ�̼�
��1����A+C��̼�ڸ����������������̼��Ӧ����һ����̼�Ļ�ѧ����ʽ�� CO2+C![]() 2CO����C��E��������̼���������Ʒ�Ӧ����̼��ƺ�ˮ�Ļ�ѧ����ʽ��CO2+Ca(OH)2�TCaCO3��+H2O��
2CO����C��E��������̼���������Ʒ�Ӧ����̼��ƺ�ˮ�Ļ�ѧ����ʽ��CO2+Ca(OH)2�TCaCO3��+H2O��
��2��һ����̼�������ȵ�����ͭ������ԭ��Ӧ����������̼�������ʶ�����̼�л�������һ����̼ʱ���ɽ������ͨ�����ȵ�����ͭ��ȥһ����̼��
��3�������£����ʶ�����̼�����������ƣ�Na2O2����Ӧ����̼���ƺ������Ļ�ѧ����ʽ�� 2CO2+2Na2O2��2Na2CO3+O2��
��4�������Ļ�ʯȼ����ú��ʯ�ͺ���Ȼ���ȡ���Ȼ������Ҫ�ɷ���CH4���ڿ�������ȫȼ�ղ���ˮ�Ͷ�����̼�Ļ�ѧ����ʽ��CH4+O2![]() CO2+ 2H2O��
CO2+ 2H2O��
��5��ȼú��Ӱ�컷�������л���������ȼúû��ֱ�ӹ�ϵ���ǣ�
A��úȼ�ղ����������������γ����ꣻ��ѡ����ȷ�������������⣻
B��úȼ�ղ�������������̼���壬�������ЧӦ����ѡ����ȷ�������������⣻
C���ƻ������������������������úȼ���أ���ѡ������������⣻
D��úȼ�ղ��������̳���ʹ��������������ӣ���ѡ����ȷ�������������⣻
��ѡ��C��
��6��CaCO3 ��C2H5OH�� CO���Ǻ�̼�������CaCO3 ��CO���������������ƣ������ǹ�Ϊ��������л������C2H5OH����ѡB��
��CO2��H2�ڴ����ͼ��������£�����ת��Ϊ����ԭ����ϩ��C2H4�����÷�Ӧ�Ļ�ѧ����ʽ����������2CO2+ 6H2  C2H4+8H2O���÷�Ӧ���������غ㶨�ɣ�������ȷ�Ӧ����2����ԭ�Ӻ�1����ԭ�ӣ�ȱ�ٵ����ʻ�ѧʽΪ��H2O��
C2H4+8H2O���÷�Ӧ���������غ㶨�ɣ�������ȷ�Ӧ����2����ԭ�Ӻ�1����ԭ�ӣ�ȱ�ٵ����ʻ�ѧʽΪ��H2O��
�۹���������̼��̼���ơ�ˮ��ͬ��Ӧ����̼�����ƵĻ�ѧ����ʽ�ǣ�CO2+ Na2CO3+ H2O��2NaHCO3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������NaOH��Һ������ͨ��CO2���壬��������������ijʵ��С���ͬѧ��������Һ�ɷֽ���������̽��������������ǵ�̽�����������������⣺
��������⣩������Һ�����ʵijɷ���ʲô��
���������ϣ�����һ����CO2����������ͨ��һ������NaOH��Һ�У����ܷ�������������ѧ��Ӧ��
�ȷ�����Ӧ��2NaOH+CO2�TNa2CO3+H2O
��NaOH��Ӧ��ȫ����������Ӧ��Na2CO3+CO2+H2O�T2NaHCO3
�Y�϶���Ca��HCO3��2������ˮ��CaCl2��Һ��NaCl��Һ�������ԣ� NaHCO3��Һ�ʼ��ԣ���ʹ��̪��Һ���ɫ��
����������裩С��ͬѧͨ�����ۣ�������������ֲ���
����һ������ΪNaOH��Na2CO3
�����������ȫΪNa2CO3
��1������Ϊ������������Ϊ_____
�����ģ�����ȫΪ NaHCO3
��ʵ��̽����С��ͬѧ��Ʋ����������ʵ�飺
ʵ�鲽�� | ʵ����� | ʵ������ | ʵ����� |
�� | ȡ������Ӧ�����Һ�����Թ� �У��������CaCl2��Һ | �а�ɫ�������� | ��2������_____������ |
�� | ȡ������������Ӧ����ϲ��� Һ���μӼ��η�̪��Һ | ��3������Ϊ_____ | ����������� |
�� | ȡ������������Ӧ����ϲ��� Һ����������ϡHCl | �����ݲ��� | ��4������_____���� |
��ʵ���ܽᣩ�������ʵ�飬ʵ��С���ͬѧ�ܽᲢд��������̽�������еĸ�����Ӧ����ʽ��
��5������Ϊ������������Ӧ�Ļ�ѧ����ʽ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ��װ��ͼ���ش��й����⡣
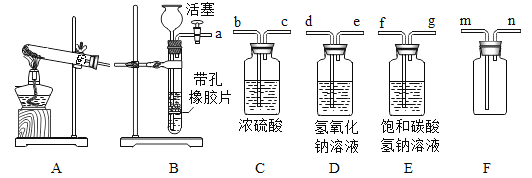
��1��ʵ������ͼ1��Aװ����ȡ����ѡ�õ�ҩƷ________________��
��2�����д���ʯ������С�մ��ĩ��ϡ���ᡢϡ���ᣬѡ����ʵ�������Bװ���Ʊ�CO2���壬�仯ѧ����ʽΪ______________��ʹ��Ӧֹͣ�IJ���������______________����Ҫ�õ�һƿ����ǧ��Ķ�����̼��������װ���⣬����ѡ����ʵ�װ�ó�ȥ���ܺ��е����ʣ���������ȷ������˳��Ϊa��___________����ĸ��ţ���װ��C��������________________��
��3����ҵ������Ϊԭ���Ʊ����ᣨHNO3���Ĺ��̣���ͼ2����
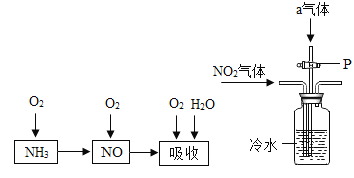
�����ͼ2��ҵ���ð�����ȡNO�Ļ�ѧ����ʽ�� _________��Ȼ�������NO������������NO2��NO2��ˮ��Ӧ�����������NO��ͼ3��ͨ�������a��_________________����Ŀ����_______________��
_________��Ȼ�������NO������������NO2��NO2��ˮ��Ӧ�����������NO��ͼ3��ͨ�������a��_________________����Ŀ����_______________��
��ͼ3��װ����һ����֮����____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п���������ĵ���Ԫ�أ��ơ�����Ԫ�ء���
��п�Ĺ㷺Ӧ�á�
��1���������������ڵĶ�ͯ�����������ȱп���ᵼ�·���������ʳ�����Ӧ�ٶۡ�ȱ������ʱ�����ᵼ�¡�_________ ֢������������������ ����п������ҩ����ʳ�����٣������Ա����ຣ��Ʒ����ɫ����Ⱥ�п��ʳ����������п���������п ��ָ_____��
A. ���� B. Ԫ�� C. ԭ�� D. ����
��2��ʵ������п��ϡ������ȡ������ͬʱ�õ�����Ʒ����п����Ӧ�Ļ�ѧ����ʽΪ___________________��
���Ʊ���ˮ����п��
�Ժ�п��������Ҫ�ɷ�ΪZnO,����ΪFeO�pCuO��Ϊԭ���Ʊ���ˮ����п��ZnSO4��7H2O�����������¡�

��1�������Ŀ����___________________��
��2����ʵ��������������Ϊ98%���ܶ�Ϊ1.84g/ml��Ũ��������200g��25%��ϡ���ᣬ��ҪŨ��������Ϊ___________����ȷ��С�����һλ��������ʱ����Ҫ�IJ�����������Ͳ�p���������ձ���__________��
��3������X��__________�������к��еĽ���������__________��
��4�������л����ˮ����пǰʡ�ԵIJ�����_______�p��ȴ�ᾧ�p���ˡ�ϴ�Ӻ͵��º�ɡ�
��5��ij�¶��£�Fe(OH)3�ֽ�õ�һ�����p��������21:8���������������Ļ�ѧʽ__________��
��6�����������У��¶ȡ�pH�Գ���Ч����Ӱ��ֱ����ͼ��ʾ����ͼ��֪������ʱ�¶�Ӧ������__________��Ϊ�ˣ�pHӦ������__________Ϊ�ˡ�
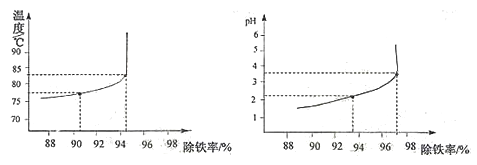
����ɲⶨ����һ�������£���ZnSO4��Һ�м���Na2CO3��Һ����ַ�Ӧ�����ˡ�ϴ�ӡ����¸���õ���������aZnCO3��bZn(OH)2��cH2O��Ϊ��ȷ��aZnCO3��bZn(OH)2��cH2O��ɣ���������ʵ�飺
���������ϡ�������ÿ����Ӧ�����վ���ȫ����ʯ��Ϊ�������ƺ���ʯ�ҵĻ�����
aZnCO3��bZn(OH)2��cH2O���ȷֽ�����ZnO��H2O��CO2���ֲ��
����ZnCO3 ![]() ZnO+CO2����Zn(OH)2
ZnO+CO2����Zn(OH)2![]() ZnO+H2O��
ZnO+H2O��
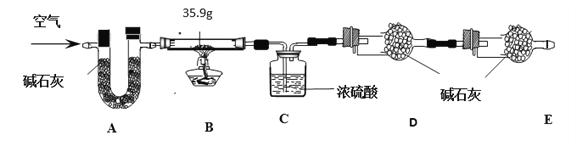
�ֳ�ȡ35.9 g aZnCO3��bZn(OH)2��cH2O��Bװ���н������գ�����ȫ���չ����в�������������ͨ��װ��C��װ��D�����Ƿֱ�����7.2 g��4.4 g��
��ʵ����������ݴ�����
��1��װ��A��������_______________��
��2����û��Eװ�ã���ö�����̼������____________���ƫ����ƫС������Ӱ�족����
��3�������������ݣ���ѧʽa ZnCO3��b Zn(OH)2�� c H2O�е�a:b:c ��_____________ ��
����˼����չ��
�����ɷ����¶ȵȲ�ͬ����a��b��c���в��죬����B��ѧʽΪZnCO3��2Zn(OH)2��H2O�����B�м���ϡ���ᣬ��Ӧ�Ļ�ѧ����ʽΪ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������һ����������������ϡ��������μ���ij̼������Һ��ʵ������У������������������̼������Һ��������ϵ��ͼ��ʾ���Լ��㣺
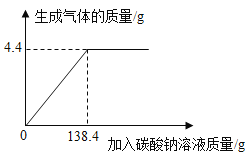
��1��ǡ����ȫ��Ӧʱ���������������Ϊ g��
��2��ǡ����ȫ��Ӧʱ������̼������Һ��Na2CO3�������Ƕ��٣�
��3����ǡ����ȫ��Ӧʱ������Һ��������������Ϊ5%����ϡ������������������Ƕ��٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ע�������е��ˮ�Ĵ���ʵ��,�缫����ע����Ͳ��,װ��ʾ��ͼ���¡�����˵������ȷ����
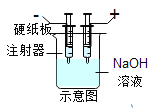
A.ˮ�м���������������,��������ǿˮ�ĵ�����
B.����ע�����ڵ�ԭʼҺ�桢�缫����Ҫ����һ��
C.��������ʱ,��ע����(����ʣ����Һ)ȡ��,���˿����ƾ��ƻ���,�ƶ���������
D.ʵ��ɹ�ʱ,���ע�����յ����������Լ���ұߵ�2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʾ��ʵ������У���ȷ���ǣ�������
![]()
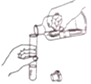


A�����Թ��ڼ�п��B�����Թ��ڵ�Һ�塡C�����Թ��ڵ�Һ�����D����������ס�Թ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڡ��¹ڷ��ס���ҽ���л�ʹ�ô�������Һ��������Һ���ɷ�Ϊ�ᡢ����dz��л�ѧѧϰ����Ҫ���ݡ�
��1�����ᡢ����ȳ������ᶼ�������ƵĻ�ѧ���ʣ�����Ϊ������ˮ��Һ�ж������___________�������ӷ��ţ���
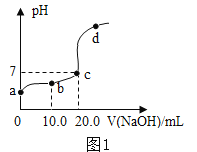
��2����20.0mL��������Ϊ30%�������еμ�����������Һ����Һ�е�pH����������������Һ������仯��ͼ1��ʾ�������й�������ȷ����_________��
A b��d���Ӧ��Һ��pH��b>d
B ��b���Ӧ����Һ�еμ�ʯ����Һ����Һ����ɫ
C ��������������Һ����������һ��Ϊ30%
D d���Ӧ����Һ��������NaCl��NaOH
��3����֪ij��84����Һ��ƿ�岿�ֱ�ǩ��ͼ2��ʾ��
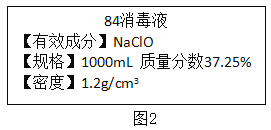
�ٸ�ƿ��84����Һ����NaC1O������Ϊ_________g��
�ڹ�ҵ��������������������Һ��Ӧ����ȡNaClO��ͬʱ����ʳ�ε���Ҫ�ɷֺ�ˮ��д���÷�Ӧ�Ļ�ѧ����ʽ_____________��
��4��ʵ������һƿ����¶���ڿ����е�����������Һ��Ϊȷ����ɷ֣�С��ͬѧ����������̽����
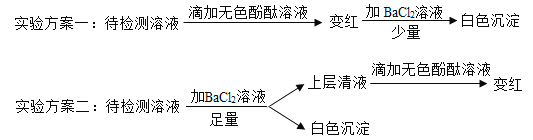
�ٸ���ʵ�鷽����ȷ����ƿ��Һ�����ʳɷ���ʲô_________��
��ʵ�鷽��һ����ȷȷ�����ʳɷ֣���˵������_________��
��ʵ����Ϊ��ֹNaOH��Һ���ʣ��ɲ�ȡʲô��ʩ_________��
��5��ij��ֽ���������������Ƶķ�ˮ�辭���������Ժ����ŷš�С��ȡ51g�÷�ˮ��Ʒ���뵽��ƿ�У���μ���10%��ϡ���ᣬ��ǡ����ȫ��Ӧʱ��������ϡ����49g������������Һ������������_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ����Լ��Zn 7%��ZnO 31%��Cu 50%��CuO 5%������Ϊ���ʣ����ʲ�����ˮ�������뷴Ӧ����������ͭ���ɵõ�����п������Ҫ������ͼ��ʾ�������м�����������ȴ��ԭ�¶ȣ�

�й���������������˵���������
A.��ҺA������������
B.��ҺA������С����ҺB
C.��ҺC�����ʵ���������С����ҺB
D.��ҺA��ZnSO4����������CuSO4
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com