
【题目】盛有等质量、等质量分数稀盐酸的两只烧杯,放在托盘天平的左右两盘,天平平衡,在左盘烧杯中加入 10gCaCO3,恰好完全反应,若要使天平重新平衡,则右盘烧杯中应加入的下列物质是( )
A.5.6g 铁和锌
B.10g 镁和氧化镁
C.10g 碳酸镁
D.10g 碳酸镁和碳酸锌
【答案】C
【解析】
设10g碳酸钙反应消耗的HCl的质量为x,生成的二氧化碳的质量为y;则
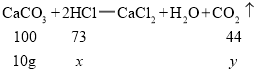
![]()
x=7.3g;
![]()
y=4.4g;
即左盘净增加为10g-4.4g=5.6g;
A、由于5.6g铁和锌,无论是否完全反应都会生成氢气,导致质量增加小于5.6g,所以不能平衡,说法错误;
B、根据HCl的质量求算反应的镁的质量以及生成氢气的质量:
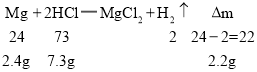
即使完全是镁也只会增加7.8g而非5.6g,如果含有氧化镁导致质量变化更大,说法错误;
C、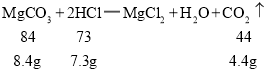 ,加入10g碳酸镁,则质量增加量为10g-4.4g=5.6g,平衡,说法正确;
,加入10g碳酸镁,则质量增加量为10g-4.4g=5.6g,平衡,说法正确;
D、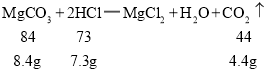 ,加入10g碳酸镁,则质量增加量为10g-4.4g=5.6g。
,加入10g碳酸镁,则质量增加量为10g-4.4g=5.6g。
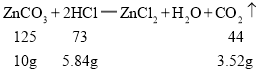 ,加入10g碳酸锌,则质量增加量为10g-3.52g=6.48。
,加入10g碳酸锌,则质量增加量为10g-3.52g=6.48。
所以10g碳酸镁和碳酸锌,天平不平衡,说法错误;
故选:C。


科目:初中化学 来源: 题型:
【题目】某食品包装袋内的“脱氧剂”查阅资料发现其成分可能含有铁粉、碳粉、Na2CO3、NaCl、Fe2O3等,为确定其成分,进行了如下实验:
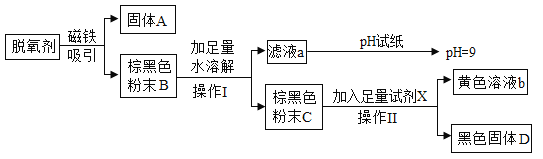
(1)固体A是_____________。
(2)操作I和操作Ⅱ为___________。
(3)加入的足量试剂X是_______。
(4)通过实验可知,脱氧剂中一定含有的物质是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学教材中的一些实验,按要求回答下列问题:
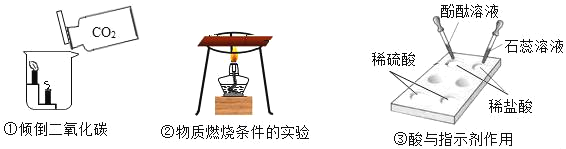
(1)实验①的实验现象为_____;
(2)实验②中薄铜片上的乒乓球碎片先燃烧,滤纸碎片后燃烧,说明燃烧的条件之一是:_____;
(3)实验③在白色点滴板上进行实验的优点有_____。(答一条)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少是,0表示物质质量不变),下列说法正确的是
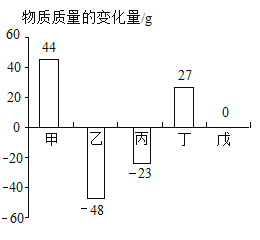
A.该反应一定属于化合反应或分解反应
B.戊一定是该反应的催化剂
C.参加反应的乙、丙的质量比一定为48:23
D.该反应中甲、丁的相对分子质量之比一定为44:27
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近日,北航化学教授杨军关于“虫子吃塑料”的演讲引发关注。研究表明,某种虫子能以塑料为食,能将聚乙烯、聚苯乙烯等降解矿化为CO2或同化为虫体脂肪。
(1)塑料、合成纤维和_________属于合成材料。
(2)昆虫降解塑料属于______变化,它可有效解决的环境问题是________。
(3)聚乙烯由乙烯经聚合制得,乙烯和聚乙烯都由碳、氢元素组成,但它们的化学性质不同,其原因是_______。
下图是乙烯燃烧的微观示意图:

该反应的化学方程式为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】盛有等质量、等质量分数稀盐酸的两只烧杯,放在托盘天平的左右两盘,天平平衡,在左盘烧杯中加入 10gCaCO3,恰好完全反应,若要使天平重新平衡,则右盘烧杯中应加入的下列物质是( )
A.5.6g 铁和锌
B.10g 镁和氧化镁
C.10g 碳酸镁
D.10g 碳酸镁和碳酸锌
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】 经过监测和治理,我国的土壤质量已经得到了很好的改善,但个别地区仍然存在盐碱地。
(一) 某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并进行探究。
[查阅资料]
①枸杞和合欢均可在轻度盐碱地中生存。
②盐碱地显碱性。
③该土样中的可溶性物质只含NaCl, CaCl2和Na2CO3.
[探究过程]
(1)甲组探究土样的酸碱度:将土壤样品与蒸馏水按1:5的质量在烧杯中混合,充分搅拌后静置,用PH试纸测澄清液体的酸碱度。得到的结果是该土样的pH___________7 (填“>”、“<”或“=”)
(2)乙组探究土样的成分(如图所示)向土样中加入足量的蒸馏水,发生反应的化学方程式_______________。经过操作Ⅰ_________(填操作名称)后同学们对溶液Ⅰ中的溶质成分很感兴趣,作出如下猜想:
猜想一:只含NaCl
猜想二:含NaCl、CaCl2
猜想三:含NaCl、Na2CO3

设计实验,继续探究:
验证猜想所用试剂 | 实验现象 | 实验结果 | |
方案一 | AgNO3溶液和稀硝酸 | 有白色沉淀生成 | 猜想①正确 |
方案二 | Na2CO3溶液 | ___________________ | 猜想②不正确 |
方案三 | ___________________ | 有气体生成 | 猜想③正确 |
[反思评价]
通过交流,甲组认为乙组的方案不太严谨, 理由是___________________。
[总结提升]改良我的盐碱地,充分利用土地资源,造福人民,我们任重而道远。以下建议你认为正确的是___________________。
a.轻度盐碱地可以种植枸杞
b.可以用熟石灰改良盐碱地
c.盐碱地应避免施用碱性化肥
(二)化学研究从定性到定量的过渡使化学能真正服务于社会生产。确定成分后兴趣小组的同学又开展了测定Na2CO3和NaCl混合固体中Na2CO3含量的探究实验,他们设计了如下的实验

(1)如图甲所示(铁夹夹持的仪器是注射器),把一定量的混合物与足量稀硫酸反应后,测定产生的二氧化碳气体的体积,检查该装置的气密性的方法是:_____________________。
(2)小明同学提出用图乙代替图甲中的收集装置,则所测CO2气体的体积____________(填“偏大”、“偏小”、“不变”) ;有同学对乙装置中的缺陷提出三种改进方案:A方案:将广口瓶中的水改为饱和的CO2水溶液;B方案:将广口瓶中的水改为氢氧化钠稀溶液;C方案:在广口瓶中的水面上覆盖一层植物油.你认为错误的方案是______________(填字母代号) ;
(3)小宇同学用图丙装置测定CO2的质量.丙装置存在一些缺陷, 这些缺陷会造成实验结果偏大,请简要分析出原因______________(写出其中一条即可) .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室欲测定一瓶标签破损的稀硫酸中溶质的质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。分析并计算:
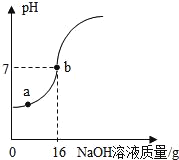
(1)a点溶液中含有的离子是_____。
(2)当pH=7时,消耗氢氧化钠溶液中NaOH质量为_____g。
(3)计算稀H2SO4中溶质的质量分数。_____
(4)计算恰好完全反应时所得溶液的溶质质量分数。_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com