
| A. | 铝和硫酸铜溶液 | B. | 硫酸和烧碱溶液 | ||
| C. | 氧化铁固体和盐酸 | D. | 碳酸钙固体和盐酸 |
分析 铝和硫酸铜反应生成硫酸铝和铜,每2个铝原子置换出3个铜原子;
稀硫酸和氢氧化钠反应生成硫酸钠和水,反应前后溶液质量不变;
氧化铁和盐酸反应生成氯化铁和水,随着反应的进行,氧化铁不断溶解,溶液质量变大;
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,每反应100份质量的碳酸钙,生成44份质量的二氧化碳,反应过程中溶液质量增大.
解答 解:A、铝和硫酸铜反应生成硫酸铝和铜,随着反应的进行,溶液质量减小;
B、稀硫酸和氢氧化钠反应生成硫酸钠和水,反应前后溶液总质量保持不变;
C、氧化铁和盐酸反应生成氯化铁和水,随着反应的进行,溶液质量增大;
D、碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,随着反应的进行,溶液质量增大.
故选:B.
点评 本题主要考查物质的性质,只有掌握了物质的性质,才能够对各种问题作出正确的解答.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:初中化学 来源: 题型:解答题
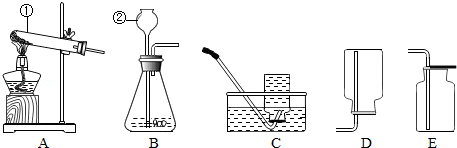
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
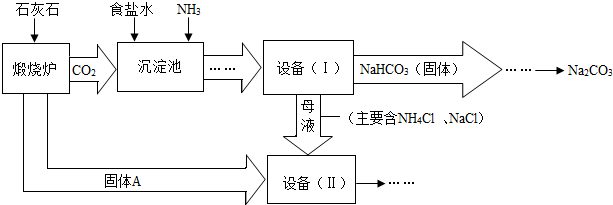
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 浓硫酸溅到皮肤上应先用大量水冲洗,再涂3%-5%的碳酸氢钠溶液 | |
| B. | 干粉灭火器主要用于扑灭图书、档案、精密仪器的火灾 | |
| C. | 普通导线外层的塑料是热塑性的聚氯乙烯塑料 | |
| D. | 不慎把烧碱溶液沾到皮肤上,应立即用较多水冲洗,然后涂上硼酸溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 加入的试剂或操作 |
| A | NaCl 溶液(CaCl2) | 过量的碳酸钠溶液,过滤 |
| B | CaCO3(CaO) | 髙温煅烧 |
| C | Cu(NO3)2 溶液(AgN03) | 足量铜粉,过滤 |
| D | CO2(HC1) | 足量的氢氧化钠溶液,洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
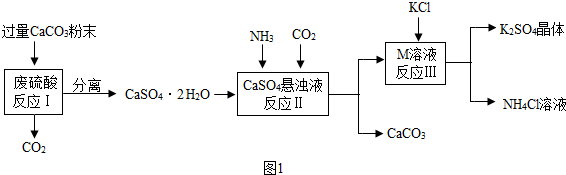
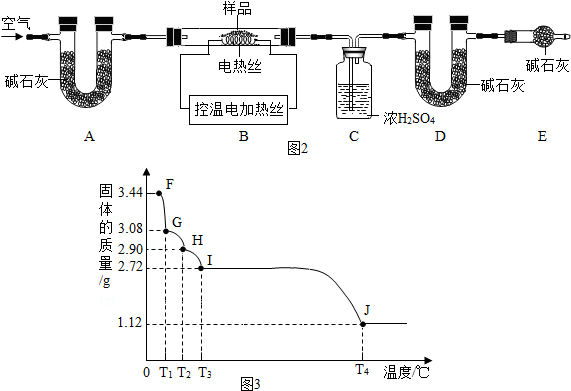
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com