
【题目】某化学兴趣小组研究一包久置的双吸剂的组成,初步研究得知其一定含有Fe、CaCO3和CaO或Ca(OH)2。可能含有Fe2O3。为进一步确定组成,他们取3g样品研碎,用磁铁充分吸引,得到剩余固体2.6g,按照下图流程进行定量实验:

(1)操作一、操作二都相同,该操作是______,使用玻璃棒是为了防止_____。
(2)溶液A中加入碳酸钠溶液发生的反应方程式为_____,判断加入的碳酸钠溶液是否过量的方法____。
(3)确定固体E是否洗涤干净的方法是_____。
(4)经计算固体C的质量,得出______(填“是”或“否”)含有Fe2O3。
【答案】过滤 液体溅出 ![]() 取上清液,继续滴加碳酸钠溶液,若无沉淀生成,则碳酸钠溶液过量 取最后一次洗涤液,加BaCl2或CaCl2或稀盐酸或无色酚酞试液等,如无现象,则已洗净 是
取上清液,继续滴加碳酸钠溶液,若无沉淀生成,则碳酸钠溶液过量 取最后一次洗涤液,加BaCl2或CaCl2或稀盐酸或无色酚酞试液等,如无现象,则已洗净 是
【解析】
(1)操作一、操作二都相同,都是进行固液分离,该操作是过滤,使用玻璃棒是为了防止液体溅出。
(2)样品 Fe、CaCO3和CaO或Ca(OH)2,可能含有Fe2O3,加入足量的水溶解得到溶液A,溶液A为氢氧化钙溶液,加入碳酸钠溶液,反应生成碳酸钙沉淀和氢氧化钠,发生的反应方程式为![]() ,判断加入的碳酸钠溶液是否过量的方法:取上清液,继续滴加碳酸钠溶液,若无沉淀生成,则碳酸钠溶液过量。
,判断加入的碳酸钠溶液是否过量的方法:取上清液,继续滴加碳酸钠溶液,若无沉淀生成,则碳酸钠溶液过量。
(3)确定固体E是否洗涤干净的方法是:取最后一次洗涤液,加BaCl2或CaCl2或稀盐酸或无色酚酞试液等,如无现象,则已洗净。
(4)由题意可知,固体C为碳酸钙或碳酸钙和氧化铁的混合物,固体C与足量稀盐酸反应生成4.4g气体(碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳),设产生4.4g二氧化碳,需要碳酸钙的质量为x,则
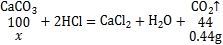
![]()
解得x=1g,而固体C为2g,故样品中含有Fe2O3。


 优学名师名题系列答案
优学名师名题系列答案科目:初中化学 来源: 题型:
【题目】学习化学后,我们学会了从微观角度认识物质。
(1)已知碳原子和氧原子的结构示意图分别为:  和
和 ,下列说法不正确的是. ______(填序号)。
,下列说法不正确的是. ______(填序号)。
A 两种原子的质子数相同
B 两种元素化学性质相同
C 两种原子的第一层电子数相同
D 两种元素位于同一周期
(2)氯化钾、金刚石、干冰三种物质中,由离子构成的物质是____(写化学式),保持干冰化学性质的粒子名称是______。
(3)下图是某反应的微观示意图, 请根据图示回答:
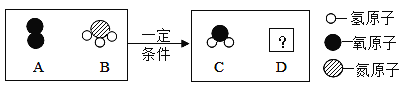
①若D为单质,则该反应的化学方程式为____;
②若A、B化学计量数之比为5:4,则D中含____种元素。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D 四个烧杯中分别盛有相等质量的水,在温度相同的条件下,向四个烧杯中分别加入 20 g、15 g、10 g、5 g 某物质,充分溶解后观察到如图所示的现象.请完成下列问题:
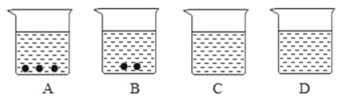
(1)在 A、B、C、D 四个烧杯中,_______ 中盛的一定是饱和溶液;_______ 中盛的一定不是饱和溶液;__________中盛的可能是饱和溶液.
(2)若固体是 KNO3,对盛有一定是饱和溶液的烧杯加热,随着温度升高,先变成不饱和溶液的是_____.
(3)在一定温度下,往 A、B 中加入相同质量的水,B 中固体刚好溶解,A 中固体能否全部溶解?_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用二氧化锰作过氧化氢分解制氧气的催化剂。

[提出问题]催化剂的用量对反应速率是否有影响?
[设计实验](1)实验装置如图所示。
(2)实验记录:每次用30mL10%的过氧化氢溶液,采用不同量的二氧化锰粉末作催化剂进行实验,测定相关数据记录于下表中:
实验序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
二氧化锰用量/g | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
待测数据 |
[分析](1)上述实验应该测定的“待测数据”可能是________________;装置中原有的空气对实验是否有干扰?____________,试说明原因:___________________________。
(2)若第2次实验比第3次实验的“待测数据”更_____________(选填“大”或“小”),说明催化剂的用量越多,反应越快。
[实验与结果]经多次实验证明,第1次实验至第7次实验中过氧化氢的分解速率依次加快,第7次实验至第10次实验所记录的“待测数据”无明显差异。
[结论]_________________________。
[拓展](1)实验后对二氧化锰进行回收、称量,发现其质量与反应前相比____________(选填“增大”“减小”或“不变”)。
(2)同一反应可用多种催化剂,为探究不同催化剂的催化效果,小组同学利用控制变量方法,探究氯化铁溶液和硫酸铜溶液对过氧化氢分解的催化效果,实验中的下列变量中,不需控制的是______________。
A 过氧化氢溶液的浓度和体积
B 催化剂的用量与浓度
C 反应温度,
D 反应开始的时间
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】孔雀石[化学式:Cu2(OH)2CO3]是一种古老的玉料,颜色酷似孔雀羽毛上斑点的绿色,用作装饰的孔雀石又被称为“翡翠蓝宝”和“蓝玉髓”。下列有关孔雀石的说法正确的是( )
A.属于有机物
B.其分子由碳、氢、氧、铜原子构成
C.铜元素显+1价
D.其中氧元素的质量分数最大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲转化为丙的微观过程,下列说法不正确的是( )
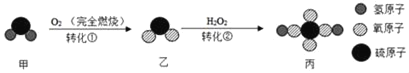
A. 转化①中甲和O2反应的分子个数比为1:1
B. 丙中硫元素的化合价是+6价
C. 转化②是化合反应
D. 反应前后原子种类不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们对市场上烧烤花蛤用的“锡纸”产生了浓厚兴趣。查阅资料获知:市售锡纸也称作铝箔、铝箔锡纸等。那么“锡纸”中的金属是什么呢?
![]()
(猜想与假设)同学们结合金属的颜色、活动性、价格等因素。猜想:可能是锡、铝、镁、铁、中的一种。
(查阅资料)金属锌似晶体状,室温下,锌较硬且相当脆;氧化铝的熔点2054℃;
(初步探究)同学们结合金属的主要的物理和化学特性设计了如下实验:
序号 | 实验方案 | 现象 | 结论 |
1 | _____ | 无明显现象 | 金属不可能是铁 |
2 | 用坩埚钳夹取打磨后的“锡纸”条,放在酒精灯上点燃。 | “锡纸”条熔化但没有滴落,也没燃烧。 | 金属不可能是_____ |
(深入探究)同学们对于“锡纸”到底是什么金属,进行了深入的实验探究。
(1)第一组同学将“锡纸”条卷成和铁钉一样粗细,先在20%的盐酸中浸泡至产生较多气泡,再取蒸馏水清洗,然后浸在蒸馏水中备用。浸泡在盐酸中目的是_____。
(2)将打磨后的铁钉和备用的“锡纸”条分别放入到装有5mL 15% 的稀盐酸中(如图所示)。观察到“锡纸”条表面产生的气泡速率比铁钉快。
(实验结论)制作“锡纸”的金属是_____。写出“锡纸”条与稀盐酸反应的化学方程式:_____。
(交流与反思)
(3)“锡纸”在酒精灯上加热,“锡纸”熔化但没有滴落的原因是:_____。
(4)第二组同学,将备用的“锡纸”条放入到装有硫酸锌溶液的试管中。一段时间后,未观察到明显现象。同学们讨论分析可能的原因是:①反应速率较慢,生成物太少;②_____。
(5)同学们在老师的帮助下,将3克烘干的备用“锡纸”片放入装有硫酸锌溶液的试管中,5分钟后,取出“锡纸”片,洗涤、烘干、称量。反应后金属质量范围是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们注意到了吗?随着现代化建设步伐的加快,我们的生活质量正在逐步提高。请你用所学的化学知识结合生活经验回答下列事例中的有关问题;
(1)走进厨房,你会发现煤气罐被方便、价廉的管道天然气代替了,天然气属于_____能源,其主要成分在空气中充分燃烧的化学方程式为_____。在厨房里,你还会发现用加了洗涤剂的水洗涤油腻的碗筷既快捷又干净,这是由于洗涤剂具有_____功能。
(2)走进干洗店作社会调查时,你会了解到有些干洗店用装有活性炭的新款干洗机代替旧款干洗机,可将有毒物质大约降至原来的![]() .这是利用了活性炭的_____性。
.这是利用了活性炭的_____性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂废液中含有氯化钠.氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如下图所示,
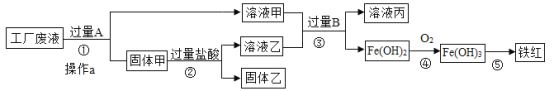
回答下列问题。
(1)加入过量A溶解后,再进行操作a时玻璃棒的作用是 。
(2)工厂废液中加入过量A反应的化学方程式为 。
(3)溶液甲中的金属离子是 (写离子符号)。
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是 (填序号)。
(5)铁红是炼铁的主要原料,写出用CO和铁红炼铁的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com