
���� ��֪ʶ����
���������ܹ�����ˮ�������ܺͶ�����̼��Ӧ����̼���ƺ�ˮ��
ϡ�����ܺ��������Ʒ�Ӧ�����Ȼ��ƺ�ˮ���ܺ�̼���Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼��
̼�����ܺ��������Ʒ�Ӧ����̼��Ƴ������������ƣ�
��������⡿
������̼��ʹ����ʯ��ˮ����ǣ�
���ݷ�Ӧ�Ļ�ѧ����ʽ���ṩ�����ݿ��Խ�����ط���ļ��㣮
��� �⣺��֪ʶ����
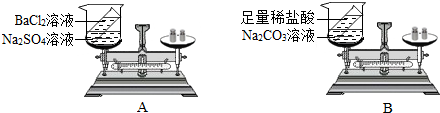
��1���������Ʋ��ܳ��ڷ��õ�ԭ���ǣ��������ƹ��岻�����տ����е�ˮ������������еĶ�����̼��Ӧ�����ʣ�
����������ƹ��岻�����տ����е�ˮ������������еĶ�����̼��Ӧ�����ʣ�
��2��ϡ�����ܺ��������Ʒ�Ӧ�����Ȼ��ƺ�ˮ���ܺ�̼���Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼��������������ķ�Ӧ��ѧ����ʽ�ǣ�NaOH+HCl=NaCl+H2O��Na2CO3+2HCl=2NaCl+H2O+CO2����
���NaOH+HCl=NaCl+H2O��Na2CO3+2HCl=2NaCl+H2O+CO2����
��3��̼�����ܺ��������Ʒ�Ӧ����̼��Ƴ������������ƣ���Ӧ�Ļ�ѧ����ʽΪ��Ca��OH��2+Na2CO3=2NaOH+CaCO3����
���Ca��OH��2+Na2CO3=2NaOH+CaCO3����
��������⡿
��1������ͬѧ�ж�ʯ��ˮ�Ƿ�����ķ����ǣ�ȡ�ϲ���Һ��������ͨ�������̼�������̼������Һ���������ǣ��а�ɫ��������������ʾʯ��ˮ������
���ȡ�ϲ���Һ��������ͨ�������̼�������̼������Һ���������ǣ��а�ɫ��������������ʾʯ��ˮ������
��2����ͬѧ������Ʒ�к��е�̼���Ƶ�����Ϊx��
Na2CO3+2HCl=2NaCl+H2O+CO2����
106 44
x 4.40g
$\frac{106}{x}$=$\frac{44}{4.40g}$��
x=10.6g��
��Ʒ��̼���Ƶ���������Ϊ��$\frac{10.6g}{16.40g}$��100%=64.6%��
����Ʒ��̼���Ƶ���������Ϊ64.6%��
��ͬѧ������Ʒ�к��е�̼���Ƶ�����Ϊy��
Ca��OH��2+Na2CO3=2NaOH+CaCO3����
106 100
y 10.00g
$\frac{106}{y}$=$\frac{100}{10.00g}$��
y=10.6g��
��Ʒ��̼���Ƶ���������Ϊ��$\frac{10.6g}{16.40g}$��100%=64.6%��
����Ʒ��̼���Ƶ���������Ϊ64.6%��
���� �������ʵ�飬��ѧ�ؽ���ʵ�顢����ʵ�飬�ǵó���ȷʵ����۵�ǰ�ᣬ���Ҫѧ�����ʵ�顢����ʵ�顢����ʵ�飬Ϊѧ�û�ѧ֪ʶ�춨������


 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ�鲽�� | Ԥ�ڵ�ʵ������ | ���� |
| ���ô�����ֽӴ���ֽ�ϵ���������ĩ�� �ڽ���ɫ���ʷ���С�Թ��У���������ϡ����۲��������μ�������NaOH��Һ�� | ���ֺ�ɫ��ĩ������ ��ɫ�����ܽ⣬��Һ�ʻ�ɫ���������ɫ���� | �������ijɷ������� ��ɫ������Fe203 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ͭ��Һ | B�� | �Ȼ�����Һ��ϡ���� | ||
| C�� | �Ѷ�����̼ͨ������ʯ��ˮ | D�� | ̼��ƹ����ϡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
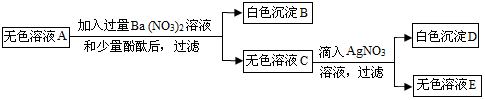
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
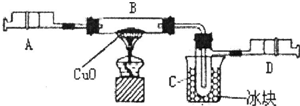
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
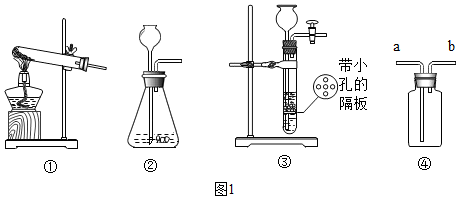
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | CO2��HCl��--ͨ������������������Һ������ | |
| B�� | NaCl����ɳ��--����������ˮ�ܽ⡢���ˡ����� | |
| C�� | K2SO4��K2CO3��--����������ϡ���ᣬ���� | |
| D�� | O2��H2O��--ͨ��������Ũ������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com