
【题目】下图是实验室制取气体的常用装置。请回答下列问题。
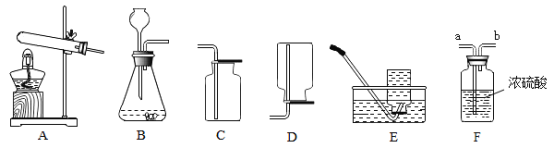
(1)实验室用装置A制取氧气的化学方程式为_______________________。
(2)装置B的错误是______________________。
(3)实验室用改正后的B装置制取二氧化碳,选用收集二氧化碳的最佳装置是______(填字母),若用F装置干燥二氧化碳气体,气体从_____ ( 填“a”或“b”)端通入。
【答案】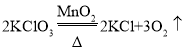 长颈漏斗下端没有伸入到液面以下 C a
长颈漏斗下端没有伸入到液面以下 C a
【解析】
(1)实验室用装置A制取氧气,由于是固体加热制取氧气,且试管口没有棉花团,所以是氯酸钾和二氧化锰加热生成氯化钾和氧气,对应的化学方程式为: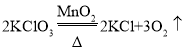 。
。
(2)装置B中的长颈漏斗没有伸入液面以下,这样会造成生成的气体从长颈漏斗逸出,所以长颈漏斗的末端要伸入液面以下;
(3)在实验室中常用大理石或石灰石(主要成分是碳酸钙)与稀盐酸反应来制取二氧化碳,二氧化碳的密度比空气大,且能溶于水,所以可用向上排空气法来收集,故选用收集二氧化碳的最佳装置是:C;若用F装置干燥二氧化碳气体,未干燥的气体从长管进入浓硫酸中,干燥后的气体从短管排出,故气体从a端通入。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:初中化学 来源: 题型:
【题目】最近,我国科学家成功合成新型催化剂,将CO2高效转化为甲醇(CH3OH)。这不仅可以缓解碳排放引起的温室效应,还将成为理想的能源补充形式。该化学反应的微观过程如下图所示。下列说法正确的是
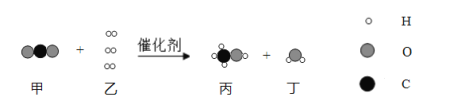
A. 该反应中四种物质均为化合物 B. 反应前后H元素的化合价不变
C. 参加反应的甲、乙分子个数比为1:3 D. 反应前后原子数目发生改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线。据图回答:
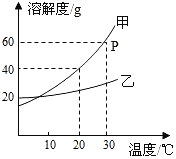
(1)P点表示的含义是____________.
(2)30°C时,将40g甲物质放入盛有50g水的烧杯中,所得溶液溶。质的质量分数为__________。
(3)若将上述烧杯内物质升温到50°C(不考虑水蒸发),溶液中变化的是_______(填字母)。
a 溶剂的质量 b 溶液的质量 c 溶质的质量分数
(4)从图中还可获得的信息是_________(答出一条)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】烧杯中盛有一定质量的MgO和Mg(OH)2的固体混合物,向其中加入氢元素质量分数为10%的稀硫酸100g,恰好完全反应,得到106g该温度下的不饱和溶液.下列数据中,与原固体混合物中Mg(OH)2的质量分数最接近的是( )
A.53.7%B.59.2%C.62.5%D.67.2%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学生测定的下列数据中不合理的是
A.用pH试纸测得某地水的pH为5.2
B.用10mL的量筒量取7.5mL的水
C.用托盘天平称得小苏打样品的质量为16.7 克
D.测得某粗盐中氯化钠的质量分数为90.5%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图为A、B、C三种固体物质的溶解度曲线,下列说法正确的是(____)
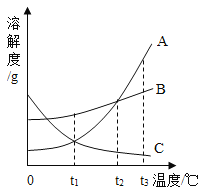
A 在t2℃时,A、C两种物质的溶解度相等
B A物质中混有少量B时可以采用蒸发结晶法提纯
C t3℃时,将三种物质的饱和溶液降温到t1℃,C溶液的溶质质量分数保持不变
D t3℃时,将等质的三种物质的饱和溶液降温到t2℃,剩余溶液中溶剂的多少_____(用“A、B、C”和“>”填空)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钙元素是一种重要的金属元素,它形成的物质种类很多。
(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂。
某实验探究小组的同学通过查阅资料得知:CaH2能与H2O反应生成Ca(OH)2和H2,请你写出该反应的化学方程式:_____。
(2)实验探究小组将Na2CO3溶液滴加到Ca (OH)2 溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
[提出问题]滤液中溶质的成分是什么?
[作出猜想]
猜想一: NaOH;.猜想二: NaOH 和Ca (OH)2; 猜想三: NaOH和_____;猜想四: NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,原因是_____;
[实验过程]
实验步骤 | 现象 | 结论 |
实验I :取滤液,向其中滴入适量Na2CO3溶液 | _____ | 猜想二不成立 |
实验Ⅱ:另取滤液,向其中加入足量_____ | 产生气泡 | 猜想_____成立 |
[拓展延伸]在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中A、B、C、D、E、F分别表示六种初中阶段常见的物质,B中含有钠元素,B和D的反应是纯碱制取烧碱的常见反应原理,A、C是两种盐溶液中的溶质,F是一种黑色粉末,片状则为银白色,E为2种元素的酸。图中用“一”表示两种物质之间能发生化学反应。用“→”表示一种物质可以转化为另一种物质,部分反应物和生成物及反应条件已略去,图中部分反应需在溶液中进行。请回答下列问题:
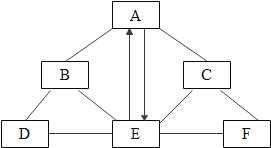
(1)D的化学式为________;F的化学式为_______;
(2)F片和足量E溶液反应的现象是_______;
(3)A和E相互转化的化学方程式是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钠的化合物在日常生活中有着广泛的应用。
(1)若将100g 9%的氯化钠溶液稀释为0.9%的氯化钠溶液,需要加入水的质量为____g。
(2)过氧化钠(Na2O2)和CO2反应,可以生成纯碱和氧气,所以可作为呼吸面具和潜水艇的供氧剂,请写出该反应的化学方程式:_______。
(3)《四川盐法志》记载,“敞锅熬盐”主要步骤为:①将黄卤和黑卤按比例混合;②放入敞口锅中加热浓缩,析出粗盐;③用“花水”冲洗粗盐得精品盐。请回答,步骤①中,黄卤所含杂质BaCl2和黑卤所含杂质MgSO4反应生成白色沉淀,该反应的化学方程式为________。步骤②中,析出粗盐的过程称为_______。步骤③用“花水”冲洗粗盐,既可除去表面的MgSO4和MgCl2杂质,又不损失NaCl.则“花水”应当是_____(填标号)
A蒸馏水 B饱和 NaCl溶液 C饱和NaOH溶液 D饱和BaCl2溶液
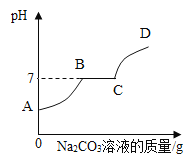
(4)某同学对实验室制取CO2后的剩余液体进行探究。首先向废液中滴加少量紫色石蕊试液,然后再逐滴加入Na2CO3溶液,溶液pH的变化如图所示。BC段的现象是______。向C点所示溶液中加入硝酸银溶液,发生反应的化学方程式________。
(5)食用纯碱中常含有少量的氯化钠。现取某食用纯碱样品10g,加入一定量的稀盐酸恰好完全反应,同时生成了3.3g气体。试计算该食用纯碱中Na2CO3的质量分数。_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com