
【题目】如图是M、N两种固体物质的溶解度曲线,下列说法正确的是()
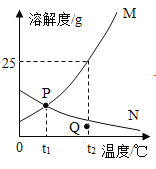
A.P点表示t1°C时M、N的饱和溶液中溶质质量相等
B.t2°C时100gM的饱和溶液中含有25gM
C.Q点对应的N溶液可通过降温变成P点对应的N溶液
D.t1°C时两物质的饱和溶液升温至t2°C,溶液中溶质质量分数M>N
【答案】D
【解析】
A、P点表示t1°C时M、N的溶解度相等,饱和溶液的质量未知,溶质质量不能确定,错误;
B、t2°C时M的溶解度是25 g,说明此时125 g M的饱和溶液中含有25 gM,错误;
C、Q点对应的N溶液为t2°C时N的不饱和溶液,P点对应的N溶液为t1°C时N的饱和溶液,且N的溶解度随温度升高而减小,通过降温的方法不能将Q点对应的N溶液变成P点对应的N溶液,错误;
D、M的溶解度随温度升高而增大,N的溶解度随温度升高而减小,将t1°C时两物质的饱和溶液升温至t2°C,得到t2°C时M的不饱和溶液,溶质质量分数与原t1°C时M的饱和溶液溶质质量分数相同,N的饱和溶液中有晶体析出,得到t2°C时N的饱和溶液,结合饱和溶液中溶质质量分数公式:![]() ,以及t1°C时M的溶解度>t2°C时N的溶解度,可知所得溶液中溶质质量分数大小关系为M>N,正确。
,以及t1°C时M的溶解度>t2°C时N的溶解度,可知所得溶液中溶质质量分数大小关系为M>N,正确。
故选D。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】在新中国成立70周年之际,2019年9月21日,第21届中国国际工业博览会圆满闭幕。太钢“手撕钢”捧回“中国国际工业博览会大奖”,彻底打破国外垄断。“手撕钢”是一款不锈钢箔材,其厚度为0.02毫米,仅有A4纸的四分之一,用手轻轻一撕就能撕开。主要应用于航空航天、高端电子、军工核电等方面。

(1)“手撕钢”属于_____(填“纯净物”或“混合物”)。
(2)“手撕钢”的学名是“宽幅超薄精密不锈带钢”,由此可知“手撕钢”在物理性能方面具有良好的_____性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予美国化学家斯坦利·惠廷厄姆、约翰·古德伊纳夫以及日本化学家吉野彰,以表彰他们对锂离子电池开发的贡献。如图是锂元素的部分信息,下列说法正确的是
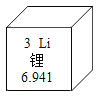
A.锂原子的最外层电子数为3
B.锂原子的质量是6.941
C.锂元素属于非金属元素
D.锂原子容易失去电子变成锂离子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学符号填空。
(1)3个氢分子_______ (2)镁元素_______
(3)硝酸根离子_______ (4)氢氧化铝中铝元素的化合价_______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合A、B、C、D、E图回答下列问题。

(1)写出A装置中仪器的名称:a___;b____。
(2)实验室用A装置制取CO2的化学方程式为_____。
(3)进行CO2性质实验时,观察到B中无明显现象,C中试液变红色,D中充有某气体的超薄气球由烧杯底部往上升,最后悬于烧杯中。B中无明显现象的原因是____,D中气球充入的气体可能是____(填序号)
A H2 B O2 C NH3 D SO2
(4)图E中四种方法都可以得到氧气,在初中化学实验室中,更符合环保、节能、安全要求的方法是___(填数字序号)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢氧化钠与稀盐酸反应观察不到明显现象,为了确定反应是否发生,丽丽小组同学设计了如下图所示的实验探究方案。
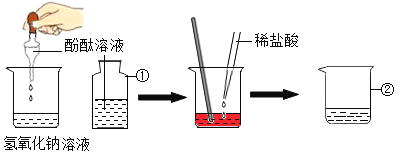
请回答下列问题:
(1)标号仪器的名称:①_____,②_____。
(2)玻璃棒在实验中的作用及目的_____。
(3)当观察到烧杯中溶液颜色_____时,说明酸碱恰好中和反应。
(4)该实验过程中发生反应的化学力程式_____。
(5)仿照填写下用圆圈内的空白,其反应的实质是_____。
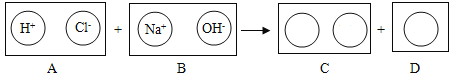
(6)若将50g质量分数7.3%的稀盐酸与50g质量分数8%的氢氧化钠溶液充分后,反应所得溶液的溶质质量分数是_____。
(7)酸、碱,盐水溶液导电是因为它们在水中溶解时能产成自由移动的离子,这个过程叫做电离。试着写出氢氧化钠的电离方程式_____。
(8)下列关于该实验方案中,能证明氢氧化钠与盐酸发生反应的序号是_____。
A 用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀盐酸,测得溶液的pH逐渐减小,最终小于7
B 用温度计测量氢氧化钠溶液在滴加稀盐酸前与后的温度,发现其明显上升
C 蒸发反应后所得的无色溶液得到白色的固体
D 向一定量NaOH溶液被中滴加稀盐酸、再滴加硫酸铜溶液,有蓝色沉淀生成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小雨阅读课外资料得知:过氧化氢分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是她对氧化铜产生了探究兴趣。
(提出问题)氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
(设计实验)小雨以生成等体积的氧气为标准,设计了下列三组实验(其他可能影响实验的因素均忽略)。
实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
① | 1.2g | — | |
② | 1.2g | 氧化铜0.5g | |
③ | 1.2g | 二氧化锰0.5g |
(1)上述实验应测量的“待测数据”是_____。
(2)若实验②比实验①的“待测数据”更_____(填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率。
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到![]() 黑色粉末,说明_____。
黑色粉末,说明_____。
(4)再将黑色粉末放入试管中,加入_____,若观察到_____,说明黑色粉末的化学性质在反应前后保持不变。
(预期结论)氧化铜也能作氯酸钾分解的催化剂。
(评价设计)你认为小雨设计实验③和实验②对比的目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铜器长期暴露在空气中会生成铜绿(俗称铜锈)。铜锈的主要成分是碱式碳酸铜,其化学式为![]() ,碱式碳酸铜不稳定,受热分解成黑色固体物质、无色气体和水。这种黑色固体和无色气体的成分是什么呢?
,碱式碳酸铜不稳定,受热分解成黑色固体物质、无色气体和水。这种黑色固体和无色气体的成分是什么呢?
(查阅资料)稀硫酸能与![]() 、
、![]() 等金属氧化物反应,生成盐和水。
等金属氧化物反应,生成盐和水。
(提出猜想)某同学对黑色固体、无色气体的成分做出了以下猜想:
①无色气体为二氧化碳;②黑色固体为氧化铜。
(实验验证)实验装置如图所示。
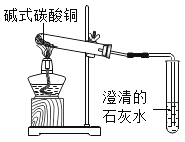
在此实验装置中,大试管的管口略向下倾斜的目的是_____。
(1)若猜想①正确,实验过程中应该看到澄清的石灰水_____,产生此现象的化学方程式是_____;在反应完全停止加热时,针对熄灭酒精灯和把导管移出液面这两步操作,你认为应该先进行的操作是_____。
(2)若猜想②正确,从装置中取下大试管并冷却到室温,然后向大试管中加入足量的稀硫酸,充分振荡,静置后能看到黑色固体消失,溶液由无色变为_____色,发生反应的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com