
【题目】甲、乙、丙三种物质的溶解度曲线如右图所示,据图回答:
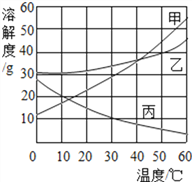
(1)30 ℃时,三种物质的溶解度由大到小的顺序为____________;
(2)要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是________________;
(3)50 ℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10 ℃时,析出晶体最多的是________,所得溶液中溶质质量分数最大的是_________。
 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:初中化学 来源: 题型:
【题目】加热氯酸钾和二氧化锰的混合物可制备氧气,该反应的化学方程式为____________________,但实验中发现有刺激性气味的气体产生。
(提出问题)刺激性气味的气体是什么呢?
(猜想假设)猜想一:臭氧(化学式为O3) 猜想二:HCl 猜想三:Cl2
同学们认为不需要实验验证就可以判断猜想_______________是错误的,理由为_______________。
(查阅资料)(1)C12+H2O===HC1O+HCl。
(2)臭氧在MnO2存在的情况下极易分解成氧气。
(3)氯气可使湿润的淀粉碘化钾试纸变蓝。
(实验探究)
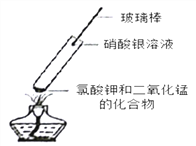
查阅资料后大家认为猜想一是错误的,理由为____________________________。他们进一步又做了如下实验:取氯酸钾和二氧化锰的混合物放人试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管口(如图),看到的现象是_____________,再将湿润的淀粉碘化钾试纸悬于试管口,试纸变_______________色,最终证明猜想三正确。
(反思拓展)
(1)欲证明二氧化锰是氯酸钾分解的催化剂,需证明二氧化锰的________、________在反应前后不变。
(2)自来水厂常用氯气来杀菌消毒,氯气和水反应后会产生H+、Clˉ和ClOˉ,而野外常用漂白粉[主要成分化学式为Ca(ClO)2]。你认为在水中起杀菌消毒作用的离子是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某研究性学习小组设计的几种装置,请你分析并回答下列问题:
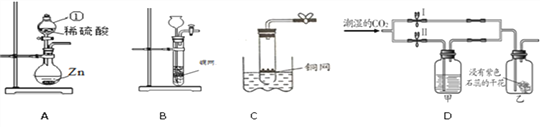
(1)图A中仪器①名称为________,发生反应的化学方程式为______________;
(2)用浓硫酸(溶质质量分数为98%,密度为1.84 g/mL)和水按照体积比为1︰10配制该实验所需的稀硫酸,所得稀硫酸的溶质质量分数约为________(保留到0.1%)。若对稀硫酸进行如下操作,溶液的pH因化学变化而升高的有______(填字母序号);
a.加少量水 b.加少量铁粉 c.加少量浓硫酸
(3)装置B是实验室常见的气体发生装置。源源同学从装置B得到启发,又用一支底部有一个小洞的试管和矿泉水瓶组合成装置C(夹持仪器都略去),用来制取二氧化碳,则C与B相比都具有的优点是__________,用装置B或C制取二氧化碳的化学反应方程式为___________;
(4)用装置D探究CO2的部分性质,若关闭Ⅱ阀,打开Ⅰ阀,紫色小花(用石蕊溶液染成)变红;若关闭Ⅰ阀,打开Ⅱ阀,紫色小花不变红,则甲瓶中所盛的试剂可能是______(填序号)。
①浓H2SO4 ②浓NaOH溶液 ③饱和NaCl溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是一盏废旧台灯,某实验小组的同学利用它进行观察分析并完成相关实验。
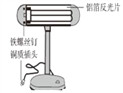
(1)小明发现台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的_______等发生了化学反应。
(2)小红发现铝箔反光片呈银白色,无锈迹,原因是铝表面有一层致密的氧化膜,生成该氧化膜的化学方程式为_____________________________。
(3)铁、铝、铜的金属活动性由强到弱的顺序为____________。为了验证三者的金属活动性顺序,小志从实验室领来氯化铝溶液、硫酸铜溶液,并利用台灯提供的一种金属进行实验,即达到了实验目的。实验中发生反应的化学方程式为_________。实验结束后,发现滤液仍呈蓝色,则所得滤液中一定含有的阳离子是___________________________(填离子符号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现取8.0 g石灰石样品放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5 g时,烧杯内物质总质量为42.3 g(气体全部逸出),产生气体的质量与加入的稀盐酸的质量关系如图所示。(友情提示:石灰石样品中的杂质不溶于水,也不发生反应)试计算 :
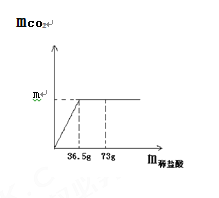
(1)m = ________。
(2)该石灰石样品中碳酸钙的质量分数是多少__________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
①称取25.0g石灰石样品,平均分成两份,并分别加工成块状和粉末状;
②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如下图所示。请回答:
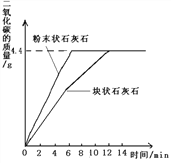
(1)由图中曲线分析得出,影响该化学反应速率的因素是:__________;
(2)每份样品充分反应后.生成二氧化碳的质量为____________.
(3)若每份样品中加入l00.0g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数为_____________。(要求写出计算过程.不考虑水、氯化氢的逸出.结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析甲乙两种固体的溶解度曲线,回答下列问题:
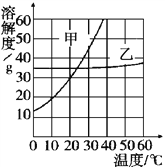
(1)观察图像,溶解度受温度影响不大的物质是_____________
(2)欲使30℃甲的饱和溶液转化为不饱和溶液,除可采用升高温度的方法外,还可采用的方法 ________________________
(3)在20℃时,将25克甲放入100克水中,充分搅拌后,从溶液是否饱和的角度看,所得溶液在20℃是_____溶液,此时溶质的质量分数为__________________
(4)甲中混有少量乙,提纯甲的方法____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硬水受热后会产生水垢,水垢的主要成分是 CaCO3 和 Mg(OH)2。实验室由水垢制取纯净 CaCl2 固体的流程如下:(水垢中其它成分不参与反应),请按要求填空:
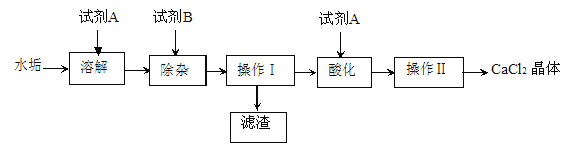
⑴ 试剂 A 的名称为_______________。
⑵ 试剂 B 的化学式是___________,若加入的试剂A、B都是过量的,则加入试剂 B 发生的非中和反应的化学反应方程式是_______________。操作Ⅰ的名称是__________,该操作中除用到玻璃仪器外,还需要的实验用品有_________。
⑶ 酸化过程加试剂 A 的作用__________________________。
⑷“操作Ⅱ”包含的操作有:蒸发浓缩、______________、过滤、洗涤、干燥等。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碱式硫酸铁(Fex(OH)y(SO4)z)可做净水剂、颜料和药物,某兴趣小组利用硫酸厂的烧渣(主要成分为:铁的氧化物、少量FeS及SiO2),在实验室制备碱式硫酸铁,主要流程如下:
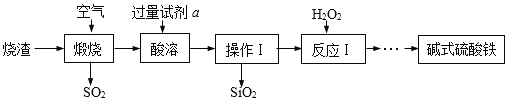
(1)操作Ⅰ中所用的玻璃仪器有烧杯、漏斗、____。
(2)煅烧时产生的SO2可选用石灰乳而不用澄清石灰水吸收的原因是_______。
(3)酸溶时加入的试剂a是_____(填序号)。
a.H2SO4 b.HCl c.HNO3
(4)反应Ⅰ中加双氧水的目的是为了将酸性FeSO4溶液氧化为Fe2(SO4)3,反应的化学方程式为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com