
用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示:
(1)该实验是将(选填“稀盐酸”或“氢氧化钠溶液”)滴 加到另一种溶液中,该反应的基本类型是 。
(2)当加入溶液的质量a为20 g时,求所得溶液中溶质的质量。
(1)氢氧化钠溶液复分解反应 (2)2.9克
解析试题分析:(1)从图示信息溶液的pH由小于7到等于7最后再到大于7可知,该反应是把氢氧化钠溶液滴加到稀盐酸中,该反应是酸碱中和反应,属于基本反应类型——复分解反应。
(2)从图示信息可知,当加入溶液的质量为a克时,氢氧化钠溶液与稀盐酸恰好完全反应,此时所得溶液中溶质的质量是氯化钠。根据氢氧化钠溶液的质量及其质量分数可以计算出纯氢氧化钠的质量,然后结合氢氧化钠与稀盐酸反应的化学方程式便可求出溶质氯化钠的质量。
解:设所得溶质质量为x,则
NaOH + HCl =" NaCl+" H2O
40 58.5
20g×10%x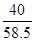 =
= 
x=2.93 g
答:当加入溶液的质量a为20 g时,所得溶液中溶质的质量为2.93 g。
考点:酸碱中和反应,根据化学方程式的计算。


 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:初中化学 来源: 题型:计算题
在电缆生产过程中会产生一定量的含铜废料.据报道,在通入空气并加热的条件下,铜与稀硫酸反应转化为硫酸铜,该反应的化学方程式为:2Cu+2H2SO4+O2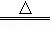 2CuSO4+2H2O.若用一定量溶质的质量分数为9.8%的稀硫酸恰好处理2000g含铜3.2%的废料(假设其他杂质不和硫酸反应且不溶于水),求反应后所得硫酸铜溶液中溶质的质量分数.
2CuSO4+2H2O.若用一定量溶质的质量分数为9.8%的稀硫酸恰好处理2000g含铜3.2%的废料(假设其他杂质不和硫酸反应且不溶于水),求反应后所得硫酸铜溶液中溶质的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为测定实验室中某过氧化氢溶液的溶质质量分数,小明取25.0g过氧化氢溶液放入烧杯中,然后进行如图所示的实验,反应的化学方程式是2H2O2 O2↑+2H2O.请计算:
O2↑+2H2O.请计算:
(1)反应后产生氧气的质量为 g。
(2)此过氧化氢溶液的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
我国首台使用二甲醚为燃料的城市客车有效地解决了公交车冒黑烟的问题.
(1)已知二甲醚的化学式为C2H6O,二甲醚的相对分子质量是 ,其中碳、氢元素的质量比为 。
(2)二甲醚在空气中完全燃烧生成二氧化碳和水,请计算完全燃烧92g二甲醚需要氧气多少克?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).如图所示:
超市销售的一种加碘盐标签上的部分文字说明.请回答下列问题:
(1)碘酸钾中钾、碘、氧三种元素质量比为 .
(2)每袋该食盐中碘元素的质量 mg.
(3)中国营养学会推荐:一个18岁的青年每天摄入碘元素的质量为0.15mg.假设碘的来源仅靠这种加碘食盐,该青年每天摄入这种食盐应为 g.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为减少龋齿,制造口香糖时常用木糖醇(C5H12O5)代替蔗糖.
(1)木糖醇的相对分子质量为 ;
(2)一个木糖醇分子中有 个原子,分子中碳、氢、氧原子的个数比为 ;
(3)木糖醇中碳元素的质量分数为 (结果保留至0.1%).
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
为测定一瓶失去标签的过氧化氢溶液的溶质质量分数,某同学取50.0g过氧化氢溶液放入烧杯中,然后加入2.0g二氧化锰,等不再放出气体,称得烧杯中剩余物质的总质量为50.4g.计算:
(1)过氧化氢中氢元素和氧元素的质量比为 .
(2)此过氧化氢溶液的溶质质量分数.(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
铜镁合金具有优良的导电性,常用作飞机天线等导电材料.欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜合金20g放入烧杯,将280g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
| 剩余固体质量/g | 18.2 | 16.4 | 14.6 | 13.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
73g质量分数为20%的盐酸与足量的大理石反应,生成二氧化碳的质量是多少?这些二氧化碳的体积(标准状况)是多少?(在标准状况下,二氧化碳的密度为1.977g/L)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com