
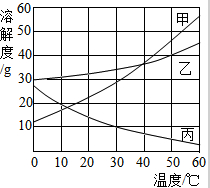
 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而丙的溶解度随温度的升高而减少;50℃时,乙物质的溶解度是40g,把50g乙物质放入100g水中,充分搅拌,所得溶液的质量=40g+100g=140g;50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是甲,所得溶液中溶剂质量最小的是甲,因为降温后溶剂质量不变,甲的溶解度最大,因此甲中的溶剂最少.
解答 解:(1)50℃时,乙物质的溶解度是40g,把50g乙物质放入100g水中,充分搅拌,所得溶液的质量=40g+100g=140g;故答案为:140g
(2)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是甲,所得溶液中溶剂质量最小的是甲,因为降温后溶剂质量不变,甲的溶解度最大,因此甲中的溶剂最少;故答案为:甲;甲;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | H2SO4、Na2SO4、KNO3、HCl | B. | CuSO4、H2SO4、NaCl、CaCl2 | ||
| C. | KOH、NaCl、NH4Cl、NaNO3 | D. | H2SO4、MgCl2、NaNO3、Ba(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  甲中氢氧化钠潮解说明氢氧化钠具有吸水性 | |
| B. |  乙中生石灰放入水中放热说明生石灰溶于水 | |
| C. |  丙中瓶塞跳起说明做功可以改变物体的内能 | |
| D. | 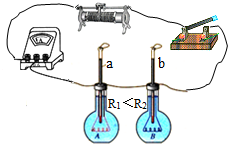 丁中玻璃管内液面上升高度不同说明电热的多少与电阻的大小有关 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 稀有气体做焊接金属时的保护气 | B. | 熟石灰做建筑材料 | ||
| C. | 浓硫酸做干燥剂 | D. | 氢氧化钠可用来去除油污 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 取一定量的剩余固体于试管中加足量的水振荡、滴入酚酞溶液. 取一定量的剩余固体于试管中加入足量的稀盐酸. | 观察到溶液变红 观察到有气泡产生 | 固体中有氧化钙 固体中有碳酸钙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com