
【题目】质量守恒定律的定量研究对化学科学发展具有重大意义。
(1)如图为某化学反应的微观模拟图,“![]() ”和“
”和“![]() ”分别表示两种不同的原子:
”分别表示两种不同的原子:
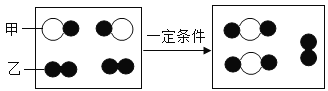
由微粒甲聚集成的物质____________________(填“可能”或“不可能”)是氧化物,参加反应的甲、乙两种反应物分子的个数比为____________________。
(2)由上述实验可知,在化学反应前后,一定不变的是____________________(填数字序号)。
①原子种类②原子数目③分子种类④分子数目⑤元素种类⑥物质种类
 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:
【题目】如图为甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
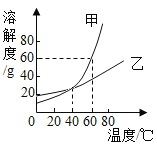
A.20℃时,甲物质的溶解度比乙物质的溶解度大
B.40℃时,甲、乙两种物质的饱和溶液中溶质质量分数相等
C.甲物质中混有少量乙物质,采用蒸发结晶的方法提纯甲物质
D.60℃时,将80g甲物质放入100g 水中,所得溶液中溶质质量分数为80%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用如图所示的装置进行水的电解实验时,有以下描述:

①甲试管应该连接在电源的正极
②甲、乙两试管收集到的气体的质量比约为2∶1
③甲试管内产生的气体能燃烧,且燃烧时火焰呈淡蓝色
④乙试管内产生的气体能使带火星的木条复燃
以上描述中错误的是( )
A. ①②③④ B. ③ C. ①② D. ①②③
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年5月18日,中国又创下一项世界第一,在我国海域试开采可燃冰获得成功。预计在 2030年以前可燃冰资源会得到商业性开发利用,将在一定程度上缓解化石能源面临被耗尽的危险。可燃冰中的主要可燃成分是甲烷。
(1)目前使用的主要化石燃料有煤、______和天然气等。
(2)甲烷燃烧的化学方程式是_______。
(3)可燃冰属于未来的新能源,下列不属于新能源的是________(填序号)。
A.汽油 B.太阳能 C.氢能 D.核能
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,为鉴别H2、CO、CH4三种气体,分别把它们的燃烧产物依次通过甲、乙两装置,甲瓶中为浓硫酸,乙瓶中为澄清石灰水。(浓H2SO4有吸水性)
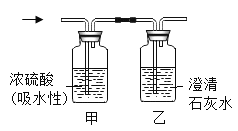
(1)若甲瓶中物质的质量增加,乙瓶中物质的质量不变,则燃烧的气体为_________,化学方程式为_________。
(2)若甲瓶中物质的质量不变,乙瓶中生成白色沉淀,则燃烧的气体为_________,燃烧的化学方程式为_______。
(3)若甲,乙两瓶中物质的质量都增加,则燃烧的气体为_________;若乙的质量增加2.2g,则甲的质量增加________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3)。下图是超市销售的一种袋装加碘盐标签上的部分文字说明。请回答下列问题:

(1)碘酸钾的相对分子质量为____________________________;
(2)中国营养学会推荐:一个18岁的青年每天摄入碘元素的质量为0.15mg。假设碘的来源仅靠这种加碘食盐,该青年每天摄入这种食盐应为____________________________g。
(3)食用碘盐的国家标准规定每千克食盐中含碘量为25士5mg。某地工商部门在对商品进行检测中,测得某袋碘盐(500g/袋)中碘酸钾的质量为21.4mg,请通过计算判断碘盐中碘元素是否符合国家标准______。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学研究型学习小组通过实验研究高炉炼铁的化学原理,设计了如图实验装置,请回答:
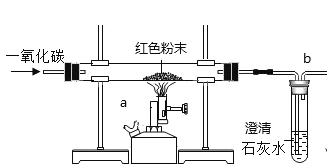
(1)实验过程中,为什么要先通入一氧化碳后加热?_____
(2)写出a中发生反应的化学方程式______
(3)该装置的不足之处是什么?_______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象分别与选项中的操作相对应,其中合理的是
A.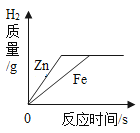 足量Zn、Fe分别与等质量、等浓度的稀硫酸反应
足量Zn、Fe分别与等质量、等浓度的稀硫酸反应
B.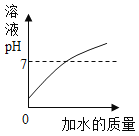 向一定量的稀盐酸中不断加水
向一定量的稀盐酸中不断加水
C. 实验室加热高锰酸钾制取氧气
实验室加热高锰酸钾制取氧气
D.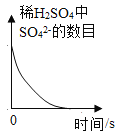 向一定质量的稀硫酸中加入锌粒
向一定质量的稀硫酸中加入锌粒
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的应用与金属导热性有关的是_____。
A 铁锤 B 铁锅 C 菜刀
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的_____。
II.铁的冶炼
工业炼铁的主要反应原理是在高温下CO夺取铁矿石里的氧,将铁还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:_____;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能_____。
Ⅲ.铁的活动性探究
现用一定量的AgNO3和Cu (NO3)2混合溶液,进行了如下图所示的实验,并对溶液A和固体B的成分进行了分析和研究。
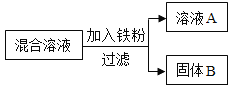
(提出问题)溶液A中的溶质成分可能有哪些?
(作出猜想)
①只有Fe(NO3)2
②有Fe(NO3)2、AgNO3
③有Fe(NO3)2、Cu(NO3)2
④有Fe(NO3)2、Cu(NO3)2、AgNO3
(交流讨论)不合理的猜想是_____(填序号)。
(实验探究)根据下表中的实验步骤及现象,完成表中的实验结论。
实验步骤 | 现象 | 实验结论 |
取少量固体B,滴加稀盐酸 | 有气泡产生 | 溶液A中的溶质成分符合猜想_____(填序号),固体B中有_____种金属。 |
Ⅳ.生铁中铁含量的测定
某课外兴趣小组测定生铁(含杂质的铁,杂质既不溶于水也不溶于酸)中铁的质量分数,他们取6份样品,分别与稀硫酸反应。测得数据如下,请根据有关信息回答问题。
实验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
取样品质量(g) | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 | 30.0 |
取稀硫酸质量(g) | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 | 300.0 |
产生气体质量(g) | 0.2 | 0.4 | 0.6 | 0.8 | 1.0 | 1.05 |
(1)第5次实验结束后,所得溶液中溶质的化学式为_____。
(2)所用稀硫酸中溶质的质量分数为_____。
(3)若配制上述浓度的稀硫酸100克,则需质量分数为98%的浓硫酸_____克。
(4)计算该样品中铁的质量分数是_____。(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com