
【题目】铝、铁、铜是我们生活中常见的金属。
(1)铝的利用比铜、铁晚是因为金属大规模开发和利用的先后顺序与_____(填字母)有关。
A 金属的活动性
B 金属的导电性
C 金属在底壳中的含量
(2)铝具有很好的抗腐蚀性能,原因是_____。
(3)化学新材料的应用,使人们的生活质量不断提高。如图是不同年代常用的水管。

①图示所有水管中,含有的金属元素是_____。
②每年全世界钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失,铁在空气中锈蚀,实际上是铁跟_____共同作用的结果;工业上常用稀盐酸来除铁锈(Fe2O3),该反应的化学方程式是_____。请你提出一种防止铁制品锈蚀的方法:_____。
③铁丝在空气中不能燃烧却在氧气中剧烈燃烧,其燃烧的化学方程式为_____。
(4)印刷铜制电路板的“腐蚀性”为与FeCl3溶液反应,化学方程式分别为①Cu+2FeCl3===2FeCl2+CuCl2;②Fe+2FeCl3===3X。则②中X的化学式为_____。
【答案】(1)A;(2)铝表面有一层致密的氧化铝保护膜,从而阻止铝进一步被氧化;
(3)①Fe、Zn;②氧气( 或空气)和水;6HCl+Fe2O3=2FeCl3+3 H2O,在铁制品表面涂漆;
③3Fe+2O2![]() Fe3O4
Fe3O4
(4)FeCl2
【解析】
试题(1)地壳里含量最高的是金属铝,但铝开发利用的时间在铜和铁之后,说明金属大规模开发、利用的先后顺序与地壳里金属含量无关,与金属的导电性也无关。金属大规模开发利用主要和金属的活动性有关,活动性弱的金属容易以单质形式存在,易被开发和利用;活动性强的金属一般以化合物形式存在,有的还比较难冶炼;
(2)根据铝与空气中的氧气反应生成的氧化物的特点分析。铝具有很好的抗腐蚀性能,原因是铝表面有一层致密的氧化铝保护膜,从而阻止铝进一步被氧化;
(3)①根据水管中含有的金属元素回答。在水管中含有的金属元素有Fe、Zn;
②根据铁生锈的条件回答。铁在空气中锈蚀,实际上是铁跟氧气( 或空气)和水共同作用的结果,工业上常用稀盐酸来除铁锈(Fe203),该反应的化学方程式是6HCl+Fe2O3=2FeCl3+3 H2O;由铁生锈的条件可知防止铁生锈的措施有:在铁制品表面涂漆,保持铁制品表面的洁净干燥等;
③铁在氧气中燃烧生成了四氧化三铁,反应的方程式是:3Fe+2O2![]() Fe3O4;
Fe3O4;
(4)根据质量守恒定律反应前后原子的种类和数目不变分析在Fe+2FeCl3=3X的左边有铁原子3个,氯原子6个,由于反应前后原子的种类和数目不变,则每个X中含有一个铁原子和2个氯原子,所以化学式是:FeCl2。


科目:初中化学 来源: 题型:
【题目】如图为甲、乙、丙、丁四种常见金属与盐酸反应的比较示意图.

(1)上述四种金属可以分为两类,其中除一种金属外,可以归为一类的是______等几种金属.
(2)若乙是金属Zn,则丙可能是______,请你说出理由是______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验设计能达到实验目的的是
选项 | A | B | C | D |
实验 目的 | 鉴别氢氧化钠、碳酸钠溶液 | 探究铁生锈的条件 | 证明CO2能和水反应 | 比较锌和铁的金属活动性强弱 |
实验 设计 |
|
|
|
|
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组对铜丝与稀硝酸的反应产生了兴趣,于是进行了以下实验:
知识卡片:
a.铜跟稀硝酸在室温下反应的化学方程式是3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
b.NO气体无色,难溶于水,很容易与O2反应生成红棕色的
NO2气体,NO2容易与水反应生成硝酸和NO。
(1)用如图装置制取NO气体,

稀硝酸应该装入_______中,当反应开始时,圆底烧瓶中可以观察到的现象是_______,溶液变为蓝色。
(2)下列哪些装置不宜用于实验室制NO气体_______(填装置序号)。
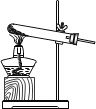
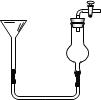
![]()
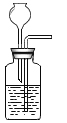
A B C D
(3)收集NO可以选择下列哪些装置_______。
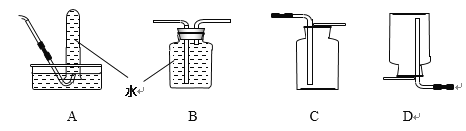
查看答案和解析>>
科目:初中化学 来源: 题型:
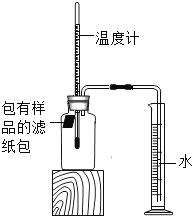
【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表。
序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
1 | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
3 | …… | 100 | 70 | 约480 |
(1)实验①和②说明NaCl可以_____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是_____。
(4)已知含碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成_____。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_____(小数点后保留1位)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学为探究Zn、Fe、Cu三种金属的活动性,设计了下列三组实验:①将Zn、Fe、Cu三种金属分别插入到稀硫酸中,②将Zn片插入到硫酸铜溶液中 ③将Cu片插入到硫酸亚铁溶液中,将Fe片插入到硫酸锌溶液中。其中可以达到目的的是( )
A. ①③
B. ③
C. ①②③
D. ②③
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有________产生,反应的化学方程式是________________________________________________________。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
试管(盛有同体积同浓度的盐酸) | ① | ② | ③ | ④ |
镁条长度 | 1cm | 2cm | 3cm | 4cm |
相同的实验现象(省略题干现象) | 快速反应,试管发热,镁条全部消失 | |||
沉淀量差异(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
[得出结论]镁条与盐酸反应产生白色沉淀与________有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是____________________(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | ________,白色沉淀________ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀________ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是: |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一些物质的近似pH如图,下列有关说法正确的是( )
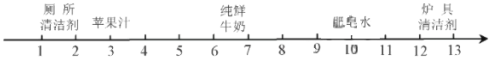
A. 苹果汁的酸性比纯鲜牛奶的酸性弱。
B. 肥皂水的碱性比炉具清洁剂的碱性强
C. 厕所清洁剂与炉具清洁剂能混用
D. 人被某些蚊虫叮咬后可涂抹肥皂水以减轻痛痒
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学设计的“从含铜电缆废料中提取铜”的实验方案如下:
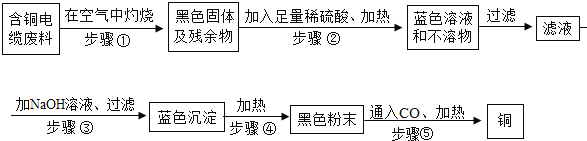
(1)过滤用到的玻璃仪器有_____、_____、_____.
(2)写出步骤③和步骤⑤发生反应的化学方程式:
步骤③:_____;
步骤⑤:_____.
(3)此方案中可能造成空气污染的步骤有_____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com