
【题目】化学兴趣小组在实验室发现一瓶氢氧化钠溶液,瓶口有少量白色固体且玻璃瓶塞打不开,这一情况激起了他们浓厚的兴趣,于是展开了如下探究:
[提出问题]瓶口白色固体的成分是什么?
[查找资料]
(1)玻璃中含有二氧化硅(SiO2) ,二氧化硅能与氢氧化钠溶液反应,生成硅酸钠(Na2SiO3) 和水。
(2)硅酸钠是一种白色固体,有很强的粘合性,可溶于水,溶液呈碱性:硅酸钠溶液能与强酸反应,如: ![]() (白色) :硅酸钠溶液能与氯化钙溶液反应:
(白色) :硅酸钠溶液能与氯化钙溶液反应: ![]() (白色)。
(白色)。
[作出猜想]白色固体的成分是:
猜想l:硅酸钠;
猜想2:硅酸钠和碳酸钠;
猜想3:硅酸钠、碳酸钠和氢氧化钠
[实验探究]取一定量白色固体溶于适量水中形成样品溶液,分别进行如下实验探究:
实验 | 实验操作 | 实验现象 | 结论与评价 |
实验一 | 取样品溶液少许于试管中,加入足量的稀盐酸 | 有气泡冒出且产生白色沉淀 | 猜想__不成立 |
实验二 | ①另取样品溶液少许于试管中,加入过量的氯化钙溶液 | ________________。 | 猜想3成立。 |
②取上述实验①后的上层清液,滴加____________ | 产生蓝色沉淀 |
写出实验二中产生蓝色沉淀的化学方程式:________________________。
[反思交流]
(1)氢氧化钠溶液必须密封保存,且试剂瓶只能用橡胶塞。
(2)实验二中过量的氯化钙溶液的作用是____________________。
【答案】1 产生白色沉淀 硫酸铜溶液 ![]() 完全除去硅酸钠和碳酸钠
完全除去硅酸钠和碳酸钠
【解析】
[实验探究]由题意可知,样品中加入足量稀盐酸,有气泡产生和产生白色沉淀,其中硅酸钠能于稀盐酸反应生成白色沉淀,碳酸钠可以与稀盐酸反应生气二氧化碳气体,故样品中一定含有碳酸钠和硅酸钠,故猜想1不成立;
①由实验一可知,样品中含有碳酸钠,且含有硅酸钠,由题中资料可知,两者都可以与氯化钙反应生成白色沉淀;
②由实验现象分析,产生蓝色沉淀,初中所学知识中,蓝色沉淀为氢氧化铜,故实验操作中应该加入铜离子的可溶性盐溶液如硫酸铜溶液;
由题意可知,实验操作中加入了硫酸铜溶液,硫酸铜溶液与氢氧化钠反应生成氢氧化铜蓝色沉淀,反应的化学方程式为:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;
[反思交流](2)由题意可知,实验二中加入了过量氯化钙溶液,因为原样品中有碳酸钠与硅酸钠,要验证样品是否含有氢氧化钠,要先除去样品中的碳酸钠与硅酸钠,由于不知道样品中碳酸钠与硅酸钠的含量,故加入过量的氯化钙,确保样品中的碳酸钠与硅酸钠全部反应完全。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:初中化学 来源: 题型:
【题目】为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中逐滴加入溶质质量分数为16%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:
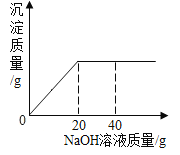
请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液_____克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液中溶质的质量分数为_________(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行探究。
(提出问题)①三种溶液的酸碱性?②它们与酸反应时溶液的pH如何变化?
pH | 2~3 | 4~6 | 7 | 8~9 | 10~11 | 12~14 |
紫甘蓝汁液显示的颜色 | 紫红 | 浅紫 | 紫色 | 蓝色 | 绿色 | 黄色 |
(实验1)向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠溶液 | 氢氧化钠溶液 |
紫甘蓝汁液 显示的颜色 | 紫色 | 蓝色 | 绿色 | 黄色 |
(实验2)向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图1所示。
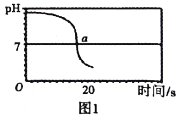
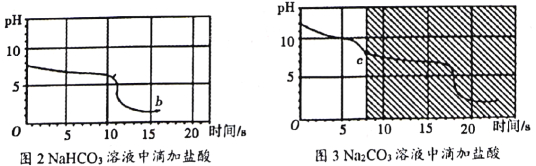
(实验3)向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图2、图3所示。将图2与图3的阴影部分进行叠加,发现两者基本重合。
(解释与结论)
(1)实验l得出三种溶液的碱性由强到弱的顺序为_____。
(2)实验2证明了氢氧化钠能与盐酸发生反应,其理由是________,实验结束,向反应后的溶液中滴加紫甘蓝汁液,观察到的现象是_____________。
(3)实验3中,b点的溶质为_______(填化学式),c点后发生反应的化学方程式为_________。
(4)依据实验
(拓展与延伸)洁厕灵是常用的陶瓷清洗液,某同学对某品牌洁厕灵的有效成分含量进行探究。向一锥形瓶中加入100g该品牌的洁厕灵,再加入足量的溶质质量分数为8%的NaHCO3溶液120g,反应结束后溶液的总质量是215. 6g。试计算下列问题:
已知:洁厕灵有效成分是HCl,洁厕灵中其他成分均不跟NaHCO3反应。
(1)该品牌洁厕灵中HCl的质量分数是____?(写出计算过程)
(2)该实验中,你认为NaHCO3溶液加入“足量”对测定结果____(填“有”或“无”)影响。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)用化学用语填空:
①氖元素_______________________;
②2个氮原子_______________________;
③4个甲烷分子_______________________;
④钙离子_______________________;
⑤标出“H2O”中氧元素的化合价_______________________。
(2)写出“2NO2”中前面“2”的含义._______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、 b、c三种物质的溶解度曲线,据图回答下列问题:
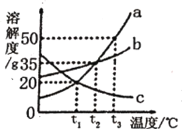
(1)三种物质的溶解度随着温度升高而减小的物质是_________。
(2)t1°C时,把50g物质a加入到200g水中充分搅拌、静置,所得溶液的质量为___g。
(3)取固体a进行如图实验,属于不饱和溶液的是_______,烧杯C中溶质的质量分数为__ (精确到0.1%)。
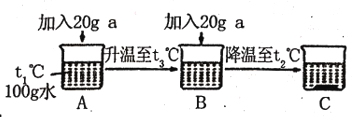
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组同学为验证氢氧化钠的化学性质,设计了下面三个实验。
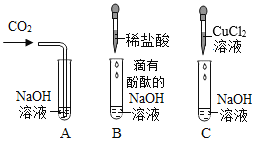
完成实验后,观察到A、B试管均为无色,C试管上层为无色溶液,试管底部有蓝色沉淀生成,C试管中反应的化学方程式是__:将A、B试管和C试管中的上层清液一起倒进一个洁净的烧杯中,观察到烧杯内溶液变为红色。
[提出问题]混合后烧杯内溶液中除酚酞外,含有的溶质是什么?
[查阅资料]碳酸钠溶液显碱性,氯化钙、氯化钡溶液显中性。
[猜想假设]猜想一:氯化钠、碳酸钠
猜想二:氯化钠、氢氧化钠
猜想三:氯化钠、碳酸钠和氢氧化钠
猜想四:氯化钠、碳酸钠、氢氧化钠、盐酸
[交流讨论]小组同学和老师交流后认为猜想_____是错误的;老师告诉同学们猜想二也不合理,理由是_____。
[实验验证]大家对剩余的猜想设计了如下实验进行验证:
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取少量烧杯中的废液于试管中,滴加适量的氢氧化钙溶液 | 有白色沉淀产生,上层溶液为______色 | 猜想三成立 |
方案二 | 取少量烧杯中的废液于试管中,滴加过量的______溶液 | 产生白色沉淀,上层溶液仍为红色 | 猜想三成立 |
[反思交流] 经小组同学交流讨论后, 认为方案一不能验证猜想三成立, 原因是________。
[拓展应用]以上实验中,若要检验氢氧化钠,必须对碳酸钠进行“屏蔽处理”,否则碳酸钠的存在会对氢氧化钠的检验产生干扰,检验有相似性质的物质,要避开共性,从个性着手,若要检验氯化钠溶液中是否混有盐酸可选用________溶液。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化,如图所示。
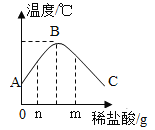
(1)由图可知,稀盐酸与氢氧化钠溶液发生的反应是________________(填“放热”或“吸热”)反应。
(2)从A到B过程中,烧杯中溶液的pH逐渐______ (填 “增大”或“减小”),B点表示的含义是_________。
(3)加入ng稀盐酸时,溶液中溶质有_______,加入盐酸到mg时pH_________(填“大于”“小于”或“等于”) 7.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业生产硫酸中的某一步反应用微观模型图表示如下,下列说法正确的是( )
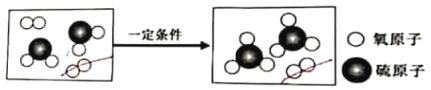
A.反应前后硫元素的化合价从+2价变成+3价
B.参加反应的反应物间分子个数比是1:1
C.反应前后分子数目不变
D.该反应属于化合反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com