
【题目】如图是a、 b、c三种物质的溶解度曲线,据图回答下列问题:
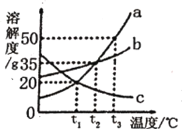
(1)三种物质的溶解度随着温度升高而减小的物质是_________。
(2)t1°C时,把50g物质a加入到200g水中充分搅拌、静置,所得溶液的质量为___g。
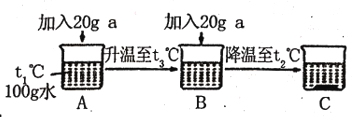
(3)取固体a进行如图实验,属于不饱和溶液的是_______,烧杯C中溶质的质量分数为__ (精确到0.1%)。
科目:初中化学 来源: 题型:
【题目】利用下列实验来探究CO2气体的制取和性质。
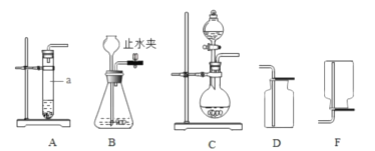
(1)A、B、C三套发生装置都可用于实验室制取CO2气体。
①仪器a的名称是____________。
②实验室制取CO2的化学方程式是__________;收集CO2可选用的装置是______(填序号),检验CO2收集满的方法是____________。
③使用B装置前,检查气密性的方法:关闭止水夹,往长颈漏斗内加水,若______,则装置漏气。
④与A装置相比,利用C装置制取CO2的优点是_________________。
(2)某化学兴趣小组利用“数字化实验”探究空气中氧气的含量,实验过程如下:如图1所示连接好实验装置,在燃烧匙内装有红磷,集气瓶底部有少量水;将压力传感器接入电脑并打开;点燃燃烧匙内的足量红磷并塞入集气瓶,一段时间后,得到如图2所示集气瓶内气压与时间关系曲线图。
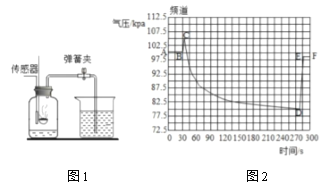
①图2中AB段气压不变的原因是___________________________。
②导致DE段气压变化的实验操作是___________________________。
③CD段气压变化的原因是______(填序号)。
a 氧气参加了反应
b 集气瓶内温度降低
c 生成的五氧化二磷是固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用下列实验装置进行实验,能达到目的的是
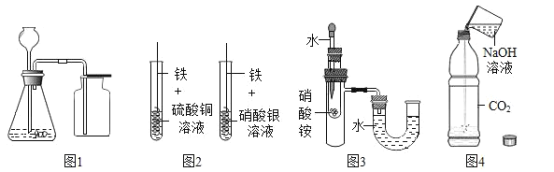
A. 图1装置可用锌粒和稀硫酸制取H2或用大理石和稀盐酸制取CO2
B. 图2装置铁丝表面均有固体析出可探究金属活动性:Fe>Cu>Ag
C. 图3装置看到U型管水面左高右低可验证NH4NO3溶于水吸热
D. 图4装置根据软塑料瓶变瘪可证明CO2能与NaOH反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸钾和氯化钠的溶解度曲线如下图所示。30℃时,分别将30g硝酸钾和氯化钠放入100 g水中,充分溶解。下列结论中,不正确的是

A.两种溶液中溶质的质量分数相等
B.通常情况下,采取降温的方法能将两种溶液都变成饱和溶液
C.若将硝酸钾溶液降温到20℃,溶液中溶质和溶剂的质量比为3∶10
D.若将硝酸钾溶液变为10℃时的饱和溶液,溶液中溶质的质量分数一定减小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组在实验室发现一瓶氢氧化钠溶液,瓶口有少量白色固体且玻璃瓶塞打不开,这一情况激起了他们浓厚的兴趣,于是展开了如下探究:
[提出问题]瓶口白色固体的成分是什么?
[查找资料]
(1)玻璃中含有二氧化硅(SiO2) ,二氧化硅能与氢氧化钠溶液反应,生成硅酸钠(Na2SiO3) 和水。
(2)硅酸钠是一种白色固体,有很强的粘合性,可溶于水,溶液呈碱性:硅酸钠溶液能与强酸反应,如: ![]() (白色) :硅酸钠溶液能与氯化钙溶液反应:
(白色) :硅酸钠溶液能与氯化钙溶液反应: ![]() (白色)。
(白色)。
[作出猜想]白色固体的成分是:
猜想l:硅酸钠;
猜想2:硅酸钠和碳酸钠;
猜想3:硅酸钠、碳酸钠和氢氧化钠
[实验探究]取一定量白色固体溶于适量水中形成样品溶液,分别进行如下实验探究:
实验 | 实验操作 | 实验现象 | 结论与评价 |
实验一 | 取样品溶液少许于试管中,加入足量的稀盐酸 | 有气泡冒出且产生白色沉淀 | 猜想__不成立 |
实验二 | ①另取样品溶液少许于试管中,加入过量的氯化钙溶液 | ________________。 | 猜想3成立。 |
②取上述实验①后的上层清液,滴加____________ | 产生蓝色沉淀 |
写出实验二中产生蓝色沉淀的化学方程式:________________________。
[反思交流]
(1)氢氧化钠溶液必须密封保存,且试剂瓶只能用橡胶塞。
(2)实验二中过量的氯化钙溶液的作用是____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用二氧化碳制取重要的化工原料乙烯的微观过程如图所示。下列说法正确的是(___)
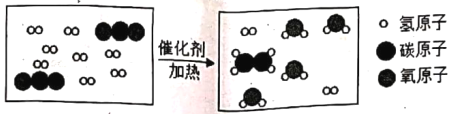
A 该反应属于置换反应
B 反应前后各元素的化合价均不变.
C 参加反应的两种分子的个数比为1: 3
D 此反应过程中涉及的氧化物的化学式是________(任写一种)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水及溶液与人类的生活生产密切相关。根据下列图示,请回答相关问题。
图1活性炭净水器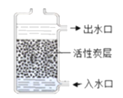 图2 水的电解
图2 水的电解
图3 溶解度曲线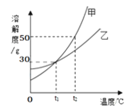 图4 探究实验
图4 探究实验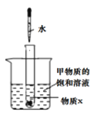
(1)图1中,活性炭净水器主要利用了活性炭具有的____性;图2所示实验中,试管b中得到的气体是(写物质名称)____。
(2)图3为甲、乙两种固体物质的溶解度曲线图。t1℃时,甲物质的溶解度是__,t2℃时,甲的饱和溶液溶质质量分数_________乙的饱和溶液溶质质量分数(填“大于”、“等于”、“小于”之一);图4所示实验中,将水滴入盛有物质X的小试管中,可观察到烧杯中有甲物质的固体析出。则物质X可能是_________(填序号之一)。
A 食盐 B 烧碱 C 生石灰 D 硝酸铵
(3)下图是氯化钠和硝酸钾在不同温度的溶解度,请回答。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
①20℃时,将136g饱和NaCl溶液蒸发10g水后,再降温到20℃,可析出NaCl晶体的质量为____;
②某小组想用20%的氯化钠溶液(密度为1.17g/cm3),配制30g质量分数为10%的氯化钠溶液,需要20%的氯化钠溶液____mL
③若将上表数据在坐标系中绘制成NaCl和KNO3的溶解度曲线,两条曲线的交点对应的温度范围是___(填序号)。
A 0~20℃ B 20~40℃ C 40~60℃ D 60~80℃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习复分解反应发生条件时,小红同学做了下表中的四个实验。
试管编号 | ① | ② | ③ | ④ |
试管内试剂 | NaOH溶液 | MgCl2溶液 | Na2CO3溶液 | Ba(NO3)2溶液 |
加入硫酸后的现象 | 无明显现象 | 无明显现象 | 产生气泡 | 白色沉淀生成 |
(1)根据以上实验,可以判断试管③④中发生了复分解反应。试管③中反应的化学方程式为_________________________________。
(2)小明同学向盛有NaOH溶液的试管中先加了一种试剂,再加稀硫酸,从而能说明试管①中也发生了反应,这种试剂是___________。
(3)为了验证试管②中是否发生复分解反应,小明同学进行了如下探究。
[提出猜想]猜想1:试管②中没有发生复分解反应,溶液中有MgCl2,即Mg2+和Cl-同时存在溶液中。
猜想2:试管②中发生了复分解反应,溶液中无MgCl2。
老师提示SO42-会对Cl-的检验有干扰,需要先除去,小明根据老师的提示和自己的猜想提出了以下实验方案。
[设计方案]
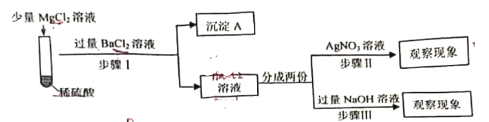
沉淀A的化学式是___________。
老师评价该方案时指出:设计思路正确,但试剂选择有误,你认为应该将所选的试剂_______改成____________。
小明按照修改后的方案进行了实验,最后得出的结论是猜想1正确,则步骤Ⅱ、步骤Ⅲ中必然会观察到的现象是____________________。
[实验反思]小明反思进行步骤Ⅲ时,加NaOH溶液采用了滴加的方式,但没有立即观察到任何现象,你认为其中的原因是_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com