
 化学兴趣小组设计的创新实验是“火龙生字”.在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1)用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究:
化学兴趣小组设计的创新实验是“火龙生字”.在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1)用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究:| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31.6 | 63.9 | 110 | 169 | 246 |
分析 根据已有的知识进行分析,化学反应前后元素的种类不变;要证明生成了氧气,可以使用带火星的木条进行检验;促进燃烧可以增大氧气的浓度;根据硝酸钾的溶解度进行分析解答.
解答 解:【猜想与假设】:二氧化氮不是单质,而硝酸钾中不含有氢元素,不可能生成氢气.
故答案为:二氧化氮不是单质,硝酸钾中不含有氢元素;
【进行实验】:要证明生成氧气,可以取硝酸钾晶体放在试管中加热,然后将带火星的木条伸进试管内,观察到木条复燃,证明生成的是氧气;
故答案为:将少量硝酸钾晶体放在试管中加热,把带火星的木条放在试管中;木条复燃;2KNO3$\frac{\underline{\;\;△\;\;}}{\;}$2KNO2+O2↑;
【解释与结论】:促进燃烧可以增大氧气的浓度,白纸上写过字的地方更容易燃烧的原因是硝酸钾晶体受热分解生成氧气,使写过字的白纸附近氧气的浓度增大;
故答案为:硝酸钾晶体受热分解生成氧气,使写过字的白纸附近氧气的浓度增大;
【反思与评价】:根据表格可以看出,硝酸钾的溶解度随温度的升高而增大,使用“硝酸钾的热饱和溶液”书写文字,可以使更多的硝酸钾晶体附着在白纸表面.
故答案为:硝酸钾的溶解度较大,用热饱和溶液能使白纸上附着更多的硝酸钾晶体.
点评 本题考查了化学实验的设计以及溶解度的知识,完成此题,可以依据已有的知识进行.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | ②③⑦①④⑥⑤ | B. | ②③⑦①④⑤⑥ | C. | ③②⑦①④⑤⑥ | D. | ②⑦③①④⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
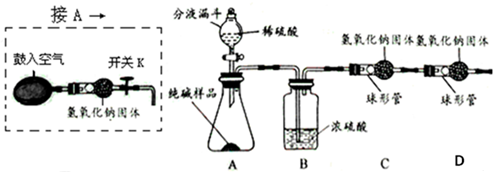
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 厨房中的食盐、味精、蔗糖三种调味品 | |
| B. | 硫酸钠、碳酸钠、硝酸钠三种无色溶液 | |
| C. | 食盐、烧碱、氯化铵三种白色固体 | |
| D. | 生石灰、熟石灰、淀粉三种白色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 2P+5O2 $\frac{\underline{\;点燃\;}}{\;}$ P2O5 | B. | 2H2O $\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | ||
| C. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$ 2H2O+O2↑ | D. | H2SO4+NaOH═NaSO4+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
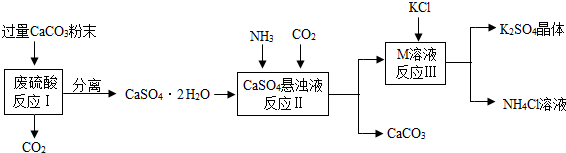
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 胃酸过多须服用抗酸药物(能与盐酸反应).如图为铝碳酸镁说明书的部分内容.兴趣小组对该药物开展如下探究.
胃酸过多须服用抗酸药物(能与盐酸反应).如图为铝碳酸镁说明书的部分内容.兴趣小组对该药物开展如下探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | X>Y>Z | B. | X>Z>Y | C. | Y>Z>X | D. | Z>X>Y |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
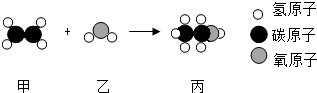
| A. | 甲的化学式为CH2 | |
| B. | 甲、乙、丙都是有机物 | |
| C. | 反应中甲、乙、丙的分子个数比为2:1:1 | |
| D. | 该化学反应基本类型为化合反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com