
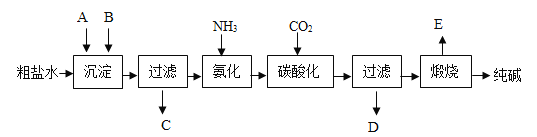
����Ŀ���ҹ�����ר�Һ�°������������Ƽ���������������з����ķ�Ӧ��Ҫ�ǣ��乤ҵ��������Ĺ�������ʾ��ͼ������ʾ�����������ˮ�м���ij�����A��B�ֱ�Ϊ�����ƺ�̼���ƣ�
�� NH3 + CO2 + H2O = NH4HCO3 �� NH4HCO3 + NaCl = NaHCO3�� + NH4Cl �� 2NaHCO3![]() Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2��
��ش��������⣺
��1��ʵ�����ᴿ���ε�ʵ���������Ϊ��ȡ�����ܽ⡢���������ˡ������ᾧ��������ʱ������Һ�����������ǣ���ʵ������ĽǶȸ���һ�ֿ��ܵ�ԭ��______��
��2��ʵ�����У����ᴿ�õ����Ȼ�������100g 0.9%��������ˮ��ʹ�õ�������ҩ�ס���������������ƽ����ͷ�ιܡ��ձ��⣬����Ҫ�ʵ���������_________��
��3����������Ĺ��������У�̼�ữʱ����NaHCO3���壬û������Na2CO3�����ԭ����____��
��4�������������а�����������ѭ��ʹ�õģ�Ϊ�ˣ�����ҺD�м���ʯ��ˮ����������������д���÷�Ӧ�Ļ�ѧ����ʽ_________��
���𰸡���ֽ�����Һ��Һ�������ֽ��Ե 100mL����Ͳ NaHCO3���ܽ��С��Na2CO3������ܽ�� Ca��OH��2+2NH4Cl�TCaCl2 +2NH3��+2H2O
��������
��1�����˲����У�����ֽ���𡢻�©���ڵ�Һ�������ֽ�ı�Ե���������ɾ����ᵼ����Һ���ǣ������ֽ�����Һ��Һ�������ֽ��Ե��
��2������100g 0.9%��������ˮ��Ҫˮ������Ϊ��100g-100g��0.9%=99.1g�����Ϊ99.1mL������Ҫ100mL����Ͳ�����100mL����Ͳ��
��3������������̼�ữʱ���ῴ����Һ���������壬��������̼���Ƶ��ܽ�ȴ���̼�����ƣ����NaHCO3���ܽ��С��Na2CO3������ܽ�ȣ�
��4����ҺD����Ҫ�ɷ����Ȼ�泥��Ȼ�����������Ʒ�Ӧ�Ǻϳ��Ȼ��ơ�ˮ�Ͱ��������Ca��OH��2+2NH4Cl�TCaCl2 +2NH3��+2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǽס��ҡ�������������ˮ�е��ܽ�����ߡ�����˵����ȷ����( )
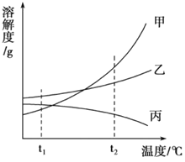
A. t2��ʱ�ܽ���ɴ�С��˳������>��>��
B. ��t2�潵��t1���������������Ǽ���Һ
C. ��t2�潵��t1�����ҺŨ��һ���������仯
D. ���ұ����������ܽ�ȶ����¶����߶�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧϰ��ѧ���õķ��������ֽⷴӦ��������Ҫ����һ�������ģ��ᡢ���֮��ֻ�е����ֻ����ﻥ�ཻ���ɷ֣����������г��������������ˮ����ʱ�����ֽⷴӦ�ſ��Է�����
���ж���������֮���ܷ������ֽⷴӦ�������ݲ��ܷ�����Ӧ��ԭ����з��࣬����ʵ������������ݣ�
��BaCl2+H2SO4����
��KNO3+H2SO4����
��NaCl+Cu��OH��2����
��CaCO3+HCl����
��NaC1+Ca��OH��2����
��BaSO4+AgNO3����

________��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᡢ�������ء��Ȼ�������Ҫ�Ļ���ԭ�ϣ�Ҳ��ʵ���ҳ������Լ���
��1�����й��������˵������ȷ����_____��
A Ũ������ճ������״��Һ��
B ϡ�������������Ʒ����
C Ũ����ε���ֽ�ϣ�ʹֽ���
D Ũ���᳨�ڷ��ã������������
д������ѡ�����漰���Ļ�ѧ����ʽ_____��
��2���������صĻ�ѧ���ʺ������������ơ�С����ʵ�����ڷ���һƿ���ھ��õ�����������Һ����ȡ��һ���֣�����ϡ��������������ɣ���д���뷢���������йص�������ѧ����ʽ_____��
��3���Ӻ�ˮ��ɹ���Ĵ����к���CaCl2��MgCl2��Na2SO4�ȿ��������ʡ�Ϊ�˳�ȥ���ʣ������²��������ܽ⣻�����μӹ�����BaCl2��NaOH��Na2CO3��Һ���۹��ˣ��ܼ�����������������ᾧ��
�ټ���Na2CO3��Һ��Ŀ����ʲô_____��
����������з����ĸ��ֽⷴӦһ���м���_____��
���������õ��Ȼ��Ƶ�������ԭ�������к��е��Ȼ��Ƶ�������ȣ���ʲô�仯_____��
��4��С���ڼ������һƿʳ��ˮ��С���������ƿʳ��ˮ���Ȼ��Ƶ�����������ȡ130gʳ��ˮ������������������Һ����ַ�Ӧ������2.87g��ɫ��������ʳ��ˮ���Ȼ��Ƶ���������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������У�����ȷ����
A.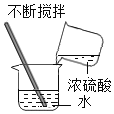 ϡ��Ũ����B.
ϡ��Ũ����B.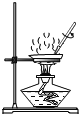 ����ʳ��ˮ
����ʳ��ˮ
C. ��ȡҺ�����D.
��ȡҺ�����D. ����ˮpH
����ˮpH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�������巢���ķ�Ӧ,������ͬ�������ͬ��ԭ�ӡ�����˵����ȷ����
![]()
A.������һ����������
B.��ѧ��Ӧ��ʵ���Ƿ��ӵ��������
C.��Ӧǰ���Ԫ�صĻ��ϼ۾������˱仯
D.�÷�Ӧ�Ȳ��ǻ��Ϸ�ӦҲ���ǷֽⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������̼���ε��������ơ�����ͼʾ��Ϣ,�ش���������:
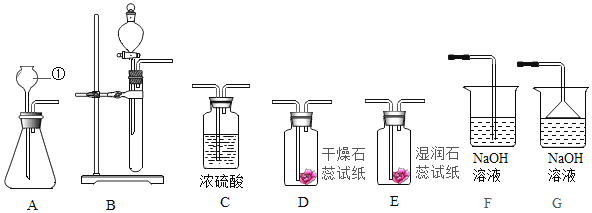
(1)ͼ�Тٵ�����������________________��ʵ��������̼�����ϡ������ȡ������̼��Ӧ�Ļ�ѧ����ʽΪ________________��
(2)ʵ���������������Ʒ�ĩ��ϡ������ȡSO2,Ӧѡ��ķ���װ����______________(�����)�����ֱ�ӽ���SO2�ķ���װ����װ��E����,ʯ����ֽ���,�ܷ�֤��SO2����ˮ��Ӧ������? _____________(��ܡ����ܡ�),������________________________________��
(3)SO2�Դ�����Ӱ���ǻ�����________________��ʵ���п���ѡ��װ��____________����β������,���ѡ��������________________________________��
(4)��ͼ��,����ijƷ�ƿ�����������ij��ȤС�����������ϰ�װ�����������ʾװ������ȡCO2.ʵ���д���ʯӦ������________________��(ѡ��ϲ������²���)����,��װ���ܿ��Ʒ�Ӧ�ķ�����ֹͣ�������������________________����װ��������ȡ��������ʱ���ܿ��Ʒ�Ӧ�ķ�����ֹͣ��ԭ����________________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����Χ��������кͷ�Ӧ������ѧ���ֳ�����С��̽�������������һ���������ʵ��̽����
����ʾʵ�飩��һ����ϡ������뵽ʢ����������Һ��С�ձ��С��÷�Ӧ�Ļ�ѧ����ʽ�ǣ�_________���÷�Ӧ�Ļ�ѧ��Ӧ����������_____��
���������ϣ�CaCl2��Һ������
��������⣩ʵ����δ�۲쵽����������ͬѧ���������ʣ���Ӧ����Һ�����ʵijɷ���ʲô��
����������裩������ʣ�����ͬѧ�������£�
���� I��ֻ�� CaCl2 ���� II����_____
���� III���� CaCl2 �� Ca(OH)2 ���� IV���� CaCl2��HCl �� Ca(OH)2
����ͬѧ�����ϲ���������ɣ���Ϊ���� IV ����������������_____��
��ʵ��̽����Ϊ����֤������룬��С���������������������̽����
ʵ�鷽�� | �μ���ɫʯ����Һ | ͨ�� CO2 | �μ� Na2CO3 ��Һ |
ʵ����� |
|
|
|
ʵ������ | ______ | _____ | ������ɫ���� |
ʵ����� | ��Һ�к��У�Ca(OH)2 | ��Һ�к��У�Ca(OH)2 | ��Һ�к��У�Ca(OH)2 |
���ó����ۣ�ͨ��̽����ȫ��ͬѧһ��ȷ������ III ����ȷ�ġ�
�����۷�˼��
��1������ͬѧ��Ϊ�μ�Na2CO3��Һ������ɫ������������֤����Һ��һ������Ca(OH)2�������������˵��ԭ��_____��
��2���ڷ�����Ӧ��������Һ�����ʵijɷ�ʱ�����˿����������⣮����Ҫ����_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��һ����ʵ��Ϊ��������Ȼѧ�ơ�������ͼʾ��ʵ������У��ܴﵽʵ��Ŀ�ĵIJ�����
ʵ�����ͼʾ |
|
|
|
|
ѡ�� | A̽�������˶� | B��ȡ35mLҺ�� | C�ⶨ������O2���� | D�ⶨ��Һ��pH |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com