
| ��ƿ | ��ƿ+ϡ���� | ��ƿ+��Ӧ����Һ | |
| �������ˣ� | 35.5 | 55.5 | 80.5 |
���� ������Һ���������������������Լ������ʵ�������
�����ṩ�����ݿ��Լ�������������Һ��������
ϡ������������Ʒ�Ӧ�����Ȼ��ƺ�ˮ�����ݷ�Ӧ�Ļ�ѧ����ʽ���ṩ�����ݿ��Լ����ƿϡ�������������������
��� �⣺��1����Ҫ����500g16%������������Һ����Ҫ�������ƹ�������Ϊ��500g��16%=80g��
���80��
��2������ʵ����ʵ�����ĵ�����������Һ����Ϊ��80.5g-55.5g=25g��
���25��
��3�����ƿϡ����������Ȼ�������Ϊx��
ϡ���������Ϊ��55.5g-35.5g=20g��
NaOH+HCl�TNaCl+H2O��
40 36.5
25g��16% x
$\frac{40}{25g��16%}$=$\frac{36.5}{x}$��
x=3.65g��
��ƿϡ�����������������Ϊ��$\frac{3.65g}{20g}$��100%=18.25%��
�𣺸�ƿϡ�����������������Ϊ18.25%��
���� ������Ҫ����ѧ�����ü��跨�ͻ�ѧ����ʽ���м�����ƶϵ�����������ʱҪע��淶�Ժ�ȷ�ԣ�


 Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 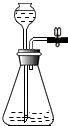 ��������� | B�� | 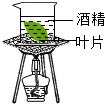 ҶƬ��ɫ | C�� | 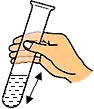 ���Թ� ���Թ� | D�� | 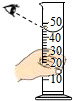 ��Һ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CaO����ʯ�ҡ������� | B�� | CH4���������л��� | ||
| C�� | Na2CO3������� | D�� | H3PO4�����ᡢ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������� | B�� | �˵���� | C�� | ���ԭ������ | D�� | ԭ�������ĵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϴ�Ӽ���ϴ�;� | B�� | ��������ϴ���� | ||
| C�� | ������ˮϴ�� | D�� | ������ϴ��ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
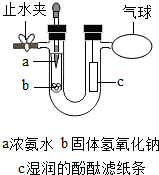 ijͬѧ��ѧ�꡶���Ӻ�ԭ�ӡ��Խ̲��е�ʵ���������ͼ�Ľ���
ijͬѧ��ѧ�꡶���Ӻ�ԭ�ӡ��Խ̲��е�ʵ���������ͼ�Ľ����鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com