
【题目】固定和利用二氧化碳能有效地利用资源,并减少空气中的温室气体。工业上用二氧化碳生产甲醇燃料:CO2+3H2 CH3OH+H2O。下列有关说法不正确的是( )
CH3OH+H2O。下列有关说法不正确的是( )
A.二氧化碳是一种宝贵的资源
B.该种方法为二氧化碳的利用创造了一种新途径
C.钌-膦铬合物的质量在反应前后发生了变化
D.碳原子数在反应前后没有变化
科目:初中化学 来源: 题型:
【题目】(10陕西19).陕西榆林是我国重要的能源基地,煤化工产业发展迅速。煤化工是指在一定条件下将煤等物质转化为H2、CO和炭黑等一系列重要化工原料的生产过程。
(1)用炭黑制成的墨汁书写或绘制的字画能够经久不变色,其原因是________________。
(2)将干燥的H2和CO两种气体分别点燃,在火焰上方各罩一个冷而干燥的烧杯,烧杯内壁出现____________的原气体是H2。
(3)CO是一种气体燃料,其燃烧的化学方程式为________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭容器中放入X、Y、Z、W 四种物质,在一定条件下发生化学反应,一段时间后,测得有关说法如下表,则关于此反应的认识不正确的是 ( )
物质 | X | Y | Z | W |
反应前的质量 | 2 | 1 | 16 | 16 |
反应后的质量 | 17 | m | 6 | 11 |
A.物质Y 可能是该反应的催化剂B.该反应为复分解反应
C.反应后 Z 和Y 的质量比为 6:1D.参加反应的 Z 和W 的质量比为 2:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活处处有化学,家庭厨房就是一个化学小世界,“锅碗瓢盆”和“柴米油盐酱醋茶”中包含着许多化学知识。
(1)铁锅用生铁铸造而成,生铁属于_____(填“金属”或“有机合成”)材料。油锅着火了,应立即盖上锅盖灭火,其原理_______。
(2)为了健康,国家卫健委推广选购和食用碘盐、锌盐、钙盐、硒盐等。这些食盐中含的“碘、锌、钙、硒”等是指______(填“原子”“离子”或“元素”)。
(3)某些食品包装袋内常有“双吸粉”,用来吸收氧气和水分,以防止食品腐败。下列属于“双吸粉”的物质是______(填序号)
①碳粉②铁粉③生石灰 ④氯化钙
(4)常用的食材有大米、面粉、食用油、鸡蛋、青菜等,其中富含维生素的是____。
(5)天然气的主要成分为甲烷,当天然气充分燃烧的的化学方程式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国首发石墨烯锂离子电池,充电效率是普通充电产品的24倍。稀有金属锂被广泛应用于电池、贮氢等领域,图1为锂在元素周期表中的信息,图2是锂原子的结构示意图。
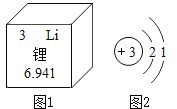
(1)从图1中可获得的一条信息是________。
(2)锂原子的最外层电子数为___,在反应中______(填“得到”或“失去”)1个电子,则所形成的离子符号为______。
(3)储氢合金是一类能够大量吸收氢气,并与氢气结合成金属氢化物的材料,同时放出热量,此过程发生了____(填“物理”或“化学”)变化,储氢合金属于_____(填“纯净物”、“混合物”)。
(4)某种锂电池的总反应式可表示为Li+MnO2═LiMnO2 ,该反应属于____反应,金属氧化物MnO2是该反应中的_____(填“反应物”或“催化剂”),LiMnO2 是一种电极材料,其中锰元素的化合价为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如右图所示。下列说法错误的是( )
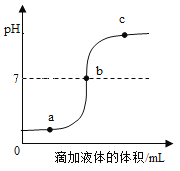
A. 图中b点所示溶液中,溶质是NaCl
B. 向图中c点所示溶液中滴加无色酚酞,溶液不变色
C. 该实验是将氢氧化钠溶液逐滴滴入到盛有稀盐酸的烧杯中
D. 由a点到b点的pH变化过程证明酸和碱发生了中和反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将 34 克碳酸钠和氯化钠的固体混合物加到盛有 100 克盐酸溶液的烧杯中,恰好完全反应,产生气体 4.4 克.求:
(1)原混合物中碳酸钠的质量____;
(2)盐酸溶液中溶质的质量分数____;
(3)反应后所得溶液溶质质量分数是多少?____(保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组设计了测定纯碱(Na2CO3)样品(只含NaCl杂质)中Na2CO3质量分数的实验方案.请回答下列问题:
小资料:碱石灰的主要成分是氢氧化钠和氧化钙的混合物
(1)气体法。
(原理思路)利用Na2CO3与稀硫酸反应产生CO2,通过测量丙装置实验前后的质量得出CO2质量,从而计算碳酸钠的质量分数。(不考虑原装置内空气的影响)
(实验分析)小科同学根据以上思路,设计了如图1的实验装置。
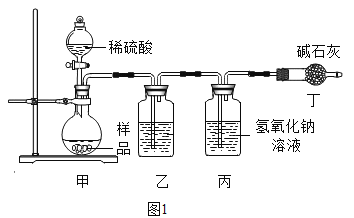
①实验装置乙中盛放的试剂为______________,
其作用是___________________________________;
装置丁中碱石灰的作用是________。(填字母)
A.吸收Na2CO3与稀硫酸反应产生CO2
B.防止外界空气中二氧化碳进入丙中
C.干燥二氧化碳
②实验中如果滴加稀硫酸的速度过快,会导致测得样品中碳酸钠的
质量分数______(填写“偏高”“偏低”或“不变”).
③小明同学认为小科的方案存在问题,即使操作规范下也会造成结果偏低,你
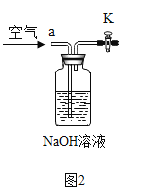
认为他的理由是_______________________________,应该将装置甲中双孔橡
胶塞换成三孔橡胶塞,并增加图2装置,实验结束后缓缓通入一段时间空气,
目的是___________________,其中NaOH溶液的作用是_________________。
(2)沉淀法.
(实验原理)利用碳酸根离子与钙离子结合生成沉淀,通过沉淀的质量而得出碳酸钠的质量分数。
(实验步骤)①用托盘天平称取样品11.0g放入烧杯中,加水使其完全溶解;
②加入过量的CaCl2溶液充分反应。证明CaCl2过量(即Na2CO3已完全反应)的方法是: 静置,向上层清液中滴加___________溶液,如果没有白色沉淀生成,证明CaCl2过量;
③过滤、操作X、干燥、称量沉淀的质量为10.0g,操作X的名称是_______,如果缺少此操作会造成碳酸钠质量分数__________(填写“偏高”“偏低”或“不变”)。
④通过以上提供的数据计算出样品中碳酸钠的质量分数为________。(写出计算过程,结果保留至0.1%,共3分)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据图回答下列问题:
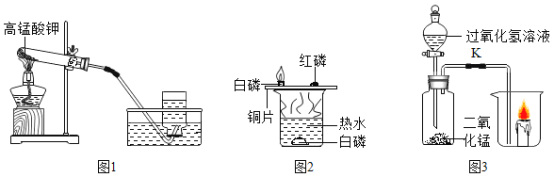
(1)图1为实验室用高锰酸钾制取氧气的装置。
①实验中反应的化学方程式为________。
②氧气可用排水法收集的原因是________。
(2)利用图2所示装置探究可燃物燃烧的条件(热水温度高于白磷着火点)。
①对比铜片上白磷燃烧和红磷不燃烧的现象,说明可燃物燃烧的条件之一是________。
②能说明可燃物燃烧需要与氧气接触的现象是________。
③烧杯中热水所起的作用是________。
(3)利用图3装置进行下列实验(烧杯中放着一支燃着的蜡烛),打开K。
①广口瓶中发生反应的化学方程式是________。
②观察到蜡烛_______,说明影响燃烧剧烈程度因素之一是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com