
【题目】下列4个坐标图分别表示4个实验过程中的某些变化,其中正确的是( )
A.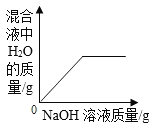 向一定量稀HCl中加入NaOH溶液
向一定量稀HCl中加入NaOH溶液
B.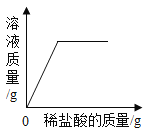 向一定量的稀盐酸中加入铁粉
向一定量的稀盐酸中加入铁粉
C.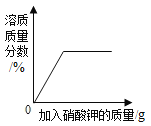 向接近饱和的硝酸钾溶液中加硝酸钾固体
向接近饱和的硝酸钾溶液中加硝酸钾固体
D.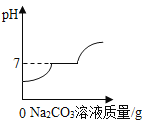 现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量碳酸钠溶液
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量碳酸钠溶液
【答案】D
【解析】
A、稀HCl与NaOH溶液反应生成氯化钠和水,原溶液中含有水,水的质量不可能为0,故选项图象错误。
B、向一定量的稀盐酸中加入铁粉,生成氯化亚铁溶液和氢气,原溶液的质量不可能为0,故选项图象错误。
C、接近饱和的硝酸钾溶液中加硝酸钾固体,能继续溶解,溶质质量分数增大;当达到饱和状态后,溶质的质量分数不再发生改变,且溶质质量分数的起点不可能为0,故选项图象错误。
D、盐酸和CaCl2的混合溶液加入过量碳酸钠溶液,碳酸钠先与稀盐酸反应生成氯化钠、水和二氧化碳气体,溶液的pH逐渐增大,至完全反应,pH=7;再与氯化钙反应生成碳酸钙沉淀和氯化钠,溶液的pH=7,再加入碳酸钠,碳酸钠溶液显碱性,pH大于7;故选项图象正确。
故选:D。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:初中化学 来源: 题型:
【题目】河南叶县的粗盐中含有![]() 、
、![]() 、
、![]() 以及泥沙等杂质以下是一种制备精盐的实验方案(用于沉淀的试剂均过量)请回答下列问题:
以及泥沙等杂质以下是一种制备精盐的实验方案(用于沉淀的试剂均过量)请回答下列问题:
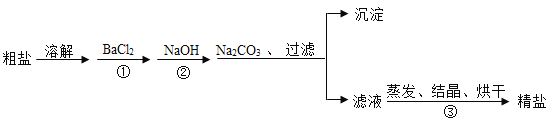
(1)碳酸钠的作用:________;
(2)①步骤中所发生的反应方程式:_____________;
(3)请设计实验证明滤液中的成分_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自来水厂净水过程示意图如下。请回答:
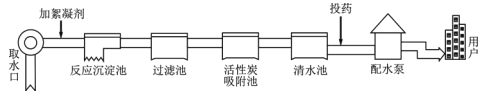
(1)除去水中固态杂质的设备是______(填正确选项前的字母);
A.过滤池 B.吸附池 C.清水池
(2)通常向清水池投放高铁酸钠(化学式为 Na2FeO4)杀菌消毒,高铁酸钠中铁元素的化合价为______;
(3)我国有关部门规定,经上述流程净化后进入用户的饮用水含铁<0.3mg·L-1,含铜<1.0mg·L-1,……。其中的“铁、铜”指的是______(填正确选项前的字母)。
A.原子 B.分子 C.元素
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学学习小组在完成“利用氯化钡溶液鉴别氯化钠和碳酸钠”的实验后,对废液缸中溶液的溶质成分进行了探究。请完成以下探究过程。
(提出问题)_____________?
(作出猜想)Ⅰ.溶质仅为氯化钠;Ⅱ溶质为氯化钡和氯化钠;Ⅲ._______________。
(设计方案)
实验操作 | 现象 | 结论 |
取少量废液缸中上层清液,向其中加入一定量的______________溶液。(填化学式,限填一种) | 无明显现象 | 猜想Ⅰ正确 |
______ | 猜想Ⅱ正确 | |
有气泡产生 | 猜想Ⅲ正确 |
(交流反思)学习小组经过讨论认为,含有可溶性钡盐的废液可以用碳酸钠溶液进行无害化处理。请写出硝酸钡与碳酸钠反应的化学方程式___________________。
若是人误吃了可溶性钡盐,不能服用碳酸钠溶液解毒而是服用硫酸钠溶液,理由是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是实验室制取气体的有关装置,依据下图回答相关问题
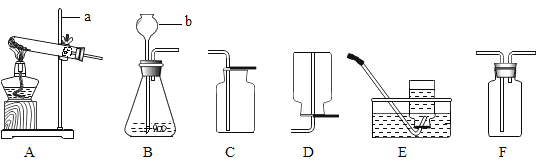
(1)写出标注仪器的名称:a________,b________。
(2)实验室制取二氧化碳所选用的装置是________(填字母),其反应的化学方程式为________。
(3)用F装置除去二氧化碳气体中混有的少量水蒸气,F中放入的试剂是________。
(4)在实验室加热氯化铵和氢氧化钙两种固体的混合物来制取氨气,其发生装置应选择________(填字母),若用此装置制取氧气,写出其化学方程式________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定镁和硫酸镁固体混合物中镁元素的质量分数,先称取5g混合物,放入一干净的烧杯中,然后取50g某溶质质量分数的稀硫酸,平均分五次加入其中,充分反应,实验所得数据如下表:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀硫酸的质量/g | 10 | 10 | 10 | 10 | 10 |
生成气体的总质量/g | 0.05 | m | 0.15 | 0.18 | n |
(l)上表中m=_____、n=_____.
(2)请计算所用稀硫酸的溶质质量分数(结果保留一位小数).____
(3)固体混合物中,硫酸镁的质量分数为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D和E是初中化学常见的五种不同种类的物质,其中B为一种红色固体,且A→B的反应过程较为复杂。图中“![]() ”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)。
”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)。
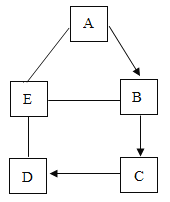
(1)E的化学式可能是____
(2)C→D的反应现象是_____E→B的反应现象为____
(3)A-E反应能发生的原因是______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用,我国化学家侯德榜创立了著名的“侯氏制碱法”,促进了世界技术的发展。
(查阅资料)①生产原料粗盐中含有少量可溶性杂质(MgCl2 和 CaC12)及不溶性杂质。
②氨气极易溶于水,二氧化碳能溶于水。
③生产原理:NaCl + NH3 + CO2+ H2O = NaHCO3↓+ NH4C1,分离得晶体 A,并使其充分受热,可分解制得纯碱及两种常见的氧化物。
④氯化铵分解的化学方程式是 NH4Cl===NH3↑+HCl↑。
⑤部分生产流程如下图所示:
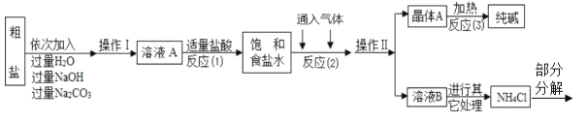
(问 题讨论)
(1)溶液 A 中的溶质为 ________,流程中加入适量盐酸的作用是 ________。
(2)反应(2)中为提高产率,所通入气体的顺序是 ________(填字母序号).
A.先通入 CO2 再通入 NH3 B.先通入 NH3 再通入 CO2
(3)上述生产流程中可循环使用的是 ________(填序号).
A.CO2 B.NH3 C.HCl D.NaOH E.Na2CO3
(组成确定)
(1)称取一定质量的纯碱样品,多次充分加热,称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀 HNO3,再滴加 AgNO3溶液,有白色沉淀。由上述实验可确定纯碱样品含有杂质 ________(写化学式).
(含量测定) 同学们为了测定该纯碱样品的纯度(假定只含一种上述杂质),设计了如下三组实验。甲组:取 12.0g 纯碱样品,向其中加入过量的盐酸,直至样品中无气泡冒出。将反应所得溶液小心蒸发,并将所得物质干燥、冷却至室温称得固体质量为 13.1g.样品中碳酸钠的质量分数为________。
乙组:取 12.0g 纯碱样品,利用下图所示装置,测出反应装置 C 增重了 4.1g(所加试剂均足量,每一步都反应完全).实验结束,发现乙组测定的质量分数偏小,其原因是_________。
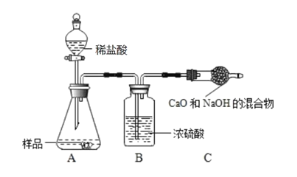
丙组:取 12.0g 的纯碱样品,完全溶于水,向其中加入过量的氯化钙溶液,待完全沉淀过滤、 洗涤、烘干称量固体质量,从而计算出碳酸钠的质量分数。组内同学提出意见,认为如果将氯化钙溶液换成氯化钡溶液则更好,老师认为有道理,原因是 ________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】食品营养与安全关系到每个人的身体健康。
(1)豆浆已成为众多家庭的早餐选择,下表是豆浆中部分成分的平均含量。
成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素 |
平均含量(%) | 96.0 | 1.8 | 0.7 | 1.1 | 0.01 | 0.03 | 0.0005 | 0.015 |
豆浆的成分中能作为机体生长、修补受损组织的原料的是________,人体缺少表中的________元素会引起贫血。
(2)霉变的花生中含有黄曲霉毒素(化学式![]() )食用后可导致癌症。黄曲霉毒素中碳、氢、氧元素的质量比是________。
)食用后可导致癌症。黄曲霉毒素中碳、氢、氧元素的质量比是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com