
【题目】根据所学的酸、碱、盐知识回答问题:(可参考提供的溶解性表)
部分碱、酸、盐的溶解性表(20℃)
阴离子 阳离子 | OH- | NO3- | C1- | SO42- | CO32- |
H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
K+ | 溶 | 溶 | 溶 | 溶 | 溶 |
Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
Ca2+ | 微 | 溶 | 溶 | 微 | 不 |
Cu2+ | 不 | 溶 | 溶 | 溶 | 一 |
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“一”表示那种物质不存在或遇到水就分解了。
(1)已知溶液中氢离子浓度越大,溶液的酸性越强,溶液的pH越小。有一同学在实验室中是这样测某溶液pH的:他先用蒸馏水润湿pH试纸,然后用____________(填仪器名称)蘸取试样进行检测,该同学测得的pH是否一定会有误差?__________________
(2)盐中含有金属离子(或NH4+)和酸根离子,组成相似的盐具有一些相似的化学性质。
①硫酸铜、硝酸铜两种物质的溶液均显_____________色,因为它们都具有相同的阳离子;向这两种物质的溶液中分别加入NaOH溶液,有相同的实验现象发生,写出其中一个反应的化学方程式______________。
② 向硫酸铜、硝酸铜两种物质的溶液中分别加入BaCl2溶液,能发生反应的物质是____________(填化学式),另外一种物质不反应。
③向硫酸铜溶液中,加入某纯净物的溶液,能同时将铜离子和硫酸根离子转变成沉淀,该纯净物的化学为______________。
(3)某实验小组将制作皮蛋的原料生石灰、纯碱和食盐放入水中,充分反应后过滤,得到澄清溶液。对该溶液的组成,甲、乙同学分别做出以下推测:

①我认为上述两位同学的推测都有不足,理由是甲:_____;乙:____。
②我的推测是:该溶液中一定存在的溶质是________________。为进一步确定该溶液可能的组成,还需设计实验并填写下表:(将答案按a-f的顺序填在答题卡上)
实验操作 (填所加试剂的化学式) | 实验现象 | 结论 |
| b__________ | 除了②推测的一定存在的溶质 外,该溶液中还含有: _____________________ |
| e__________ | 除了②推测的一定存在的溶质 外,该溶液中还含有: ____________________ |
上述两实验均无明显现象 | 只含有②推测的一定存在的溶质 |
【答案】玻璃棒 不一定 蓝 2NaOH+CuSO4═Na2SO4+Cu(OH)2↓或2NaOH+Cu(NO3)2═2NaNO3+Cu(OH)2↓ CuSO4; Ba(OH)2 碳酸钙不溶于水,因此溶液中不含有碳酸钙 氢氧化钙和碳酸钠不能共存 氯化钠、氢氧化钠 CaCl2 产生白色沉淀 碳酸钠 Na2CO3 产生白色沉淀 氢氧化钙
【解析】
(1)测定溶液pH的方法是:用洁净干燥的玻璃棒蘸取溶液,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH,如果先用蒸馏水润湿pH试纸,测定显中性溶液时不影响实验结果,测定酸性溶液时,导致实验结果偏高,测定碱性溶液时,导致实验结果偏低;
(2)含有铜离子的溶液是蓝色溶液;氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,和硝酸铜反应生成氢氧化铜沉淀和硝酸钠;硫酸铜和氯化钡反应生成硫酸钡沉淀和氯化铜,和氢氧化钡反应生成氢氧化铜沉淀和硫酸钡沉淀;
(3)氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠;
碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠。
(1)有一同学在实验室中是这样测某溶液pH的:他先用蒸馏水润湿pH试纸,然后用玻璃棒蘸取试样进行检测,该同学测得的pH不一定有误差,例如测定氯化钠溶液时,不影响实验结果,测定氢氧化钠溶液时,由于稀释了氢氧化钠溶液,导致实验结果偏小;故填:玻璃棒;不一定;
(2)①硫酸铜、硝酸铜两种物质的溶液均显蓝色,因为它们都具有相同的阳离子(铜离子);向这两种物质的溶液中分别加入NaOH溶液,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,和硝酸铜反应生成氢氧化铜沉淀和硝酸钠,反应的化学方程式:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓,2NaOH+Cu(NO3)2═2NaNO3+Cu(OH)2↓;故填:蓝;2NaOH+CuSO4═Na2SO4+Cu(OH)2↓或2NaOH+Cu(NO3)2═2NaNO3+Cu(OH)2↓;
②向硫酸铜、硝酸铜两种物质的溶液中分别加入BaCl2溶液,能发生反应的物质是硫酸铜,是因为硫酸铜和氯化钡反应生成硫酸钡沉淀和氯化铜,另外一种物质不反应;故填:CuSO4;
③向硫酸铜溶液中,加入某纯净物的溶液,能同时将铜离子和硫酸根离子转变成沉淀,该纯净物的化学式为Ba(OH)2,是因为氢氧化钡和硫酸铜反应生成氢氧化铜沉淀和硫酸钡沉淀;故填:Ba(OH)2;
(3)①上述两位同学的推测都有不足,理由是甲:碳酸钙不溶于水,因此溶液中不含有碳酸钙;乙:氢氧化钙和碳酸钠能发生反应生成碳酸钙和氢氧化钠,不能共存;故填:碳酸钙不溶于水,因此溶液中不含有碳酸钙;氢氧化钙和碳酸钠不能共存;
②我的推测是:该溶液中一定存在的溶质是没有反应的氯化钠和碳酸钠和氢氧化钙反应生成的氢氧化钠;故填:氯化钠、氢氧化钠;
氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠;氢氧化钙和碳酸钠可能恰好完全反应,也可能其中一个过量,碳酸钠能与氯化钙反应生成碳酸钙,氢氧化钙能与碳酸钠反应生成碳酸钙,故实验过程如下:
实验操作 | 实验现象 | 结论 |
a:CaCl2 | b产生白色沉淀 | 除了②推测的一定存在的溶质外,该溶液中还含有:c碳酸钠 |
d:Na2CO3 | e产生白色沉淀 | 除了②推测的一定存在的溶质外,该溶液中还含有:f氢氧化钙 |
上述两实验均无明显现象 | 只含有②推测的一定存在的溶质 |
故答案为:CaCl2;产生白色沉淀;碳酸钠;Na2CO3;产生白色沉淀;氢氧化钙。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】今天是学校实验室的开放日,九年级1班某小组的同学来到实验室准备练习制取和收集氧气,实验员为他们提供了下列装置、仪器和药品。装置和仪器:药品:氯酸钾、过氧化氢溶液、二氧化锰。
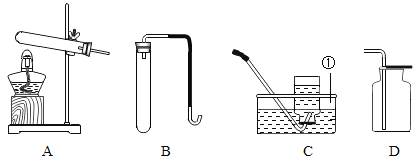
(1)标出有序号的仪器名称:①_____________。
(2)张勇同学选择了A和D制取、收集氧气,如果要检验氧气是否收集满,可以用带火星的小木条检验,检验方法是_____________。
(3)除可用于收集氧气外,D装置还可用于收集①氢气、②氮气、③二氧化碳、④一氧化碳四种气体中的________(填序号)。
(4)若用B制取氧气,其化学方程式是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小金通过实验室制取和收集二氧化碳的方法获得了一瓶二氧化碳气体。接着利用这瓶二氧化碳气体完成了图示实验,观察到蜡烛火焰自下而上依次熄灭。下列说法错误的是( )
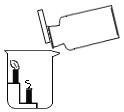
A.实验室制取二氧化碳的药品为块状大理石和稀硫酸
B.实验室可采用向上排空气法收集二氧化碳
C.图示实验可说明二氧化碳密度比空气大
D.图示实验可说明二氧化碳不支持蜡烛的燃烧
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】医用消毒酒精为75%的乙醇溶液,化工生产中可用A(主要成分的化学式为C8H18)作原料,经以下流程制取乙醇:
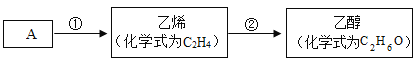
(1)步骤①的转化属于_____(选填“化学”或“物理”)变化。
(2)步骤②是乙烯和含两种元素的化合物B发生化合反应,则B中所含元素是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是拉瓦锡实验所用的氧化汞分解微观示意图,下列说法不正确的是
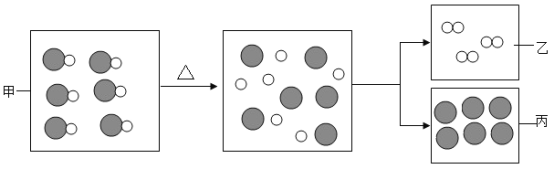
A.氧化汞属于化合物
B.构成物质的微粒是在不断运动的
C.生成物丙是金属汞
D.化学反应前后微粒的个数不改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
八达岭高铁站
八达岭高铁站位于世界文化遗产长城核心景区,车站最大埋深102米,地下建筑面积3.6万平方米,是目前国内埋深最大的高铁地下车站;车站主洞数量多、洞型复杂、交叉节点密集,是目前国内最复杂的暗挖洞群车站;车站两墙单洞开挖跨度达32.7米,是目前国内单拱跨度最大的暗挖铁路隧道;旅客进出站电梯提升高度62米,扶梯梯级每块重15千克,却可以承受3吨的瞬间冲击力。八达岭长城站首次采用环形救援廊道设计,具备了紧急情况下快速无死角救援的条件。服务冬奥、八达岭景区、八达岭长城等多方面需要,埋深之所以大,特别是保护我国近代工业的象征——青龙桥车站人字形线路的需要。配置了污水处理站,采用先进的曝气生物滤池过调系统,通过絮凝沉淀、生物滤池、活性类等处理工艺,达到污水达标排放。
阅读文本,回答问题:
(1)进出候车大厅的塑料活动挡板属于______材料。
(2)超长钢轨的使用为高铁的高速运行。工业上炼铁的化学方程式是________。
(3)电梯扶梯使用了大量的不锈钢护板,体现金属的___性,电梯梯级应具备的特性是___。
(4)污水处理环节中活性炭的作用是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】节能减排中“减排”的重要手段是合理利用二氧化碳。科学家正致力于将二氧化碳转化为甲烷,其反应的微观示意图如图所示。下列叙述正确的是( )
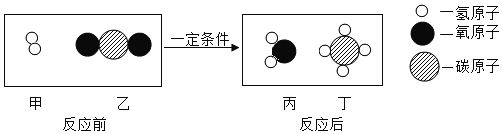
A.反应前后分子的总数不变
B.甲、乙、丙、丁四种物质中属于氧化物的有三种
C.参加反应的甲分子与生成的丙分子个数比为1:1
D.参加反应的甲物质和乙物质的质量比为2:11
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年 5月 18日电,国内首台 80吨液氧甲烷火箭发动机——“天鹊”发动机(TQ-12)日前试车成功,这意味着我国民营航天力量首次掌握了百吨级液体火箭发动机关键技术,并具备发动机研制所需的保障能力。试回答下列问题:
(1)“液氧”通常为____色液体。工业上常采用分离液态空气方法获得氧气,此方法是利用液态空气各成分的______(填“熔点”或“沸点”)不同将其分离的;
(2)写出甲烷燃烧的化学方程式_______;
(3)氧气的用途很广,请说出一例氧气的用途________;
(4)过氧化钠(Na2O2)作供氧剂,发生如下反应![]() ,Na2O2中氧元素的化合价为_______,过氧化钙(CaO2) 与水发生类似反应,请写出该反应的化学方程式_______。
,Na2O2中氧元素的化合价为_______,过氧化钙(CaO2) 与水发生类似反应,请写出该反应的化学方程式_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com