
分析 反应前后固体的质量差即为生成氧气的质量;根据氧气的质量可以计算氯酸钾的质量,进而求质量分数.
解答 解:根据质量守恒定律,生成氧气的质量为:16g-14.08g=1.92g;
设原混合物中氯酸钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
245 96
x×$\frac{1}{3}$ 1.92g
$\frac{245}{x×\frac{1}{3}}=\frac{96}{1.92g}$
x=14.7g
原混合物中MnO2的质量为:16g-14.7g=1.3g
答:原混合物中KClO3和MnO2各14.7g、1.3g.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验目的 | 实验方案 | |
| A | 探究燃烧所有条件 | 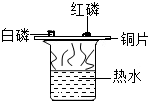 |
| B | 探究铁生锈所有条件 | 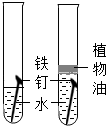 |
| C | 探究MnO 2 对过氧化氢溶液 分解速度的影响 | 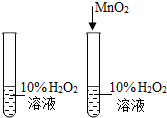 |
| D | 实验室制取二氧化碳的药品研究 | 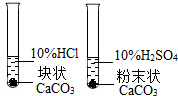 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验 | 实验操作 | 实验现象 | 结论与解释 |
| 试管1 | 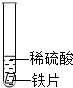 | 铁片表面产生气泡较慢,溶液变为浅绿色. | (1)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜的. (2)甲同学得到的结论是猜想1正确. |
| 试管2 |  | 铬片表面产生气泡较快,溶液变为蓝色. | |
| 试管3 | 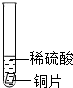 | 铜片上没有变化 |
| 实验 | 实验操作 | 实验现象 | 结论与解释 |
| 试管4 | 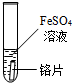 | (1)甲同学的结论正确. (2)请写出铬与硫酸铜反应的化学方程式Cr+CuSO4=CrSO4+Cu. | |
| 试管5 | 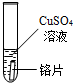 |
| 实验操作和实验现象 | 结论与解释 |
| 甲同学的结论正确. |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
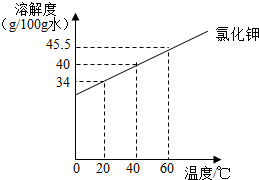 根据下表实验,回答相关问题.
根据下表实验,回答相关问题.| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 在盛有100g水的烧杯中,加入25g氯化钾,搅拌,恢复到20℃ | 全部溶解 |
| Ⅱ | 再加Xg氯化钾,搅拌,恢复到20℃,恰好饱和 | 全部溶解 |
| Ⅲ | 再加6g氯化钾,搅拌,恢复到20℃ | 固体不溶 |
| Ⅳ | 加热至40℃ | 全部溶解 |
| Ⅴ | 冷却至20℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com