
ЁОЬтФПЁПЯТСагІгУЃЌЯрЙиЛЏбЇЗНГЬЪНМАЛљБОЗДгІРраЭЖМе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
A. вЛбѕЛЏЬМгУгкСЖЬњЃК4CO+Fe3O4![]() 3Fe+4CO2 жУЛЛЗДгІ
3Fe+4CO2 жУЛЛЗДгІ
B. гУЧтбѕЛЏИЦШмвКЮќЪеЖўбѕЛЏЬМЦјЬхЃКCaЃЈOHЃЉ2+CO2ЃНCaCO3Ё§+H2O ИДЗжНтЗДгІ
C. гУКЌгаЧтбѕЛЏТСЕФвЉЮяжЮСЦЮИЫсЙ§ЖржЂЃКAlЃЈOHЃЉ3+3HClЃНAlCl3+3H2O ИДЗжНтЗДгІ
D. ЪЕбщЪвМгШШИпУЬЫсМижЦШЁбѕЦјЃКK2MnO4![]() 2KMnO4+MnO2+O2Ёќ ЗжНтЗДгІ
2KMnO4+MnO2+O2Ёќ ЗжНтЗДгІ
ЁОД№АИЁПC
ЁОНтЮіЁП
AЁЂИУЛЏбЇЗНГЬЪНЪщаДЭъШЋе§ШЗЃЌЕЋИУЗДгІЕФЗДгІЮяОљЮЊЛЏКЯЮяЃЌВЛЪєгкжУЛЛЗДгІЃЌЙЪбЁЯюДэЮѓЁЃ
BЁЂИУЛЏбЇЗНГЬЪНЪщаДЭъШЋе§ШЗЃЌЕЋИУЗДгІВЛЪЧСНжжЛЏКЯЮяЯрЛЅНЛЛЛГЩЗжЩњГЩСНжжаТЕФЛЏКЯЮяЕФЗДгІЃЌВЛЪєгкИДЗжНтЗДгІЃЌЙЪбЁЯюДэЮѓЁЃ
CЁЂИУЛЏбЇЗНГЬЪНЪщаДЭъШЋе§ШЗЃЌЧвИУЗДгІЪЧСНжжЛЏКЯЮяЯрЛЅНЛЛЛГЩЗжЩњГЩСНжжаТЕФЛЏКЯЮяЕФЗДгІЃЌЪєгкИДЗжНтЗДгІЃЌЙЪбЁЯюе§ШЗЁЃ
DЁЂИпУЬЫсМидкМгШШЬѕМўЯТЩњГЩУЬЫсМиЁЂЖўбѕЛЏУЬКЭбѕЦјЃЌе§ШЗЕФЛЏбЇЗНГЬЪНЪЧ2KMnO4![]() K2MnO4+MnO2+O2ЁќЃЌЙЪбЁЯюДэЮѓЁЃ
K2MnO4+MnO2+O2ЁќЃЌЙЪбЁЯюДэЮѓЁЃ
ЙЪбЁЃКCЁЃ


 УППЮБиСЗЯЕСаД№АИ
УППЮБиСЗЯЕСаД№АИ ЧЩбЇЧЩСЗЯЕСаД№АИ
ЧЩбЇЧЩСЗЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГаЃЛЏбЇаЫШЄаЁзщВЮЙлжЦМюГЇКѓЃЌЛёЕУвдЯТаХЯЂВЂЖдЯрЙиЮЪЬтНјаабаОПЃЎ
ВњЦЗдРэЃКИУГЇВЩгУЁАКюЪЯжЦМюЗЈЁБЩњВњЛЏЙЄВњЦЗЉЉДПМюЃЈNa2CO3ЃЉКЭЛЏЗЪNH4ClЃЎ
ЩњВњдРэЪЧЃКНЋNH3КЭCO2ЭЈШыБЅКЭЪГбЮЫЎжаЕУЕНNaHCO3ОЇЬхКЭNH4ClШмвКЃЌЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК_____ЃЛКѓЗжРыГіNaHCO3ЃЌМгШШжЦЕУДПМюЃЎ
ЩњВњСїГЬЃК
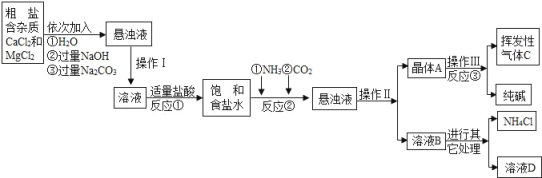
ЯрЙизЪСЯЃК
ЃЈ1ЃЉNH4Cl ![]() NH3Ёќ+HClЁќ
NH3Ёќ+HClЁќ
ЃЈ2ЃЉвбжЊ20ЁцЪБгаЙиЮяжЪЕФШмНтЖШШчЯТЃЈЦјЬхжИ1ЬхЛ§ЫЎжаФмШмНтЕФЦјЬхЬхЛ§ЃЉ
ЮяжЪ | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
ШмНтЖШ | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
ЮЪЬтЬжТлЃК
ЃЈ1ЃЉВйзїЂёЁЂЂђжаЃЌЯрЭЌВйзїЕФУћГЦЮЊ_____ЃЎЗДгІЂйжаЗЂЩњСЫСНИіЗДгІЃЌаДГіЦфжавЛИіЛЏбЇЗНГЬЪНЃК_____ЃЌЗДгІЂйМгЪЪСПЕФбЮЫсЃЌЪЪСПЪЧжИ_____ЃЎ
ЃЈ2ЃЉМьбщЛгЗЂадЦјЬхCЕФЗНЗЈ_____ЃЎ
ЃЈ3ЃЉЩЯЪіЩњВњСїГЬжаПЩбЛЗЪЙгУЕФЪЧ_____ЃЈЬюађКХЃЉЃЎ
AЛгЗЂадЦјЬхCЃЛ BШмвКDЃЛ CЧтбѕЛЏУОЃЛDЛЏЗЪNH4Cl
зщГЩШЗЖЈЃК
ЃЈ1ЃЉГЦШЁвЛЖЈжЪСПЕФДПМюбљЦЗЃЌОЖрДЮГфЗжМгШШКѓЃЌдйГЦжиЃЌжЪСПЮоБфЛЏЃЛ
ЃЈ2ЃЉСэШЁЩйСПДПМюбљЦЗМгШыЪЪСПЫЎЃЌбљЦЗЭъШЋШмНтЃЌЯђИУШмвКжаМгШыЙ§СПЯЁHNO3ЃЌдйЕЮМгAgNO3ШмвКЃЌгаАзЩЋГСЕэЃЎгЩЩЯЪіЪЕбщПЩШЗЖЈДПМюбљЦЗКЌгадгжЪ_____ЃЈаДЛЏбЇЪНЃЉЃЎ
КЌСПВтЖЈЃК
ЪЕбщвЛ | ЪЕбщЖў | ЪЕбщШ§ | ЪЕбщЫФ | |
ЙЬЬхЛьКЯЮяШмвКжЪСП | 100g | 100g | 100g | 100g |
МгШыCaCl2ШмвКжЪСП | 10g | 20g | 30g | 40g |
ЩњГЩЕФГСЕэЕФжЪСП | 4g | m | 10g | 10g |
ГЦШЁИУДПМюбљЦЗ44gЙЬЬхЛьКЯЮяЃЌМгЫЎХфГЩ400gШмвКЃЌЦНОљЗжЮЊЫФЗнЃЌШЛКѓЗжБ№МгШывЛЖЈжЪСПЗжЪ§ЕФCaCl2ШмвКЃЌЪЕбщЪ§ОнМћБэЃК
ЧыЗжЮіБэжаЪ§ОнЛиД№ВЂМЦЫуЃК
ЃЈ1ЃЉmЃН_____gЃЛ
ЃЈ2ЃЉдкЪЕбщШ§жаЃЌЭъШЋЗДгІКѓЫљЕУШмвКжаШмжЪТШЛЏФЦЕФжЪСПЗжЪ§ЪЧЖрЩйЃП_____ЃЈвЊЧѓаДМЦЫуЙ§ГЬЃЌНсЙћБЃСє0.1%ЃЉ
змНсЗДЫМЃК
ЧыЭЈЙ§МЦЫуВЂНсКЯЯТБэХаЖЯДЫДПМюбљЦЗЕШМЖЮЊ_____ЦЗЃЌдкЩЯЪіДПМюКЌСПВтЖЈжаЃЌНЋCaCl2ШмвКИФЮЊBaCl2ШмвКЃЌВтЖЈЮѓВюЛсМѕаЁЃЎ
ЙЄвЕДПМюБъзМЃКЃЈNa2CO3% ЃЉ | |||
гХЕШЦЗ | вЛЕШЦЗ | КЯИёЦЗ | ДЮЦЗ |
Ён95 | Ён80 | Ён75 | Ём40 |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЫФжжЮяжЪдквЛЖЈЬѕМўЯТГфЗжЛьКЯЗДгІЃЌВтЕУЗДгІЧАКѓИїЮяжЪЕФжЪСПЗжЪ§ШчЭМЫљЪОЃЌдђгаЙиЫЕЗЈжае§ШЗЕФЃЈ ЃЉ

A. БћвЛЖЈЪЧЛЏКЯЮя
B. ИУЗДгІПЩФмЪЧЫЎЕФЕчНт
C. вввЛЖЈЪЧИУЗДгІЕФДпЛЏМС
D. ВЮМгЗДгІЛђЩњГЩЕФМзКЭБћЕФжЪСПБШЮЊ19ЃК41
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМзЁЂввЁЂБћШ§жжЙЬЬхЮяжЪЕФШмНтЖШЧњЯпШчЭМЫљЪОЃЌЧыЛиД№ЁЃ
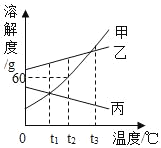
ЃЈ1ЃЉЮТЖШЮЊ_____ЁцЪБЃЌМзЁЂввЁЂБћШ§жжЮяжЪЕФШмНтЖШДѓаЁЙиЯЕЮЊввЃОМзЃНБћЁЃ
ЃЈ2ЃЉШєМзжаКЌгаЩйСПввЃЌПЩгУ_____ЕФЗНЗЈЬсДПМзЁЃ
ЃЈ3ЃЉt2ЁцЪБЃЌдк50gЫЎжаМгШы_____gМзЮяжЪЃЌЧЁКУаЮГЩБЅКЭШмвКЁЃ
ЃЈ4ЃЉНгНќБЅКЭЕФБћШмвКЃЌдкБЃГжШмжЪжЪСПЗжЪ§ВЛБфЕФЧщПіЯТзЊБфЮЊБЅКЭШмвКЃЌПЩВЩШЁЕФЗНЗЈЪЧ_____ЁЃ
ЃЈ5ЃЉНЋt3ЁцЪБЃЌЕШжЪСПЕФМзЁЂввЁЂБћШ§жжЮяжЪЕФБЅКЭШмвКЃЌЭЌЪБНЕЮТЕНt1ЁцЃЌЫљЕУШмвКжаШмжЪжЪСПЗжЪ§гЩДѓЕНаЁЕФЫГађЪЧ_____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПt2ЁцЪБЃЌНЋМзЁЂввИї80gЗжБ№ЗХЕНЪЂга100gЫЎЕФСНИіЩеБжаЃЌГфЗжШмНтКѓЃЌЛжИДЕНt2ЁцЃЌЯжЯѓШчЭМЃЌМзКЭввЕФШмНтЖШЧњЯпШчЭМЁЃЧыНсКЯЭМЪОЛиД№ЯТСаЮЪЬтЃК

ЃЈ1ЃЉФмЫЕУїЙЬЬхМзЖдгІЕФШмНтЖШЧњЯпЪЧaЕФжЄОнЪЧ_______ЁЃ
ЃЈ2ЃЉЯТСаЙигкt2 ЁцЪБЃЌМзЁЂввЫљЕУШмвКЕФЫЕЗЈВЛе§ШЗЕФЪЧ______ЃЈЬюађКХЃЉЁЃ
A ШмжЪжЪСПЃКМз<вв B ввЮЊБЅКЭШмвК
C ШмжЪжЪСПЗжЪ§ЃКМз=вв D НЋШмвКНЕЮТжСt1 ЁцЪБЃЌМзЁЂввЕФШмНтЖШЯрЕШЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПОХФъМЖзлКЯЪЕМљЛюЖЏаЁзщгУЙ§бѕЛЏЧтШмвККЭЖўбѕЛЏУЬРДжЦШЁбѕЦјЃЌзюКѓЫљЕУЕНЦјЬхжЪСПгыЪБМфЕФЙиЯЕШчЭМЫљЪОЃЎ
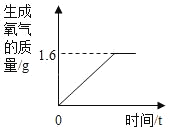
ЃЈ1ЃЉЙ§бѕЛЏЧтжабѕдЊЫиЕФЛЏКЯМлЪЧ_____МлЃЛ
ЃЈ2ЃЉЗДгІЩњГЩбѕЦјЕФжЪСПЮЊ_____g
ЃЈ3ЃЉМЦЫуВЮМгЗДгІЕФЙ§бѕЛЏЧтЕФжЪСПЃП_____ЃЈаДГіМЦЫуЙ§ГЬЃЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
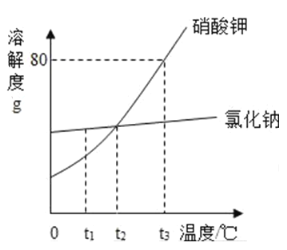
ЁОЬтФПЁПЧыИљОнШчЭМЫљЪОЕФШмНтЖШЧњЯпЛиД№ЯТСаЮЪЬтЃЎ
ЃЈ1ЃЉt1ЁцЪБЃЌЯѕЫсМиШмНтЖШ_____ЃЈбЁЬюЁАЃОЁБЁЂЁАЃМЁБЛђЁАЃНЁБЃЉТШЛЏФЦЕФШмНтЖШЃЛ
ЃЈ2ЃЉШєЯыЪЙt2ЁцЕФЯѕЫсМиЕФВЛБЅКЭШмвКБфГЩИУЮТЖШЯТЕФБЅКЭШмвКЃЌзюМђЕЅЕФЗНЗЈЪЧ_____ЃЛ
ЃЈ3ЃЉt3ЁцЪБНЋ60gЯѕЫсМиШмвК50gЫЎжаЃЌЫљЕУШмвКжаШмжЪгыШмМСЕФжЪСПБШЮЊ_____ЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдФЖСЯТУцПЦЦеЖЬЮФЁЃ
ЫЕЦ№ЖўбѕЛЏСђЃЈSO2ЃЉЃЌФуПЩФмЪзЯШЯыЕНЫќЪЧПеЦјжЪСПВЅБЈжаЬсМАЕФДѓЦјЮлШОЮяЁЃЦфЪЕФуецЕФСЫНтSO2Т№ЃПФбЕРЫќжЛЪЧгаКІЮяжЪТ№ЃП
SO2гыЪГЦЗЙЄвЕ
SO2зїЮЊЗРИЏМСЁЂЦЏАзМСКЭПЙбѕЛЏМСЙуЗКгУгкЪГЦЗаавЕЁЃЦЯЬбОЦФ№жЦжаЪЪСПЬэМгSO2ЃЌПЩЗРжЙЦЯЬбОЦдкГТФ№КЭжќВиЙ§ГЬжаБЛбѕЛЏЃЌвжжЦЦЯЬбжжаЮЂЩњЮяЕФЛюЖЏЁЃЪГЬЧМгЙЄЙ§ГЬжаПЩЪЙгУSO2НјааЭбЩЋЁЃАДееЮвЙњЁЖЪГЦЗЬэМгМСЪЙгУБъзМЃЈGB2760-2014ЃЉЁЗЃЌКЯРэЪЙгУSO2ВЛЛсЖдШЫЬхНЁПЕдьГЩЮЃКІЁЃ
БъзМжаВПЗжЪГЦЗSO2ЕФзюДѓВаСєСП
ЪГЦЗ | УлНЄ | ЦЯЬбОЦ | ЪГЬЧ | ЫЎЙћИЩ | ЧЩПЫСІ | ЙћЪпж |
зюДѓВаСєСП | 0.35g/kg | 0.25g/L | 0.1g/kg | 0.1g/kg | 0.1g/kg | 0.05g/kg |
SO2гыСђЫсЙЄвЕ
СђЫсЪЧживЊЕФЛЏЙЄдСЯЃЌЙЄвЕжЦСђЫсЕФЙиМќВНжшЪЧSO2ЕФЛёШЁКЭзЊЛЏЁЃЙЄвЕРћгУСђжЦСђЫсЕФжївЊЙ§ГЬЪОвтШчЯТЃК
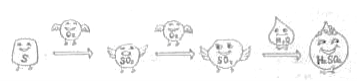
СђЫсЙЄвЕЕФЮВЦјжаКЌгаЩйСПSO2ЃЌШєжБНгХХЗХЛсЮлШОПеЦјЃЌВЂЕМжТСђЫсаЭЫсгъЁЃЙЄвЕЩЯПЩЯШгУАБЫЎЮќЪеЃЌдйгУСђЫсДІРэЃЌНЋжиаТЩњГЩЕФSO2бЛЗРћгУЁЃ
SO2гыЛЏЪЏШМСЯ
ЛЏЪЏШМСЯжаЕФУКЭЈГЃКЌгаСђдЊЫиЃЌжБНгШМЩеЛсВњЩњSO2ЁЃЮЊСЫМѕЩйУКШМЩеВњЩњЕФSO2ЮлШОПеЦјЃЌПЩвдВЩШЁЁАЬсИпШМУКжЪСПЃЌИФНјШМЩеММЪѕЁБЕФДыЪЉЃЌР§ШчЃЌЖдШМУКНјааЭбСђЁЂЙЬСђДІРэЃЛЛЙПЩвдВЩШЁЁАгХЛЏФмдДНсЙЙЁЂМѕЩйШМУКЪЙгУЁБЕФДыЪЉЃЌР§ШчЃЌББОЉДѓСІЭЦЙуЕФЁАУКИФЦјЁЂУКИФЕчЁБЙЄГЬЃЌгааЇИФЩЦСЫПеЦјжЪСПЁЃ
ЯждкЃЌФуЖдSO2вЛЖЈгаСЫаТЕФШЯЪЖЃЌдкНёКѓЕФЛЏбЇбЇЯАжаФуЖдSO2ЛЙЛсгаИќШЋУцЕФШЯЪЖЃЁ
вРОнЮФеТФкШнЛиД№ЯТСаЮЪЬтЁЃ
ЃЈ1ЃЉАДееЙњМвБъзМЃЌЪГЬЧжаЕФSO2зюДѓВаСєСПЮЊ g/kgЁЃ
ЃЈ2ЃЉЦЯЬбОЦФ№жЦЙ§ГЬжаSO2ЕФзїгУЪЧ ЁЃ
ЃЈ3ЃЉгУСђжЦСђЫсЕФжївЊЙ§ГЬжаЃЌЩцМАЕНЕФКЌСђЮяжЪгаSЁЂ КЭH2SO4ЁЃ
ЃЈ4ЃЉСђЫсЙЄвЕЩњВњжаЃЌЮќЪеЮВЦјжаSO2ЕФЮяжЪЪЧ ЁЃ
ЃЈ5ЃЉЯТСаДыЪЉФмМѕЩйSO2ХХЗХЕФЪЧ ЃЈЬюађКХЃЉЁЃ
AЃЎНЋУКПщЗлЫщ BЃЎЖдШМУКНјааЭбСђ
CЃЎЭЦЙуУКИФЦјЁЂУКИФЕч DЃЎбЛЗРћгУЙЄвЕЮВЦјжаЕФSO2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКГѕжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПAЁЂBЁЂCЁЂDЁЂEЁЂFЁЂGЁЂHАЫжжЮяжЪЃЌгаЯТЭМЫљЪОЙиЯЕЃКЦфжаAЪЧвЛжжАЕзЯЩЋЙЬЬхЃЌBЪЧКкЩЋЙЬЬхЃЌDФмЪЙДјЛ№аЧЕФФОЬѕИДШМЃЌE ЁЂFЖМЪЧЮоЩЋвКЬхЃЌGЪЧФОЬПЃЌHЪЧвЛжжФмЪЙГЮЧхЪЏЛвЫЎБфЛызЧЕФЦјЬхЃЌдкЂкЕФЗДгІЧАКѓBЕФжЪСПКЭЛЏбЇаджЪЖМВЛИФБфЁЃ

ЧыФуИљОнЩЯЪіаХЯЂЃЌЭЦЖЯГіЯТСаЮяжЪЁЃ
ЃЈ1ЃЉЬюУћГЦЃКA ЁЂB ЃЌC ЁЂH ЁЃ
ЃЈ2ЃЉаДГіЗДгІЂлЕФЛЏбЇЗНГЬЪНЃЌВЂжИГіЗДгІЕФЛљБОРраЭЃК
Ђл ЃЛ ЗДгІ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com