
”¾ĢāÄæ”æijŠ£»ÆѧŠĖȤŠ”×é²Ī¹ŪÖĘ¼ī³§ŗ󣬻ńµĆŅŌĻĀŠÅĻ¢²¢¶ŌĻą¹ŲĪŹĢā½ųŠŠŃŠ¾æ£®
²śĘ·ŌĄķ£ŗøĆ³§²ÉÓĆ”°ŗīŹĻÖĘ¼ī·Ø”±Éś²ś»Æ¹¤²śĘ·©©“æ¼ī£ØNa2CO3£©ŗĶ»Æ·ŹNH4Cl£®
Éś²śŌĄķŹĒ£ŗ½«NH3ŗĶCO2ĶØČė±„ŗĶŹ³ŃĪĖ®ÖŠµĆµ½NaHCO3¾§ĢåŗĶNH4ClČÜŅŗ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ_____£»ŗó·ÖĄė³öNaHCO3£¬¼ÓČČÖʵƓæ¼ī£®
Éś²śĮ÷³Ģ£ŗ
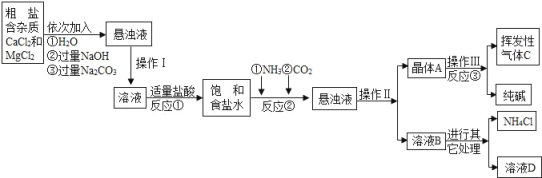
Ļą¹Ų׏ĮĻ£ŗ
£Ø1£©NH4Cl ![]() NH3”ü+HCl”ü
NH3ӟ+HClӟ
£Ø2£©ŅŃÖŖ20”ꏱӊ¹ŲĪļÖŹµÄČܽā¶ČČēĻĀ£ØĘųĢåÖø1Ģå»żĖ®ÖŠÄÜČܽāµÄĘųĢåĢå»ż£©
ĪļÖŹ | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
Čܽā¶Č | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
ĪŹĢāĢÖĀŪ£ŗ
£Ø1£©²Ł×÷¢ń”¢¢ņÖŠ£¬ĻąĶ¬²Ł×÷µÄĆū³ĘĪŖ_____£®·“Ó¦¢ŁÖŠ·¢ÉśĮĖĮ½øö·“Ó¦£¬Š“³öĘäÖŠŅ»øö»Æѧ·½³ĢŹ½£ŗ_____£¬·“Ó¦¢Ł¼ÓŹŹĮæµÄŃĪĖį£¬ŹŹĮæŹĒÖø_____£®
£Ø2£©¼ģŃé»Ó·¢ŠŌĘųĢåCµÄ·½·Ø_____£®
£Ø3£©ÉĻŹöÉś²śĮ÷³ĢÖŠæÉŃ»·Ź¹ÓƵďĒ_____£ØĢīŠņŗÅ£©£®
A»Ó·¢ŠŌĘųĢåC£» BČÜŅŗD£» CĒāŃõ»ÆĆ¾£»D»Æ·ŹNH4Cl
×é³ÉČ·¶Ø£ŗ
£Ø1£©³ĘČ”Ņ»¶ØÖŹĮæµÄ“æ¼īѳʷ£¬¾¶ą“Ī³ä·Ö¼ÓČČŗó£¬ŌŁ³ĘÖŲ£¬ÖŹĮæĪŽ±ä»Æ£»
£Ø2£©ĮķȔɣĮæ“æ¼īѳʷ¼ÓČėŹŹĮæĖ®£¬ŃłĘ·ĶźČ«Čܽā£¬ĻņøĆČÜŅŗÖŠ¼ÓČė¹żĮæĻ”HNO3£¬ŌŁµĪ¼ÓAgNO3ČÜŅŗ£¬ÓŠ°×É«³Įµķ£®ÓÉÉĻŹöŹµŃéæÉČ·¶Ø“æ¼īѳʷŗ¬ÓŠŌÓÖŹ_____£ØŠ“»ÆѧŹ½£©£®
ŗ¬Įæ²ā¶Ø£ŗ
ŹµŃéŅ» | ŹµŃ鶞 | ŹµŃéČż | ŹµŃéĖÄ | |
¹ĢĢå»ģŗĻĪļČÜŅŗÖŹĮæ | 100g | 100g | 100g | 100g |
¼ÓČėCaCl2ČÜŅŗÖŹĮæ | 10g | 20g | 30g | 40g |
Éś³ÉµÄ³ĮµķµÄÖŹĮæ | 4g | m | 10g | 10g |
³ĘČ”øĆ“æ¼īѳʷ44g¹ĢĢå»ģŗĻĪļ£¬¼ÓĖ®Åä³É400gČÜŅŗ£¬Ę½¾ł·ÖĪŖĖÄ·Ż£¬Č»ŗó·Ö±š¼ÓČėŅ»¶ØÖŹĮæ·ÖŹżµÄCaCl2ČÜŅŗ£¬ŹµŃ鏿¾Ż¼ū±ķ£ŗ
Ēė·ÖĪö±ķÖŠŹż¾Ż»Ų“š²¢¼ĘĖć£ŗ
£Ø1£©m£½_____g£»
£Ø2£©ŌŚŹµŃéČżÖŠ£¬ĶźČ«·“Ó¦ŗóĖłµĆČÜŅŗÖŠČÜÖŹĀČ»ÆÄʵÄÖŹĮæ·ÖŹżŹĒ¶ąÉŁ£æ_____£ØŅŖĒ󊓼ĘĖć¹ż³Ģ£¬½į¹ū±£Įō0.1%£©
×ܽį·“Ė¼£ŗ
ĒėĶعż¼ĘĖć²¢½įŗĻĻĀ±ķÅŠ¶Ļ“Ė“æ¼īѳʷµČ¼¶ĪŖ_____Ę·£¬ŌŚÉĻŹö“æ¼īŗ¬Įæ²ā¶ØÖŠ£¬½«CaCl2ČÜŅŗøÄĪŖBaCl2ČÜŅŗ£¬²ā¶ØĪó²ī»į¼õŠ”£®
¹¤Ņµ“æ¼ī±ź×¼£ŗ£ØNa2CO3% £© | |||
ÓŵČĘ· | Ņ»µČĘ· | ŗĻøńĘ· | “ĪĘ· |
”Ż95 | ”Ż80 | ”Ż75 | ”Ü40 |
”¾“š°ø”æNaCl+NH3+CO2+H2O£½NaHCO3”ż+NH4Cl ¹żĀĖ NaOH+HClØTNaCl+H2O µĪµ½ĪŽĘųÅŻ·Å³öĪŖÖ¹ ½«ĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ®ÖŠ£¬¹Ū²ģŹĒ·ń±ä»ė×Ē A”¢B NaCl 8 10.1% ÓŵČ
”¾½āĪö”æ
øł¾Ż“æ¼īµÄÖĘČ”ŅŌ¼°ÓŠ¹ŲµÄĪļÖŹµÄŠŌÖŹ½ųŠŠ·ÖĪö”£¹żĀĖŹĒ·ÖĄė²»ČÜŠŌ¹ĢĢåŗĶŅŗĢåµÄ·½·Ø£¬ĒāŃõ»ÆÄĘŗĶĢ¼ĖįÄʶ¼ÄÜÓėŃĪĖį·¢Éś»Æѧ·“Ó¦£¬ŃĪĖįÄÜÓėĢ¼ĖįÄĘ·“Ӧɜ³É¶žŃõ»ÆĢ¼ĘųĢ壻¶žŃõ»ÆĢ¼ÄÜŹ¹³ĪĒåµÄŹÆ»ŅĖ®±ä»ė×Ē£»×é³ÉČ·¶Ø£ŗøł¾Ż±ķøńĢį¹©µÄŹż¾Ż·ÖĪöµĆ³ömµÄÖµ£¬Ķعż¼ĘĖćĢ¼ĖįÄʵÄŗ¬Įæ£¬Č·¶ØĘäµČ¼¶”£
[²śĘ·ŌĄķ]½«NH3ŗĶCO2ĶØČė±„ŗĶŹ³ŃĪĖ®ÖŠµĆµ½NaHCO3¾§ĢåŗĶNH4ClČÜŅŗ£¬øĆ·“Ó¦ŹĒĀČ»ÆÄĘ”¢°±Ęų”¢¶žŃõ»ÆĢ¼ŗĶĖ®·“Ӧɜ³ÉĢ¼ĖįĒāÄĘŗĶĀČ»Æļ§£¬¹ŹĢī£ŗNaCl+NH3+CO2+H2O£½NaHCO3”ż+NH4Cl£»
[ĪŹĢāĢÖĀŪ]£Ø1£©²Ł×÷¢ń”¢¢ņÖŠ£¬¶¼ŹĒµĆµ½ĮĖ¹ĢĢåŗĶŅŗĢ壬ŹōÓŚ¹żĀĖ·Ø·ÖĄė»ģŗĻĪļ£¬ČÜŅŗÖŠµÄĒāŃõ»ÆÄĘŗĶĢ¼ĖįÄʶ¼ÄÜÓėŃĪĖį·“Ó¦£¬Ģ¼ĖįÄĘÓėŃĪĖį·“Ӧɜ³É¶žŃõ»ÆĢ¼ĘųĢ壬µĪČėµÄŃĪĖįµ±ĪŽĘųÅŻĆ°³öŹ±ĪŖÖ¹£¬¹ŹĢī£ŗ¹żĀĖ£¬NaOH+HClØTNaCl+H2O»ņNa2CO3+2HCl£½2NaCl+H2O+CO2”ü£¬µĪµ½ĪŽĘųÅŻ·Å³öĪŖÖ¹£»
£Ø2£©Ģ¼ĖįĒāÄĘŹÜČČ·Ö½āÉś³ÉµÄ¶žŃõ»ÆĢ¼ÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬¹Ź¼ģŃ鶞Ńõ»ÆĢ¼Ź¹ÓƵďĒŹÆ»ŅĖ®£¬¹ŹĢī£ŗ½«ĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ®ÖŠ£¬¹Ū²ģŹĒ·ń±ä»ė×Ē£»
£Ø3£©A”¢µĆµ½µÄ»Ó·¢ŠŌĘųĢåCŹĒ¶žŃõ»ÆĢ¼£¬æÉŅŌŃ»·ĄūÓĆ£»
B”¢µĆµ½µÄČÜŅŗDÖŠŗ¬ÓŠĀČ»ÆÄĘ£¬æÉŅŌŃ»·ĄūÓĆ£»
C”¢ĒāŃõ»ÆĆ¾²»ÄÜŃ»·ĄūÓĆ£»
D”¢ĀČ»Æļ§ŹĒ·“Ó¦µÄø±²śĪļ£¬²»ÄÜŃ»·ĄūÓĆ£»¹ŹĢī£ŗA”¢B”£
[×é³ÉČ·¶Ø]£ŗµĆµ½µÄ²śĪļÓėĖį»ÆµÄĻõĖįŅųČÜŅŗ·“Ó¦²śÉśĮĖ°×É«³Įµķ£¬ŌņæÉŅŌĶĘ³öѳʷ֊ŗ¬ÓŠĀČ»ÆÄĘ£¬¹ŹĢī£ŗNaCl£»
[ŗ¬Įæ²ā¶Ø]£Ø1£©øł¾Ż±ķøńæÉŅŌ擳ö£¬ŹµŃéŅ»ÖŠ10gĀČ»ÆøĘČÜŅŗÉś³É³ĮµķµÄÖŹĮæŹĒ4g£¬ŹµŃéČżÖŠ30gĀČ»ÆøĘČÜŅŗÉś³É³ĮµķµÄÖŹĮæŹĒ10g£¬±ķĆ÷ŹµŃ鶞֊µÄĀČ»ÆøĘČÜŅŗČ«²æ²Ī¼Ó·“Ó¦ĒŅÉś³É³ĮµķµÄÖŹĮæŹĒ8g£¬¹ŹĢī£ŗ8£»
£Ø2£©½ā£ŗÉč²Ī¼Ó·“Ó¦µÄNa2CO3µÄÖŹĮæĪŖx£¬Éś³ÉµÄĀČ»ÆÄʵÄÖŹĮæĪŖy
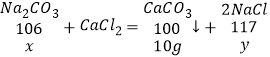
![]()
½āµĆ£ŗx£½10.6g y£½11.7g
ĀČ»ÆÄʵÄÖŹĮæ·ÖŹżĪŖ£ŗ![]() £½10.1%
£½10.1%
“š£ŗĀČ»ÆÄʵÄÖŹĮæ·ÖŹżĪŖ10.1%£»
[×ܽį·“Ė¼]Ģ¼ĖįÄʵÄŗ¬ĮæĪŖ£ŗ![]() £¾95%£¬¹ŹøĆ“æ¼īѳʷĪŖÓÅµČ£¬¹ŹĢī£ŗÓÅµČ”£
£¾95%£¬¹ŹøĆ“æ¼īѳʷĪŖÓÅµČ£¬¹ŹĢī£ŗÓÅµČ”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖ®ŹĒÉśĆüÖ®Ō“£¬ČĖĄąµÄÉś»īÉś²śĄė²»æŖĖ®”£
£Ø1£©×ŌĄ“Ė®ŹōÓŚ_____£ØĢī”°“æ¾»Īļ”±»ņ”°»ģŗĻĪļ”±£©”£¼ģŃé×ŌĄ“Ė®ŹĒÓ²Ė®»¹ŹĒČķĖ®£¬æÉŃ”ÓƵÄĪļÖŹŹĒ_____”£Éś»īÖŠ¼ČÄܽµµĶĖ®µÄÓ²¶Č£¬ÓÖÄÜɱ¾śĻū¶¾µÄ·½·ØŹĒ_____”£
£Ø2£©Ä³Ķ¬Ń§ŹÕ¼Æµ½Ņ»±ÓŠ³ōĪ¶µÄ»ģ×ĒĪŪĖ®£¬ĻČÓĆĀĖÖ½½ųŠŠ¹żĀĖ£¬¹żĀĖŹ±ĖłÓĆµÄ²£Į§ŅĒĘ÷ÓŠÉÕ±”¢²£Į§°ōŗĶ_____£¬¹żĀĖŗó·¢ĻÖĖ®ĖäČ»±äĒ壬µ«ŹĒŅĄČ»ÓŠ³ōĪ¶£¬Äܹ»³żČ„³ōĪ¶µÄ·½·ØŹĒ_____”£
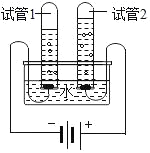
£Ø3£©øĆĶ¬Ń§ĪŖĮĖĢ½¾æĖ®µÄ×é³É£¬×öĮĖĖ®µÄµē½āŹµŃ飬ČēĶ¼ĖłŹ¾”£Š“³öøĆ·“Ó¦µÄĪÄ×Ö±ķ“ļŹ½£ŗ_____£¬ŹµŃéæŖŹ¼ŗó·¢ĻÖĮ½¼«¶¼ÓŠ_____Ć°³ö£¬ŹŌ¹Ü1ÖŠµÄĘųĢåŹĒ_____£»ŹŌ¹Ü2ÖŠµÄĘųĢåÄÜ_____£¬ŹĒ_____”£
£Ø4£©“ĖŹµŃéÄܹ»Ö¤Ć÷Ė®ŹĒÓÉ_____×é³ÉµÄ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»°ü¹ĢĢå·ŪÄ©æÉÄÜŗ¬ÓŠMg(NO3)2”¢CaCO3”¢NaOH”¢CuCl2”¢NaClŗĶCa(NO3)2ÖŠµÄŅ»ÖÖ»ņ¼øÖÖ£¬ĪŖČ·¶ØĘä×é³É£¬Ä³Ķ¬Ń§Éč¼ĘĮĖČēĻĀŹµŃé·½°ø£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
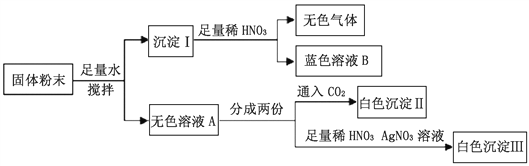
A. ³Įµķ¢ńŹĒĒāŃõ»ÆĶ³Įµķ
B. ĪŽÉ«ČÜŅŗAÖŠŅ»¶ØÓŠNaOH
C. Ō¹ĢĢå·ŪÄ©æĻ¶ØÓŠNaCl
D. Ō¹ĢĢå·ŪÄ©Ņ»¶ØÓŠCaCO3”¢NaOH”¢Mg(NO3)2”¢CuCl2ŗĶCa(NO3)2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ”°ŗź¹Ū”Ŗ”ŖĪ¢¹Ū”Ŗ”Ŗ·ūŗÅ”±Ö®¼ä½ØĮ¢ĮŖĻµ£¬ŹĒ»ÆѧѧæĘĢŲÓŠµÄĖ¼Ī¬·½Ź½”£Ä³·“Ó¦µÄĪ¢¹ŪŹ¾ŅāĶ¼ČēĻĀ£¬Ļą¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ
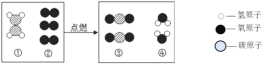
A. “Ė·“Ó¦ŹĒĪļÖŹČ¼Éյķ“Ó¦
B. ·“Ó¦Īļ¢ŁµÄ»ÆѧŹ½ŹĒCH2
C. ²Ī¼Ó·“Ó¦µÄ¢Ł”¢¢ŚĪļÖŹµÄ·Ö×ÓøöŹż±ČĪŖ1:3
D. ·“Ӧɜ³ÉµÄ¢Ū”¢¢ÜĪļÖŹµÄÖŹĮæ±ČĪŖ 22:9
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ÆѧŹµŃ銔×éĶ¬Ń§ŌŚŹµŃéŹŅÓĆ¹żŃõ»ÆĒāČÜŅŗÖĘŃõĘų”£
£Ø1£©ÓĆ¹żŃõ»ÆĒāŗĶ¶žŃõ»ÆĆĢ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ__________________________”£
£Ø2£©Ķ¬Ń§ĆĒ·¢ĻÖ·“Ó¦Ź±ÓŠ°×Īķ²śÉś£¬ÓĆČēĻĀĮ½øö×°ÖĆĄ“ÕŅŌŅņ£¬ĘäÄæµÄŹĒ£ŗ___________”£
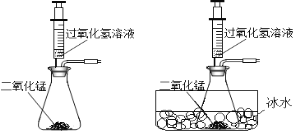
Ķ¬Ź±ÓÖÕ¹æŖĮĖĻĀĮŠĖ¼æ¼ÓėĢ½¾æ£ŗ
£Ø3£©“߻ƼĮMnO2µÄÓĆĮæ¶Ō·“Ó¦ĖŁĀŹŹĒ·ńÓŠÓ°ĻģÄŲ£æ
ĖūĆĒ×öĮĖÕāŃłŅ»×鏵Ńé£ŗĆæ“Ī¾łÓĆ30mL10%µÄH2O2ČÜŅŗ£¬²ÉÓĆ²»Ķ¬ÖŹĮæMnO2·ŪÄ©×ö“߻ƼĮ£¬²ā¶Øø÷“ĪŹÕ¼Æµ½500mLŃõĘųĖłÓƵď±¼ä£¬½į¹ūČēĻĀ£ŗ£ØĘäĖüŹµŃéĢõ¼ž¾łĻąĶ¬£©
ŹµŃé“ĪŠņ | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
MnO2·ŪÄ©ÓĆĮæ£ØæĖ£© | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
ĖłÓĆŹ±¼ä£ØĆė£© | 17 | 8 | 6 | 3 | 2 | 2 | 2 | 2 | 2 | 2 |
Ēėøł¾Ż±ķÖŠŹż¾Ż»Ų“š£¬MnO2·ŪÄ©µÄÓĆĮæ¶Ō·“Ó¦ĖŁĀŹµÄÓ°ĻģŹĒ___________”£
£Ø4£©H2O2ČÜŅŗµÄČÜÖŹÖŹĮæ·ÖŹż¶Ō·“Ó¦ĖŁĀŹŹĒ·ńÓŠÓ°ĻģÄŲ£æŠ”×éĶ¬Ń§ÓÖ×öĮĖŅ»×鏵Ńé£ŗ
Ćæ“Ī¾łČ”5mL30%µÄH2O2ČÜŅŗ£¬Č»ŗóĻ”ŹĶ³É²»Ķ¬ČÜÖŹÖŹĮæ·ÖŹżµÄČÜŅŗ½ųŠŠŹµŃ锣¼ĒĀ¼Źż¾ŻČēĻĀ£ŗ£ØŹµŃé¾łŌŚ20”ęŹŅĪĀĻĀ½ųŠŠ£¬ĘäĖüŹµŃéĢõ¼ž¾łĻąĶ¬£©
ŹµŃé“ĪŠņ | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
H2O2ČÜŅŗČÜÖŹÖŹĮæ·ÖŹż | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
MnO2·ŪÄ©ÓĆĮæ£ØæĖ£© | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
ŹÕ¼Æµ½540mLĘųĢåŹ±ĖłÓĆŹ±¼ä£ØĆė£© | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
·ÖĪö±ķÖŠŹż¾ŻæÉµĆ³öµÄ½įĀŪŹĒ___________”£
£Ø3£©ŹµŃé·“Ė¼£ŗMnO2æÅĮ£µÄ“󊔶Ō·“Ó¦ĖŁĀŹŹĒ·ńÓŠÓ°Ļģ£æĒėÉč¼ĘŹµŃéÖ¤Ć÷£ØÓļŃŌŠšŹö£¬²»ÓĆ»×°ÖĆĶ¼£©___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒā»ÆøĘ£ØCaH2£©³£ĪĀĻĀÄÜÓėĖ®·“Ӧɜ³ÉH2ŗĶŅ»ÖÖ¼ī£¬ŹĒŅ°Ķā¹¤×÷ČĖŌ±±ćŠÆČ¼ĮĻµÄĄ“Ō“”£ĻÖĄūÓĆŠæĮ£ŗĶŃĪĖįÖʱøH2Óė½šŹōøĘ·“Ó¦ÖĘČ”CaH2£ØČēĶ¼£¬×°ÖĆ×ó²ąĮ¬ĘųĢå·¢Éś×°ÖĆ£©”£ŌņĻ“ĘųĘæÖŠm”¢nӦєĻĀĮŠŹŌ¼ĮµÄ_____”¢_____£ØĢīŠņŗÅ£©”£
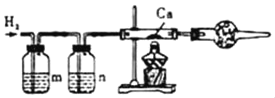
I£®NaHCO3ČÜŅŗ ¢ņ£®NaOHČÜŅŗ ¢ó£®ÅØĮņĖį”£
ĪŖ·ĄÖ¹øʱ»Ńõ»Æ£¬ŌŚµćČ¼Ö®Ē°±ŲŠė½ųŠŠµÄ²Ł×÷ŹĒ_____”£CaH2ÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____£¬ĪŖ·ĄÖ¹æÕĘųÖŠµÄO2”¢CO2”¢Ė®ÕōĘųÓėCa»ņCaH2·“Ó¦£¬±ŲŠėŌŚµ¼¹ÜÄ©¶ĖĮ¬½ÓµÄøÉŌļ¹Ü×°ÖĆÖŠĢķ¼ÓµÄŅ©Ę·ŹĒ_____£ØĢīŠņŗÅ£©
A NaOHŗĶCaOµÄ»ģŗĻĪļ B ÅØĮņĖį C Ģś·Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒÄĘŌŖĖŲŗĶĀČŌŖĖŲŌŚŌŖĖŲÖÜĘŚĻŽ±ķÖŠµÄŠÅĻ¢ŗĶ3ÖÖĮ£×ӵĽį¹¹Ź¾ŅāĶ¼”£Ēė»Ų“šø“ĻĀĮŠĪŹĢā£ŗ
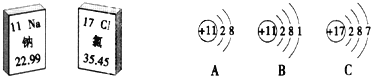
(1)ĀČŌ×ÓµÄŗĖµēŗÉŹżŹĒ_____”£CĮ£×Ó¶ŌÓ¦ŌŖĖŲ×é³Éµ„ÖŹµÄ»ÆѧŹ½ŹĒ____
(2)ÄĘŗĶĀČĘųÉś³ÉĀČ»ÆÄʵķ“Ó¦ÖŠ£¬µĆµ½µē×ӵďĒ____Ō×Ó(Ģī×ÖÄø)£¬AĮ£×Ó»ÆѧŹ½ŹĒ___
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫Ņ»øłĢś°ō·ÅŌŚĮņĖįĶČÜŅŗÖŠŅ»¶ĪŹ±¼ä”£·“Ó¦Ē°ŗóČÜŅŗÖŠ“ęŌŚµÄĄė×ÓÖÖĄąČēĶ¼ĖłŹ¾”£ĘäÖŠ”°![]() ”±”°
”±”°![]() ”±”°
”±”°![]() ”±±ķŹ¾²»Ķ¬Ąė×Ó”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
”±±ķŹ¾²»Ķ¬Ąė×Ó”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
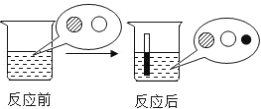
A. ”°![]() ”±±ķŹ¾ĢśĄė×ÓB. ”°
”±±ķŹ¾ĢśĄė×ÓB. ”°![]() ”±±ķŹ¾ĶĄė×Ó
”±±ķŹ¾ĶĄė×Ó
C. ·“Ó¦ŗóČÜŅŗÖŹĮæ¼õŠ”D. ·“Ó¦ŗóĢś°ōÖŹĮæ¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓ¦ÓĆ£¬Ļą¹Ų»Æѧ·½³ĢŹ½¼°»ł±¾·“Ó¦ĄąŠĶ¶¼ÕżČ·µÄŹĒ£Ø””””£©
A. Ņ»Ńõ»ÆĢ¼ÓĆÓŚĮ¶Ģś£ŗ4CO+Fe3O4![]() 3Fe+4CO2 ÖĆ»»·“Ó¦
3Fe+4CO2 ÖĆ»»·“Ó¦
B. ÓĆĒāŃõ»ÆøĘČÜŅŗĪüŹÕ¶žŃõ»ÆĢ¼ĘųĢå£ŗCa£ØOH£©2+CO2£½CaCO3”ż+H2O ø“·Ö½ā·“Ó¦
C. ÓĆŗ¬ÓŠĒāŃõ»ÆĀĮµÄŅ©ĪļÖĪĮĘĪøĖį¹ż¶ąÖ¢£ŗAl£ØOH£©3+3HCl£½AlCl3+3H2O ø“·Ö½ā·“Ó¦
D. ŹµŃéŹŅ¼ÓČČøßĆĢĖį¼ŲÖĘČ”ŃõĘų£ŗK2MnO4![]() 2KMnO4+MnO2+O2”ü ·Ö½ā·“Ó¦
2KMnO4+MnO2+O2”ü ·Ö½ā·“Ó¦
²éæ““š°øŗĶ½āĪö>>
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com