
【题目】在“宏观——微观——符号”之间建立联系,是化学学科特有的思维方式。某反应的微观示意图如下,相关说法不正确的是
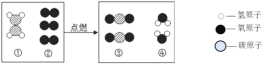
A. 此反应是物质燃烧的反应
B. 反应物①的化学式是CH2
C. 参加反应的①、②物质的分子个数比为1:3
D. 反应生成的③、④物质的质量比为 22:9
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】农业上常用质量分数为16%的NaCl溶液选种。实验室配制100 g该浓度溶液的过程如下图所示。下列说法不正确的是

A. 实验操作顺序为④②①⑤③B. ②中需称量NaCl的质量为16 g
C. 选用100 mL量筒量取所需水的体积D. ①中有部分固体洒落所得溶液的浓度偏大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】《千里江山图》是北宋王希孟创作的绢本设色画,其颜料选用各色天然矿石,描绘了祖国的锦绣河山。一些矿石的主要成分及颜色如下表。

矿石 | 蓝铜矿 | 孔雀石 | 雌黄 | 赭石 |
主要成分 | Cu3(OH)2(CO3)2 | Cu(OH)CO | As2S3 | Fe2O3 |
颜色 | 蓝色 | 绿色 | 黄色 | 红色 |
(1)四种矿石主要成分中,属于氧化物的是______。
(2)蓝铜矿和孔雀石的主要成分在组成上具有的相同点是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)维生素C(C6H8O6)能溶于水,在人体内不能合成,须从食物中摄取,它主要存在于_____类食物中,能增强人体的抗病能力,人体缺乏维生素C会引起_____病.
(2)现取3粒维生素C压碎后溶于10mL水中,然后过滤.取少量滤液,向其中滴加几滴紫色石蕊试液,试液变红色,说明维生素C的水溶液呈_____性; 维生素C在酸性环境中比较稳定,高温时易被破坏.如何食用黄瓜才能充分利用黄瓜中丰富的维生素C?_____.
(3)小芳为测定维生素C药片中维生素C的质量分数,进行如下实验:
反应原理:C6H8O6+I2=C6H6O6+2HI(I2不和Vc药片中的其他成分反应)
实验数据:取维生素C药片2g,共消耗I2的质量为2.54g.
请你帮助小芳计算该Vc药片中维生素C的质量分数._____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了研究物质的溶解现象,进行如下探究活动。
探究I:将足量的碳酸钠、氯化钠和硝酸钾三种物质分别溶解在一定量的水中,溶解过程的温度变化如下图所示。
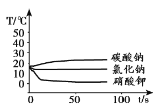
探究II:
实验 |
① |
② |
③ |
现象 | 固体溶解, 形成紫红色溶液 | 固体溶解,形成紫红色溶液 | 固体几乎不溶解 |
探究III: 探究过程如下图所示:
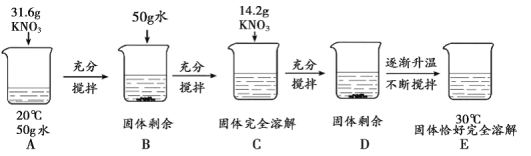
回答下列问题:
(1)探究I中,溶解过程放出热量的物质是__________。
(2)对探究II中实验现象进行分析,需要做的对比是________。分析得出的结论之一是__________。
(3)探究III中,所得溶液一定属于饱和溶液的是__________。通过该探究得出的结论是__________(答一点即可)。
(4)在上述探究的基础上,同学们想通过探究,比较食盐和氯化铵在水中的溶解度大小,探究方案应该是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组用下图装置进行两个实验。已知:白磷的着火点是40℃。
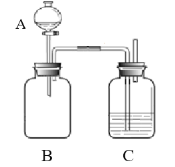
(1)实验一:证明可燃物燃烧条件。A中放有过氧化氢溶液,B中放有一定量二氧化锰;C中放有约半瓶80℃热水,C中左侧长导管出气口处放一块白磷。打开分液漏斗活塞后观察到C中白磷燃烧。该实验证明可燃物燃烧的条件之一是______。该实验C中水的作用是_________。
(2)实验二:证明二氧化碳与氢氧化钠发生化学反应。B中充满二氧化碳,C中液体是足量稀盐酸,打开分液漏斗的活塞,将A中氢氧化钠溶液加入到广口瓶中,关闭活塞,实验过程中可观察到明显的实验现象,产生该现象的原因是________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
产品原理:该厂采用“侯氏制碱法”生产化工产品﹣﹣纯碱(Na2CO3)和化肥NH4Cl.
生产原理是:将NH3和CO2通入饱和食盐水中得到NaHCO3晶体和NH4Cl溶液,反应的化学方程式为:_____;后分离出NaHCO3,加热制得纯碱.
生产流程:
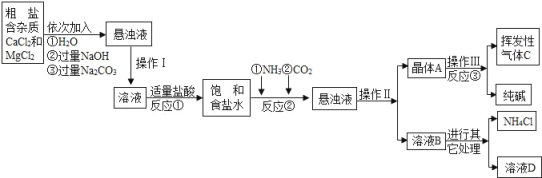
相关资料:
(1)NH4Cl ![]() NH3↑+HCl↑
NH3↑+HCl↑
(2)已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解的气体体积)
物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
问题讨论:
(1)操作Ⅰ、Ⅱ中,相同操作的名称为_____.反应①中发生了两个反应,写出其中一个化学方程式:_____,反应①加适量的盐酸,适量是指_____.
(2)检验挥发性气体C的方法_____.
(3)上述生产流程中可循环使用的是_____(填序号).
A挥发性气体C; B溶液D; C氢氧化镁;D化肥NH4Cl
组成确定:
(1)称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.由上述实验可确定纯碱样品含有杂质_____(写化学式).
含量测定:
实验一 | 实验二 | 实验三 | 实验四 | |
固体混合物溶液质量 | 100g | 100g | 100g | 100g |
加入CaCl2溶液质量 | 10g | 20g | 30g | 40g |
生成的沉淀的质量 | 4g | m | 10g | 10g |
称取该纯碱样品44g固体混合物,加水配成400g溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见表:
请分析表中数据回答并计算:
(1)m=_____g;
(2)在实验三中,完全反应后所得溶液中溶质氯化钠的质量分数是多少?_____(要求写计算过程,结果保留0.1%)
总结反思:
请通过计算并结合下表判断此纯碱样品等级为_____品,在上述纯碱含量测定中,将CaCl2溶液改为BaCl2溶液,测定误差会减小.
工业纯碱标准:(Na2CO3% ) | |||
优等品 | 一等品 | 合格品 | 次品 |
≥95 | ≥80 | ≥75 | ≤40 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国大部分地区深受酸雨危害,煤燃烧产生的SO2是形成酸雨的主要污染物,SO2与水结合生成弱酸性亚硫酸(H2SO3)。
已知:H2SO3易分解生成水和SO2,也易与空气中的氧气或稀硝酸反应生成H2SO4;H2SO3和SO2都能使红色的品红溶液褪色。
(1)酸雨是pH小于______的降雨。
(2)常用脱硫方法减少废气中的SO2,以生石灰(CaO)为脱硫剂,高温下与废气中的SO2与O2化合生成CaSO4,化学方程式为_______
(3)实验室常用亚硫酸盐与HCl或H2SO4反应制备SO2,Na2SO3与盐酸反应的化学方程式______
(4)小鸿同学利用中和反应的原理,在空气中放置一段时间的酸雨(pH约为3)中加入足量的KOH,并就反应后混合溶液的中盐成分进行如何探究:
[提出猜想]反应后的混合溶液中盐的成份是什么?
[进行猜想]猜想1:只有K2SO3
猜想2:__________
猜想3:既有K2SO4,也有K2SO3
[实验探究]限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、澄清石灰水、品红溶液、紫色石蕊溶液
实验操作 | 实验现象 | 结论 | |
1 | 各取2mL反应后的混合溶液分别加入A、B两只试管 | 猜想3成立 | |
2 | 向A试管中滴加足量的稀硫酸,随即滴入几滴红色品红溶液 | _____ | |
3 | 向B试管中,加入_____,再加入足量的_____ | 先有白色沉淀,后有气泡产生,沉淀部分溶解, |
反思与拓展:证明混合溶液中的K2SO4的化学反应方程式为________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答。
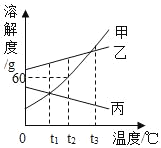
(1)温度为_____℃时,甲、乙、丙三种物质的溶解度大小关系为乙>甲=丙。
(2)若甲中含有少量乙,可用_____的方法提纯甲。
(3)t2℃时,在50g水中加入_____g甲物质,恰好形成饱和溶液。
(4)接近饱和的丙溶液,在保持溶质质量分数不变的情况下转变为饱和溶液,可采取的方法是_____。
(5)将t3℃时,等质量的甲、乙、丙三种物质的饱和溶液,同时降温到t1℃,所得溶液中溶质质量分数由大到小的顺序是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com