
【题目】(9分)某面包膨松剂由碳酸氢钠和碳酸氢铵两种物质组成。化学小组为验证该膨松剂的成分及各成分含量的测定,通过查阅资料,设计如图所示实验。

查阅资料:①膨松剂在面包制作过程中发生的两个化学反应的方程式分别是:
2NaHCO3 △ Na2CO3+H2O+CO2↑
NH4HCO3 △ NH3↑+H2O+CO2↑
②通常状况下,1体积水溶解700体积氨气,氨气溶于水所得溶液为氨水
③二氧化碳溶于水,溶液呈酸性
实验定性验证:
操 作 步 骤 | 实 验 现 象 | 实 验 结 论 |
组装仪器, | ||
装入药品进行加热,打开阀 门 、关闭阀门 。 | 观察到 | 则说明有碳酸氢铵存在 |
然后打开阀门K2、关闭阀门 K1继续加热 | 最终观察到B中试管内没有气泡冒出,且____________ 。 | 则说明有碳酸氢钠存在 |
实验分析及反思:(1) 同学甲认为应将装置B中水换成澄清石灰水,才能判断样品的成分。
同学乙认为没有必要,他的理由是 。
(2) 请你分析装置C中碱石灰的作用是 。
实验数据分析及成分含量计算:
小组同学利用电子天平共同作了以下测定实验,实验数据记录如下:
称量项目 | 称量 时间 | 质量(g) |
装置A中试管质量 | 反应前 | 50.00 |
装置A中试管+样品质量 | 反应前 | 70.00 |
装置A中试管+固体质量 | 反应后 | 60.60 |
请你分析表中实验数据并计算该膨松剂中碳酸氢铵的质量分数。(写出计算的详尽过程)
解:
【答案】实验定性验证:实验步骤:检验装置的气密性;K1;K2;实验现象:酚酞溶液变红;原药品中仍有固体残留;实验分析及反思:(1)试管中的水只是判断反应是否完全;(2)吸收二氧化碳,避免二氧化碳溶于水形成酸,干扰装置D中可能看不到变红现象,不能判断有氨气生成。实验数据分析及成分含量计算16%
【解析】
试题分析:实验定性验证:组装好仪器,先检查装置的气密性,如果导管口产生气泡,说明装置不漏气;装入药品进行加热,打开阀门K1、关闭阀门K2,如果观察到酚酞试液变红色,说明有碳酸氢铵存在;然后打开阀门K2、关闭阀门K1继续加热,最终观察到B中试管内没有气泡冒出,且原药品中仍有固体残留物,说明有碳酸氢钠存在.故填:检查装置的气密性;导管口有气泡冒出;K1;K2;酚酞试液变红;原药品中仍有固体残留物.实验分析及反思:(1)同学甲认为应将装置B中水换成澄清石灰水,才能判断样品的成分.同学乙认为没有必要,他的理由是试管中的水只是判断反应是否完全.故填:试管中的水只是判断反应是否完全.(2)装置C中碱石灰的作用是吸收二氧化碳,避免干扰对碳酸氢铵的检验.
解:设碳酸氢钠的质量为x,
碳酸氢钠受热分解生成碳酸钠的质量为:60.60g-50.00g=10.60g,
样品质量为:70.00g-50.00g=20.00g,
2NaHCO3△ Na2CO3+H2O+CO2↑,
106
x10.60g
168:106=x:10.60g
x=16.8g,
该膨松剂中碳酸氢铵的质量分数为:20.00g-16.8g/20.00g×100%=16%,
答:该膨松剂中碳酸氢铵的质量分数为16%.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:
【题目】(.4分)、下图是三种固体物质的溶解度曲线。
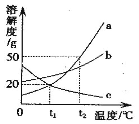
(1)物质c的溶解度随温度的升高而 ;
(2)将t1℃时a、b、c三种物质的饱和溶液升温至t2℃(溶剂量不变),溶液中溶质质量分数不变的是 。
(3) 将t2℃时a、b、c三种物质的饱和溶液降温至t1℃,析出晶体最多的是 ;
(4)若b为氯化钠,那么从它的饱和溶液中获得较多的氯化钠晶体,应采取 方法。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质的用途主要由物理性质决定的是( )
A.镁粉用于制作照明弹 B.钨用于制作白炽灯丝
C.生石灰做食品干燥剂 D.氮气用作焊接金属时的保护气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)石灰石有许多重要的用途。
(1)以石灰石为原料,可以生产生石灰,生石灰可做干燥剂,某化学兴趣小组的同学对食品厂某批次包装完整、粉状的生石灰成分进行质量检测。
【提出问题】该批次的生石灰成分及含量是否与标签相符?
(标签如图所示)

【猜想与假设】固体成分为:
A:全部是碳酸钙和杂质 B:既有碳酸钙,也有氧化钙和杂质
C:全部是 和杂质。
【设计并完成实验】
实验操作 | 实验现象 | 实验结论 |
第一步操作:取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有 |
第二步操作:再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有 |
【实验结论】该兴趣小组同学得出的结论:剩余固体成分与【猜想与
假设】中的 (填A、B或C)相同。
【定量测定】称取10克该批次的生石灰样品,置于锥形瓶中,向其中缓慢加稀盐酸,直至无气泡产生,电子天平读数变小0.88克,将锥形瓶中残留物进行过滤、洗涤、干燥,得到固体质量为0.2克。

【问题讨论】由于生石灰与酸反应放出热量,导致水蒸气随CO2一起从导管口逸出,这一因素使测得的生石灰的最终含量将 (选填“偏小”“偏大”或“无影响”)。反应生成的CO2也会代替原有的空气残留在锥形瓶中,这一因素对测定结果也有影响。
(2)实验小组的同学对实验室制取二氧化碳反应后的溶液进行了如下探究:
取大理石和盐酸反应且过滤后所得废液20克于烧杯中,逐滴滴入碳酸钠溶液至过量,滴入碳酸钠溶液的质量与生成沉淀的质量的变化关系如图所示。请根据图中信息计算废液中氯化钙的质量分数是多少?(写出计算过程)
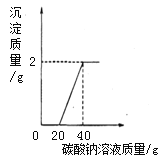
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组设计了测定纯碱(Na2CO3)样品(只含NaCl杂质)中Na2CO3质量分数的实验方案.请回答下列问题:
小资料:碱石灰的主要成分是氢氧化钠和氧化钙的混合物
(1)气体法。
【原理思路】利用Na2CO3与稀硫酸反应产生CO2,通过测量丙装置实验前后的质量得出CO2质量,从而计算碳酸钠的质量分数。(不考虑原装置内空气的影响)
【实验分析】小科同学根据以上思路,设计了如下图的实验装置。
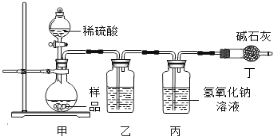
①实验装置乙中盛放的试剂为 。
装置丁中碱石灰的作用是 。(填字母)
A.吸收Na2CO3与稀硫酸反应产生CO2
B.防止外界空气中二氧化碳进入丙中
C.干燥二氧化碳
②实验中如果滴加稀硫酸的速度过快,会导致测得样品中碳酸钠的
质量分数 (填写“偏高”“偏低”或“不变”).
③小明同学认为小科的方案存在问题,即使操作规范下也会造成结果偏低,你认为他的理由是 ,应该将装置甲中双孔橡胶塞换成三孔橡胶塞,并增加下图装置,实验结束后缓缓通入一段时间空气,目的是 ,其中NaOH溶液的作用是 。
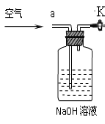
(2)沉淀法.
【实验原理】利用碳酸根离子与钙离子结合生成沉淀,通过沉淀的质量而得出碳酸钠的质量分数。
【实验步骤】①用托盘天平称取样品11.0g放入烧杯中,加水使其完全溶解;
②加入过量的CaCl2溶液充分反应。证明CaCl2过量(即Na2CO3已完全反应)的方法是: 静置,向上层清液中滴加 溶液,如果没有白色沉100%=96.4%淀生成,证明CaCl2过量;
③过滤、操作X、干燥、称量沉淀的质量为10.0g,操作X的名称是 ,如果缺少此操作会造成碳酸钠质量分数 (填写“偏高”“偏低”或“不变”)。
④通过以上提供的数据计算出样品中碳酸钠的质量分数为 。(写出计算过程,结果保留至0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向含有和Cu(N03)2和AgNO3的混合溶液中加入一定量的铁粉,并绘制参加反应的铁与溶液中溶质种类的关系图(如图)。下列说法正确的是
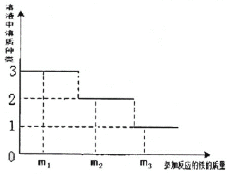
A.当参加反应的铁的质量为m1时,溶质的种类、析出的金属单质种类均为3种
B.当参加反应的铁的质量为m2时,加入盐酸,有白色沉淀生成
C.当参加反应的铁的质量为m3时,溶质为Fe(N03)2
D.当参加反应的铁的质量为m2时,加入稀盐酸,有气泡产生
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(12分)油条是人们喜欢的早点,中国油条的传统加工配方是用明矾(KAl(SO4)2)作为膨松剂,明矾常引起铝残留影响人体健康问题,现在的膨松剂常用臭粉(碳酸氢铵)、小苏打。
(1)油条中的主要营养素是油脂和
(2)“铝残留影响人体健康”中的铝是指 (选填“原子”或“元素”或“单质”)
(3)已知某膨松剂含碳酸氢铵、碳酸氢钠中的一种或两种,兴趣小组对该膨松剂进行如下探究:
【查阅资料】① 2NaHCO3![]() Na2CO3+H2O+CO2↑; NH4HCO3
Na2CO3+H2O+CO2↑; NH4HCO3 ![]() NH3↑+H2O+CO2↑。
NH3↑+H2O+CO2↑。
②氨气能使湿润的红色石蕊试纸变蓝。浓硫酸可用于吸收氨气。
③ 碱石灰是固体氢氧化钠和氧化钙的混合物,能作干燥剂,和二氧化碳反应,不与氨气反应。
实验I:探究膨松剂的成分
按下图所示连接好装置。
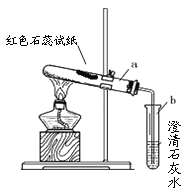
实验记录
实验操作 | 主要实验现象 | 实验结论 及解释 | |
① | 检查装置的气密性 | 装置的气密性良好 | |
② | 点燃酒精灯。 | 试管中白色固体减少,红色石蕊试纸 ,澄清石灰水变浑浊。 | 有二氧化碳和氨气生成 |
③ | 继续充分 加热 | 试管中仍有固体。 | |
得出结论:该膨松剂的成分为 (写出化学式)。
实验II:探究产生气体的量
①测定二氧化碳的质量:如下图所示装置(气密性良好,各装置中的试剂为足量)。
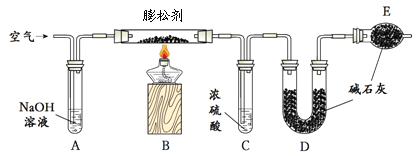
将8g膨松剂装入装置B中,加热前,先对已连接好的装置A、B和C通一段时间的空气,再连接装置D、E;加热过程中,装置C的作用是 ;停止加热后,继续通入一段时间的空气,目的是 。实验中,测定实验前后装置 (填字母序号)的质量,其质量差即为样品产生的二氧化碳气体的质量。若没有装置A,可能会造成测定结果 (填“偏大”、“不变”或“偏小”)。
②测定氨气的质量:将上图装置中 (填字母序号) 的连接顺序为对调。另取8g膨松剂装入装置B中,通过测定实验前后盛有浓硫酸的试管质量,其质量差即为样品产生的氨气的质量。若该装置的质量增加了1.36g,则同时共产生二氧化碳质量是多少? (有计算过程,结果精确到0.01)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分) 小明将14.4g含杂质的纯碱样品(碳酸钠与氯化钠的混合物)与90g稀盐酸相混合,恰好完全反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示:
反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 | t 7 |
气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | X | 4.4 |
表中X的值为 ;
计算样品中NaCl的质量;
计算完全反应后所得溶液中溶质的质量分数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com