

分析 (1)根据水库中水的组成分析其类别;
(2)①分离出液体和不溶物的操作方法为过滤;
②根据化合价原则、质量守恒定律分析回答;
③需要利用pH计测定溶液的酸碱度;
(3)根据氯离子的检验方法及水垢的成分分析回答;
(4)根据蒸馏的原理及注意的事项分析;
(5)对临时水源的水进行处理的方法为:先需要自然沉降、过滤,然后对过滤后的水进行消毒,最后加热煮沸后才能饮用.
解答 解:(1)由于水库中的水处于敞开的环境中,混入了一些物质,所以水库中的水属于混合物,
故答案为:混合物;
(2)①)A池中通过过滤除去水中的固体杂质,
故答案为:过滤;
②在二氧化氯(ClO2)中,由氧-2价,则氯的化合价是+4价;在Cl2+2NaClO2═2ClO2+2X方程式中左边有:氯原子、钠原子、氧原子的数目分别是4、2、2,在右边有氯原子、氧原子的数目分别是2、2、由质量守恒定律反应前后原子的种类及数目不变可知,X的化学式是NaCl,
故答案为:+4;NaCl;
③为了准确测定家用自来水的酸碱度,应用pH计来进行检测,
故答案为:pH计;
(3)自来水中通常都含有Cl-,可以在水样中滴加少量稀硝酸和硝酸银检验,若出现白色沉淀现象,说明水中含有Cl-;水中的Ca2+,Mg2+受热后转化为沉淀,即通常所说的水垢,水垢的主要成分为碳酸钙和氢氧化镁,
故答案为:硝酸银;白色沉淀;碳酸钙和氢氧化镁;
(4)可以利用沸点不同通过蒸馏的方法把自来水进一步净化为蒸馏水;蒸馏操作中通常加入碎瓷片或沸石,其目的是防止暴沸,
故答案为:蒸馏;防止暴沸;
(5)A.加热煮沸,通过加热除去水残留的消毒剂并降低水的硬度;B.消毒,加入消毒剂,杀灭水的病毒过;C.过滤,把水中不溶性固体杂质从水中除去;D.自然沉降,通过静置的方法使水中固体杂质沉至水底部,综上所述对临时水源的水进行处理的合理顺序是D、C、B、A,
故答案为:DCBA.
答案:
(1)混合物;
(2)①过滤;②+4;NaCl;③pH计;
(3)硝酸银;白色沉淀;碳酸钙和氢氧化镁;
(4)蒸馏;防止暴沸;
(5)DCBA
点评 本题考查了三废处理及环境保护、水的净化原理,题目难度中等,明确氧化还原反应原理、水的净化原理为解答关键,试题知识点较多、综合性较强,充分考查学生的分析能力及化学实验能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 溶解度是指在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的溶质的质量.
溶解度是指在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的溶质的质量.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 镁原子的核电荷数为12 | |
| B. | 镁原子的相对原子质量为24.31g | |
| C. | 镁属于非金属元素 | |
| D. | 在化学反应中,镁原子容易得到电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
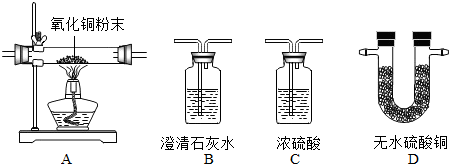
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 纯净物一定是化合物 | |
| B. | 混合物中元素不一定都是化合态 | |
| C. | 某物质不是化合物就是单质 | |
| D. | 某物质中只含有一种元素,它一定是纯净物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验操作 | 实验现象 | 结论 |
| 将澄清的石灰水分别滴入盛有教室内的空气和操场上的空气的集气瓶中 | 教室内的空气瓶中石灰水变浑浊;操场上的空气瓶中石灰水无明显变化. | 教室内的空气中二氧化碳含量比操场上的空气中高. |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁. | 试管外壁发热 | 原因是氢氧化钠溶于水放热 |
| ②向①所得的溶液中逐滴加入过量稀硝酸 | 一开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体. | 样品中含有的 杂质是碳酸钠. |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有的杂 质是氯化钠 |
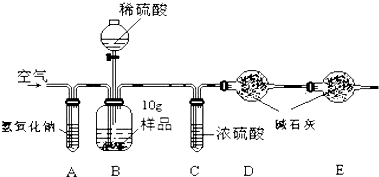
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com