
分析 根据实验室制取二氧化碳的反应原理、工业制取二氧化碳的反应原理(煅烧石灰石),检验二氧化碳使用澄清的石灰水,进行分析解答.
解答 解:实验室常用石灰石与稀盐酸反应制取二氧化碳,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.
检验二氧化碳常用澄清的石灰水,将气体通入澄清的石灰水中,观察是否变浑浊,若澄清的石灰水变浑浊,说明是二氧化碳;二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
工业制取二氧化碳,常用的煅烧石灰石的方法,碳酸钙高温分解生成氧化钙和二氧化碳,反应的化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;将气体通入澄清的石灰水中;澄清的石灰水变浑浊;CO2+Ca(OH)2═CaCO3↓+H2O;CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
点评 本题难度不大,掌握实验室制取二氧化碳的反应原理、工业制取二氧化碳的反应原理、二氧化碳的检验方法是正确解答本题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
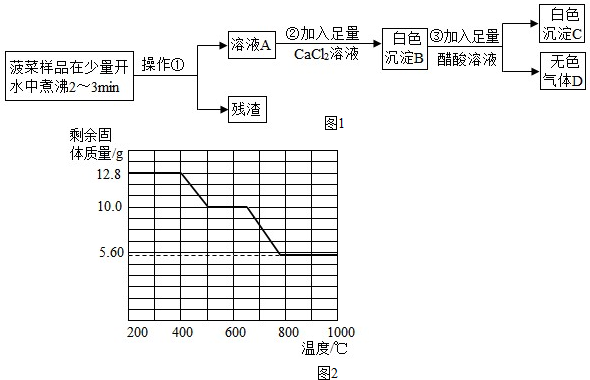
| 实验操作 | 实验现象 | 实验结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
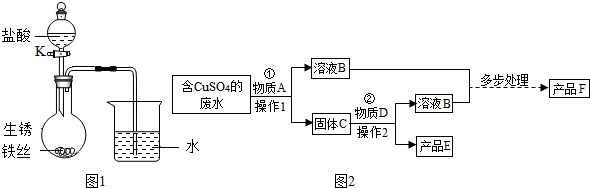
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
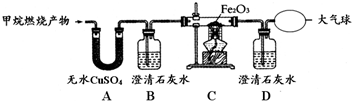
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com