
学完酸碱盐知识后,小美对妈妈焙制糕点用的小苏打很感兴趣,她把小苏打带到实验室与小刚一起进行探究。
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显 性;
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有 产生,说明小苏打能与酸反应。在医疗上可以用小苏打治疗 ;
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了CO2气体呢?于是她用下图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成。
当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①NaOH;②Na2CO3;③NaCl。小刚认为猜想
一定不正确,理由是 。小刚从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,他判断该固体为NaOH,小美认为他的实验设计不合理,因为
(4)小美和小刚继续探究固体成分,设计了如下实验:
| 操作步骤 | 实验现象 | 结论 |
| 取少量白色固体于试管中,加水溶解,向其中滴加 溶液 | 产生白色沉淀 | 试管内剩余的固体为Na2CO3 |
碱性;气泡,胃酸过多;③,碳酸氢钠中不含氯元素;碳酸钠溶液也呈碱性;氯化钙溶液;
NaHCO3="==" Na2CO3+H2O+CO2↑;低温保存。
解析试题分析:(1)碱性溶液能使酚酞变成红色;
(2)小苏打是碳酸氢钠,能与盐酸反应生成二氧化碳气体,医疗上常用于治疗胃酸过多;
(3)根据质量守恒定律化学反应前后元素的种类不变,由于碳酸氢钠中不含氯元素,故不可能生成氯化钠;由于碳酸钠溶液也呈碱性,也能使无数酚酞变红,故不能通过加指示剂来确定;
(4)根据结论,试管内剩余的固体为Na2CO3,碳酸钠能与氯化钙反应生成碳酸钙白色沉淀;由实验探究可知碳酸氢钠分解生成了二氧化碳和碳酸钠,利用质量守恒定律,另一张生成物是水;碳酸氢钠高温易分解,故要在低温干燥处保存。
考点:碳酸氢钠的性质


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:探究题
(8分)石灰石有许多重要的用途。
(1)以石灰石为原料,可以生产生石灰,生石灰可做干燥剂,某化学兴趣小组的同学对食品厂某批次包装完整、粉状的生石灰成分进行质量检测。
【提出问题】该批次的生石灰成分及含量是否与标签相符?
(标签如图所示)
【猜想与假设】固体成分为:
A:全部是碳酸钙和杂质 B:既有碳酸钙,也有氧化钙和杂质
C:全部是 和杂质。
【设计并完成实验】
| 实验操作 | 实验现象 | 实验结论 |
| 第一步操作:取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有 |
| 第二步操作:再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有 |


查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(10分)实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物,极易与空气中水蒸汽和CO2反应而变质。某同学对一瓶久置的“碱石灰”作了如下探究:
(1)猜想:
猜想Ⅰ:没有变质,“碱石灰”只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和Na2CO3。
则CaO与水反应的反应方程式为 。
(2)实验:如图所示:
(3)判断:
a. 若Ca(OH)2、CaCO3和Na2CO3投入到水中不会放热,则由操作②现象判断:猜想Ⅱ
(填:成立、不成立)
b. 操作④发生化学反应的方程式为 ;由操作⑤⑥的现象判断:滤液中含有
(写化学式);由此判断猜想Ⅰ (填:成立、不成立)。
c. 综合a和b的结论,判断该样品变质情况为 。
(4)拓展:由上述实验说明,实验室中“碱石灰”应 保存;操作③中玻棒的作用是 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(7分)资料表明:在不同温度下,CO可将Fe2O3还原为Fe、Fe3O4中的一种或两种。为探究温度对该反应产物的影响,进行如下实验。
【查阅资料】
Ⅰ.Fe3O4与盐酸反应,得到FeCl2和FeCl3的混合溶液
Ⅱ.用溶质质量分数一定的FeCl2和FeCl3溶液进行如下实验,为方案设计提供参考
| | FeCl2溶液 | FeCl3溶液 |
| 加入Fe | 无明显变化 | 溶液变成浅绿色 |
| 加试剂A | 无明显变化 | 溶液变成红色 |
| 实验操作 | 实验现象 | 结论与解释 |
| ①取少量的黑色固体于试管中,滴加适量的______ ②向步骤①所得的溶液中,滴加试剂A | 甲组: 固体溶解,无气泡冒出 加试剂A后,溶液变成红色 | 黑色固体的成分是______ 甲组用CO还原Fe2O3反应的化学方程式是______ |
| 乙组: 固体溶解, 加试剂A后,溶液颜色无明显变化 | 黑色固体的成分是Fe |
 (2)有人认为乙组的实验结论有欠缺,你是否认同此观点,其理由是 。
(2)有人认为乙组的实验结论有欠缺,你是否认同此观点,其理由是 。查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(6分)依据表中的元素所组成初中化学常见的物质,回答下列问题。
| 元素名称 | 氢 | 碳 | 氧 | 氯 | 钠 | 钙 |
| 元素符号 | H | C | O | Cl | Na | Ca |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(8分)“海水晒盐”所获得的粗盐中,除含有泥沙等难溶性杂质外,还含有氯化镁、氯化钙等可溶性杂质,某化学小组为得到较纯净的食盐,进行了下列实验探究活动,请参与他们的探究活动。
[提出问题]如何获得较纯的食盐晶体?
[查阅资料]
20℃时,部分物质的溶解性
情况如下表所示:
| | OH- | CO32- |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |

查看答案和解析>>
科目:初中化学 来源: 题型:探究题
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小强和小华同学很感兴趣,决定对其成分进行探究:
提出问题:这瓶试剂可能是什么溶液呢?
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是
A.酸 B.碱 C.盐
查阅资料:Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ.Na2CO3和NaHCO3溶液都呈碱性。
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 | 产生大量的气泡 | 该溶液是 |

查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动。以下是教学片段,请你参与学习并帮助填写空格(包括表中空格)。
【演示实验】将一定量的稀硫酸加入到盛有NaOH溶液的小烧杯中。
【学生板演】该反应的化学方程式______________。
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想。甲组同学的猜想如下:
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的猜想是
____________________。
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有____________。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究。
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:信息分析题
(4分)A-G和X都是初中化学中的常见物质,其中A、C、E是无色气体,B是红棕色固体,X为蓝色溶液,它们的转化关系如下图所示(部分反应物、生成物已省略):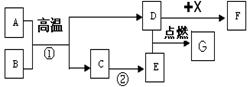
(1)G的化学式是 ;
(2)写出反应①的化学方程 ;
(3)写出在自然界普遍存在反应②,其名称为
(4)D与X充分反应后过滤后得滤渣F,在滤渣F中加入稀盐酸,有气泡产生,则滤渣的成分是 ____ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com