
【题目】实验室常用下列装置来制取氧气:

(1)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是______(填序号),其中二氧化锰起___________作用。
(2)用氯酸钾制取氧气时,发生反应的文字表达式为_______________________________.当O2收集满并取出集气瓶后停止该实验的正确操作步骤是先 ___________,再_________.(3)用E装置收集氧气的依据是________________________,检验氧气是否集满的方法是_________
【答案】 B 催化 氯酸钾![]() 氯化钾+氧气 撤导气管 撤酒精灯 氧气密度比空气大 将带火星的木条放在集气瓶口,若木条复燃,则证明氧气已经收集满
氯化钾+氧气 撤导气管 撤酒精灯 氧气密度比空气大 将带火星的木条放在集气瓶口,若木条复燃,则证明氧气已经收集满
【解析】(1)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是固液常温型B,其中二氧化锰起催化作用,可以加快过氧化氢的分解速率;(2)用氯酸钾制取氧气时,氯酸钾在二氧化锰和加热条件下生成氯化钾和氧气,发生反应的文字表达式为:氯酸钾![]() 氯化钾+氧气,当O2收集满并取出集气瓶后停止该实验的正确操作步骤是先 将导管移出水面,再移走酒精灯,防止水倒流入试管内,使试管炸裂;(3)用E装置收集氧气的依据是氧气的密度比空气大,检验氧气是否集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则证明氧气已经收集满。
氯化钾+氧气,当O2收集满并取出集气瓶后停止该实验的正确操作步骤是先 将导管移出水面,再移走酒精灯,防止水倒流入试管内,使试管炸裂;(3)用E装置收集氧气的依据是氧气的密度比空气大,检验氧气是否集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则证明氧气已经收集满。


科目:初中化学 来源: 题型:
【题目】在一密闭容器中加入甲、乙、丙、丁四种物质,在运动条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是

A. 该反应为化合反应
B. 丙可能为该反应的催化剂
C. 该反应中,乙、丁的质量变化之比为7:5
D. 该反应中,甲、乙的质量变化之比为1:4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】点燃10gH2和O2的混合物气体,爆炸后,生成4.5g水,求原混合气体中H2、O2的质量分别为( )
A. H25g O25g B. H26g O24g C. H20.5g O29.5g D. H24g,O26g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】装有50g稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量.有关量的变化情况见图(横坐标表示氢氧化钡溶液的质量,纵坐标表示小烧杯中量的变化).其中肯定不正确的是( )
A. 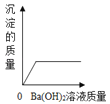 B.
B. 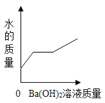
C. 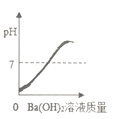 D.
D. 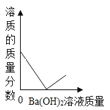
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】石灰石是常见的主要矿石之一,学校研究性学习小组为了测定某矿山石灰石中的碳酸钙的质量分数,取来一些矿石样品,并取来稀盐酸200克,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量(克) | 5 | 10 | 15 | 20 |
生成CO2的质量(克) | 1.76 | 3.52 | 4.4 | m |
﹙1) 哪几次反应中矿石有剩余?
﹙2)上表中m的数值是多少?
﹙3) 试计算这种石灰石中碳酸钙的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从用石灰浆抹的墙壁上掉下一块白色固体,为探究其成分,进行如下实验:

由此得出的结论正确的是 ( )
A. 一定有CaCO3和Ca(OH)2
B. 一定有Ca(OH)2,可能有CaCO3
C. 一定没有CaCO3和Ca(OH)2
D. 一定有CaCO3,可能有Ca(OH)2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】去年2月中旬,某市的内河河面上漂浮大量死鱼。小亮闻讯后,取回水样和同学们一起探究。
(1)观察水质的能见度,然后过滤,过滤时无需用到以下仪器中的_________(填序号)。
A. 漏斗 B. 烧杯 C. 玻璃棒 D. 铁架台 E. 酒精灯
(2)取过滤后的水样。用两种不同类型的物质来检验水样是否显酸性,他们选用的物质可能是_______、___________。请你任选上述两种物质中的一种,设计一个实验进行验证:①________________,②_________,③_____________。

(3)经验测水样呈酸性,是上游某化工厂排放的污水造成的。你认为工厂应在排放污水前,先加入适量__________进行处理。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】维生素C(化学式为C6H8O6)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。近年来科学家还发现维生素C有防癌作用。下列关于维生素C的说法中错误的是( )
A. 维生素C 的相对分子质量为176 B. 维生素C 是由碳元素、氢元素和氧元素组成的
C. 维生素C中,C、H、O三种元素的质量之比为9:1:12 D. 维生素C是一种氧化物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸氢钠(NaHCO3)俗称小苏打,是一种白色固体,是焙制糕点所用的发酵粉的主要成分之一,它能与稀硫酸等酸反应生成CO2。试回答:
(1)写出NaHCO3与稀硫酸反应的化学方程式 。
(2)如何用98%的硫酸(密度为1.84 g/mL)配制980 g 18.4%的硫酸溶液?
(3)现将45g NaHCO3(混有KHCO3)固体粉末加入100mL稀硫酸,恰好完全反应后使气体全部逸出,固体粉末的质量与产生CO2体积的关系如图(该状况下,CO2的密度为2g/L)。
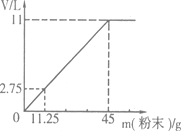
通过计算:
①求100mL稀硫酸中硫酸的质量。
②若稀硫酸为120mL时,加入固体粉末为58.5g,求产生CO2的体积。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com