
【题目】根据以下实验装置图进行气体制取和性质实验的探究:

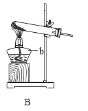
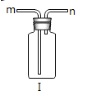
(1)请写出仪器名称a:_______,b:_______
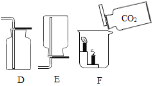
(2)实验室里不使用催化剂制取氧气时,可选用的发生装置是_______(填字母代号,下同);用该装置制取氧气的化学反应方程式为_______; 实验室制取CO2气体时发生的化学反应方程式为_______;连 接A、I、D实验装置,可制取并收集一瓶干燥的CO2气体,I装置中加入的药品是_______,气体通过I时应从_______(填“m”或“n”)端进入,收集CO2一般不使用C装置 的原因是________
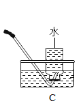
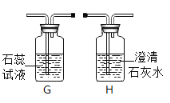
(3)晓丽用图中A、G、H装置组合制备CO2气体并验证相关性质,则装置A应该先连接装 置______(填“G”或“H”),G装置中的现象是_______;如图F所示,向烧杯中慢慢倾倒CO2,发现下层的蜡烛先熄灭,上层蜡烛后熄灭,说明CO2 具有的化学性质是_________(答—点即可)。
(4)若装置A中的反应过于剧烈,从安全角度考虑,可以采取的措施有________(填字母序号)。
a用容积较小的锥形瓶 b减慢液体的滴加速度
c加热反应物 d降低液体反应物的浓度
查阅资料:二氧化硫为无色透明气体,有刺激性气味,有毒,密度比空气大,易溶于水。化学 性质与二氧化碳的相似,都能和碱反应。在实验室里,常用亚硫酸钠与浓硫酸反应制取二氧化硫,反应的化学方程式为![]() .
.
(5)实验室制取二氧化硫最好选择的发生装置是________,收集二氧化硫最好选择的装置是I,进气口应为_______端(填“m”或“n”),因为二氧化硫有毒,多余的二氧化硫常用________溶液来吸收,请写出用该溶液吸收二氧化硫气体的化学反应方程式:_________
【答案】分液漏斗 酒精灯 B 2KMnO4![]() K2MnO4+MnO2+O2↑ CaCO3+2HCl==CaCl2+H2O+CO2↑ 浓硫酸 m 二氧化碳能溶于水且和水反应 G 紫色石蕊试液变红 二氧化碳不可燃、不助燃或密度比空气的大 bd A m NaOH 2NaOH+SO2===Na2SO3+H2O
K2MnO4+MnO2+O2↑ CaCO3+2HCl==CaCl2+H2O+CO2↑ 浓硫酸 m 二氧化碳能溶于水且和水反应 G 紫色石蕊试液变红 二氧化碳不可燃、不助燃或密度比空气的大 bd A m NaOH 2NaOH+SO2===Na2SO3+H2O
【解析】
(1)仪器名称a:分液漏斗,b:酒精灯;
(2)实验室里用高锰酸钾法制氧气不使用催化剂,可选用的发生装置是固-固加热型B;高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰、氧气,化学反应方程式为2KMnO4![]() K2MnO4+MnO2+O2↑; 实验室常用石灰石和稀盐酸反应制取CO2气体,原理是碳酸钙和氯化氢反应生成二氧化碳、氯化钙、水,化学反应方程式为:CaCO3+2HCl==CaCl2+H2O+CO2↑;连接A、I、D实验装置,可制取并收集一瓶干燥的CO2气体,1装置中加入的药品是浓硫酸,利用浓硫酸的吸水性,除掉二氧化碳中水分,气体通过I时应从m端进入,以充分吸收水分,收集CO2 一般不使用C装置 的原因是二氧化碳能溶于水且和水反应;
K2MnO4+MnO2+O2↑; 实验室常用石灰石和稀盐酸反应制取CO2气体,原理是碳酸钙和氯化氢反应生成二氧化碳、氯化钙、水,化学反应方程式为:CaCO3+2HCl==CaCl2+H2O+CO2↑;连接A、I、D实验装置,可制取并收集一瓶干燥的CO2气体,1装置中加入的药品是浓硫酸,利用浓硫酸的吸水性,除掉二氧化碳中水分,气体通过I时应从m端进入,以充分吸收水分,收集CO2 一般不使用C装置 的原因是二氧化碳能溶于水且和水反应;
(3)晓丽用图中A、G、H装置组合制备CO2气体并验证相关性质,则装置A应该先连接装置G,G装置中的现象是紫色石蕊试液变红,如果先连接H,二氧化碳会被氢氧化钙反应,G中没有现象;如图F所示,向烧杯中慢慢倾倒CO2,发现下层的蜡烛先熄灭,上层蜡烛后熄灭,说明CO2 具有的化学性质是二氧化碳不可燃、不助燃、密度比空气的大;
(4)反应物间接触越充分,反应越快。若装置A中的反应过于剧烈,从安全角度考虑,可以采取的措施有减慢液体的滴加速度或降低液体反应物的浓度,以减小反应物的接触程度,而使反应速率减小;
(5)实验室制取二氧化硫最好选择的发生装置是固-液常温型A,收集二氧化硫最好选择的装置是I,二氧化硫密度比空气大,易溶于水进气口应为m端,因为二氧化硫有毒,多余的二氧化硫常用氢氧化钠溶液来吸收,原理是二氧化硫和氢氧化钠反应生成亚硫酸钠和水,化学反应方程式:2NaOH+SO2===Na2SO3+H2O。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:初中化学 来源: 题型:
【题目】(1)下表为部分元素的原子结构示意图:
元素名称 | 氢 | 氦 | 碳 | 氧 | 钠 | 硫 |
元素符号 | H | He | C | O | Na | S |
原子结构 示意图 |
|
|
|
|
|
|
请回答下列问题:
①硫原子的结构示意图的最外层电子数x=_____。
②原子的核外电子排布,特别是最外层的电子数目,与元素的性质有密切的关系。表中具有相对稳定结构的原子是_____(填元素符号)。
③NaH是由离子构成化合物,其形成过程与氯化钠类似。简述NaH的形成过程_____。
④在化学反应中,如果有元素化合价升高,则必定有元素化合价降低。NaH能与水发生化学反应,生成碱和一种气体。甲同学认为生成的气体是O2,乙同学认为生成的气体是H2。从化合价角度分析,你认为哪位同学的说法正确?并说明理由。_____。
(2)汽车尾气催化转换器可将有害气体转化为无害气体排放,其反应过程的微观变化如下图:
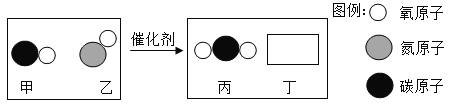
则丁是_____(写化学式),下列说法中正确的有_____。
A 该反应中含氧元素的物质有3种 B 该反应是置换反应
C 参加反应的甲和乙的质量比为14∶15 D 生成丙和丁的分子个数比为1∶1
(3)某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,取一定量该气体按图所示装置进行实验(假设每步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重
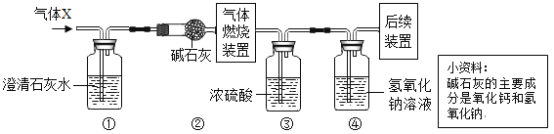
下列关于气体X成分的分析中,正确的有:_____。
A 一定没有二氧化碳 B 可能含有甲烷和氢气
C 可能只有甲烷 D 可能含有氢气和一氧化碳
查看答案和解析>>
科目:初中化学 来源: 题型:
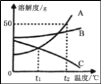
【题目】A、B、C三种固体物质的溶解度曲线如图所示,请回答:当A中混有少量B时,可采用_____方法提纯 A物质。t2℃时,将75 g A的饱和溶液稀释为20%的溶液,需加水的质量为_____g.t2 ℃时,将A、B、C三种物质的饱和溶液降温至t1 ℃,所得溶液溶质的质量分数由大到小的顺序为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】按要求写出下列反应的化学方程式。
(1)电解水的方程式_____;
(2)铝和硫酸铜溶液的反应方程式_____;
(3)测空气中氧气含量的原理_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的工具,下列化学用语表述不正确的是( )
A.过氧化氢中氢、氧元素的化合价:![]()
B.氯离子的结构示意图: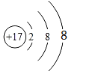
C.工业炼铁的主要反应原理: 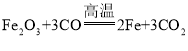
D.淀粉的化学式:C6H10O5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是()
A. 用氢气还原10g氧化铜,加热片刻后,冷却称得剩余固体质量为8.4g,则参加反应的氧化铜的质量是8g
B. 将5g某物质完全溶解于95g水中,所得溶液中溶质的质量分数一定是5%
C. 将3g碳和6g氧气在密闭容器中点燃,充分反应后,容器中的气体为纯净物
D. 将一定量的氢氧化钠和氢氧化钙的混合物溶于足量水中,再向溶液中加入过量的碳酸钠溶液,充分反应后,生成的沉淀质量与原混合物的质量相等,则原混合物中氢氧化钠的质量分数为26%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,通过长颈漏斗向该装置中慢慢加入x,可观察到气球逐渐胀大,再慢慢加入y,又看到气球逐渐变小,则x、y可能分别为( )
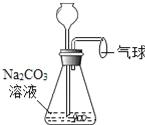
A.盐酸、硫酸铜溶液B.盐酸、饱和澄清石灰水
C.硫酸、氢氧化钠溶液D.硫酸、氯化镁溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将宏观、微观及化学符号联系在一起是化学学科的特点。
(1)A、B、C、D表示四种物质,其微观示意图如图所示:
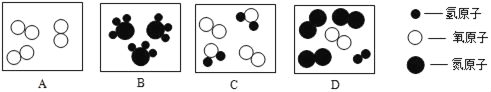
①从微观角度看,B图表示:_____(填化学符号);
②从宏观角度看,图中表示化合物的是_____(填字母符号,下同);
(2)在一定的条件下,A和B能发生化学反应生成 E和F,其中F是单质,其微观示意图如图所示:
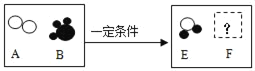
则该反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶未知浓度的氯化钠溶液,小丽要测定其溶质的质量分数。
实验步骤:
(1)取样:小丽测得该NaCl溶液的密度为1.2g/cm3,决定量取出50克氯化钠溶液作为样品量取时用到的仪器有_____。
(2)获取溶质:从氯化钠溶液中得到氯化钠的方法是______。
(3)称量食盐:小丽加了一个砝码,待天平静止时,出现如图所示的情况,小丽接下来的操作是:______。读数,得到氯化钠的质量。
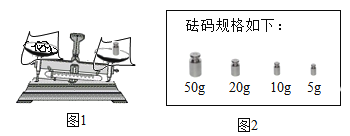
(4)小丽发现有少量氯化钠粘在玻璃棒等器皿上,这对测定结果的影响是___(写“偏大”或“偏小”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com