
【题目】1949年10月1日中华人民共和国成立,在开国大典上首次实现了电动升国旗。为保证国旗不被卷入,要求旗杆上的“阻断球”要足够结实,不易被撞裂。在“阻断球”的制作过程中不仅使用了铁,还熔入了一定比例的铬(Cr)等金属,这是利用了合金____________________的性质。在常见金属活动性顺序中没有铬,同学们决定对铬与常见金属镁和铜的活动性强弱进行探究。
(查阅资料)铬(Cr)是一种银白色金属,其化合物硫酸亚铬(CrSO4)的水溶液呈蓝色。硫酸亚铬中铬元素的化合价为___________。
(提出猜想)三种金属的活动性强弱为:
猜想一:Cr>Mg>Cu;
猜想二:__________;
猜想三:Mg>Cu>Cr
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
①分别向盛有Cr和Cu两种金属片的试管中加入同体积同浓度的稀硫酸 | 只有盛________的试管中有气泡产生,并得到蓝色溶液 | 猜想三错误 |
②向盛有硫酸镁溶液的试管中加入金属Cr | 无明显现象 | 猜想______正确 |
(交流与讨论)
(1)实验前所用的金属片都需用砂纸打磨,目的是_________。
(2)实验①中发生反应的化学方程式为__________。
(3)结合探究结论,有同学提出上述三个实验可进行优化,只需选择三种药品,即可判断金属的活动性强弱。合理的选择是__________(选填序号)。
①硫酸镁溶液 ②硫酸亚铬溶液 ③硫酸铜溶液 ④稀硫酸 ⑤镁片 ⑥铬片 ⑦铜片
(拓展延伸)若将步骤①和②中反应后的混合物倒入同一烧杯中, 搅拌、过滤,得到固体X和溶液Y。则:
(1)溶液Y中溶质的成分__________(选填序号)。
A一定有MgSO4
B一定有CrSO4
C可能有H2SO4
D可能有CuSO4
(2)过滤过程中,用到的玻璃仪器有烧杯、玻璃棒和__________,其中玻璃棒的作用是__________。
【答案】硬度比组成它的纯金属大 +2 Mg>Cr>Cu 铬(或Cr) 二 除去表面的氧化膜(合理即可) ![]() ①③⑥(或②⑤⑦) ABC 漏斗 引流
①③⑥(或②⑤⑦) ABC 漏斗 引流
【解析】
在“阻断球”的制作过程中不仅使用了铁,还熔入了一定比例的铬(Cr)等金属,不易被撞裂。这是利用了合金硬度比组成它的纯金属大的性质;
查阅资料:
铬(Cr)是一种银白色金属,其化合物硫酸亚铬(CrSO4)的水溶液呈蓝色。硫酸亚铬中硫酸根的化合价为-2价,根据化合物中各元素的化合价代数和为零可知,铬元素的化合价为+2;
提出猜想:
已知镁的活动强于铜,三种金属的活动性强弱为:
猜想一:Cr>Mg>Cu;
猜想二:Mg>Cr>Cu;
猜想三:Mg>Cu>Cr
进行实验:
①若猜想三错误,说明Cr的活动性大于Cu,分别向盛有Cr和Cu两种金属片的试管中加入同体积同浓度的稀硫酸,只有盛铬(或Cr)的试管中有气泡产生,并得到蓝色溶液;
②向盛有硫酸镁溶液的试管中加入金属Cr,无明显现象,说明镁的活动性大于铬,猜想二正确;
交流与讨论:
(1)实验前所用的金属片都需用砂纸打磨,目的是除去表面的氧化膜,防止氧化膜干扰实验;
(2)实验①中发生的反应是铬与硫酸反应生在成硫酸亚铬和氢气,反应的化学方程式为![]() ;
;
(3)利用①③⑥,把铬片分别放入硫酸镁、硫酸铜溶液中,伸入硫酸镁溶液中的铬片,无明显现象,说明镁比铬活泼;伸入硫酸铜溶液中的铬片,表面析出红色固体,说明铬比铜活泼;
利用②⑤⑦,把镁片、铜片分别伸入硫酸亚铬溶液中,镁片表面析出银白色固体,说明镁比铬活泼,铜片表面无明显现象,说明铬比铜活泼。故填:①③⑥(或②⑤⑦);
拓展延伸:
步骤①中反应后的混合物一定含有CrSO4、Cu,可能有H2SO4、Cr中的一种;步骤②中反应后的混合物中一定存在MgSO4和Cr,倒入同一烧杯中, 搅拌,能发生的反应是步骤①硫酸与步骤②Cr反应生成CrSO4。过滤,得到固体X和溶液Y。
(1)溶液Y中溶质的成分一定有MgSO4,一定有CrSO4,可能有H2SO4,不可能有CuSO4。故选ABC;
(2)过滤过程中,用到的玻璃仪器有烧杯、玻璃棒和漏斗,其中玻璃棒的作用是引流。


科目:初中化学 来源: 题型:
【题目】下列4个图像中,能正确反映变化关系的是
A. 将水通电电解一段时间
将水通电电解一段时间
B. 镁在空气中加热
镁在空气中加热
C. 加热一定质量的高锰酸钾固体
加热一定质量的高锰酸钾固体
D. 用两份完全相同的过氧化氢溶液分别制取氧气
用两份完全相同的过氧化氢溶液分别制取氧气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了分析生铁中铁的含量,某学习小组进行了如下测定:称取6g生铁,然后将100g稀硫酸平均分五次加入,测得加入稀疏酸质量与放出氢气的质量如下表。(说明:生铁中的杂质不溶于水,也不与硫酸反应)
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
产生氢气的累计质量/g | 0.05 | 0.10 | m | 0.20 | 0.20 |
(1)上表中m的值为__________。
(2)计算生铁中含铁的质量分数是_________?(写出计算过程,结果精确到0.1%)
(3)请根据数据和计算结果,在下图坐标中画出对应的曲线图______。
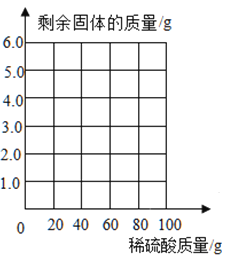
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班化学兴趣小组对催化剂的问题做了以下两类探究,请你一起参与他们的探究活动,并填空:
(1)甲同学探究“催化剂的种类对氯酸钾分解速率的影响”,设计了两组对比实验:
I将3.0g氯酸钾和0.5 g二氧化锰粉末均匀混合加热
II将3.0g氯酸钾和Xg氧化铜粉末均匀混合加热
①在相同条件下比较上述两组实验产生氧气的快慢,实验II中X的值应为___________。
②若氧化铜可以催化氯酸钾分解,写出反应的化学方程式____________。
(2)乙同学探究“红砖粉末是否也可以作为过氧化氢分解的催化剂”。
[提出问题]红砖粉末能不能做“过氧化氢分解”的催化剂呢?
[做出猜想]红砖粉末能做“过氧化氢分解”的催化剂。
[实验验证]
实验步骤 | 实验现象 | 实验结论 |
①将带火星的木条伸入装有过氧化氢溶液的试管中 | 木条不复燃 | 常温下过氧化氢分解速率很慢 |
②在上述试管中加入0.2g红砖粉末,然后将带火星的木条伸入试管中 | 木条复燃 | ①__________________, |
③待上述试管反应停止时,重新加入过氧化氢溶液,并把带火星的木条伸入试管 | 在化学反应前后,红砖粉末的②____________没有改变。 |
[实验讨论]
有同学认为:仅凭上述实验还不能证明红砖粉末能做过氧化氢分解的催化剂,还需要增加一个实验。 将实验后剩余固体提纯后称量,如果所得固体的质量等于0.2g,则说明红砖粉末可以作为过氧化氢分解的催化剂。
[实验拓展]查阅资料得知:硫酸铜、猪肝、土豆等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是____________(填字母)。
A催化剂能增加生成物的量
B在工业生产中催化剂起到极大的作用
C催化剂只能加快化学反应的速率
D同一个化学反应可以有多种催化剂
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气和水是人类赖以生存的物质基础。
(1)为减少煤燃烧带来的空气污染,可将其转化为可燃性气体,此过程可认为是碳与水的反应,其微观示意图如图所示:
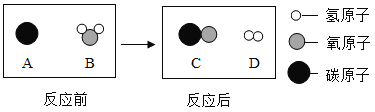
A、B、C、D四种物质中,属于氧化物的是__________(选填序号);该反应中生成的C和D的分子个数比为___________。
(2)NH3作为一种新燃料,具有无碳(不产生温室气体二氧化碳)、发热量高等优点。
①NH3燃烧的化学方程式是: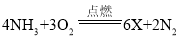 ,其中X的化学式为___________。
,其中X的化学式为___________。
②NH3作为燃料还具有的优点是______________。
(3)由于活性炭具有______________的结构,所以活性炭具有较好的吸附性,可除去水中的_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列现象说明空气中存在着某种物质请将物质的名称或符号写在空格内。
(1)小白鼠在装有空气的密闭容器内可存活一段时间,说明空气内存在着_____________。
(2)石灰水长期露置在空气中。瓶壁和石灰水底部会出现白色固体物质说明空气中有______________。写出相关反应的化学方程式_________________。
(3)夏天,盛放冰棒的杯子外壁上附有一层水珠说明空气中有______________。
(4)空气可以用于制氮肥,说明空气中有______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是最简明、信息丰富、国际通用的语言请用化学用语填空:
(1)2个氢原子____________。
(2)氢氧根离子_____________。
(3)氯化亚铁_____________。
(4)五氧化二磷中氧的化合价___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图象能正确反映对应变化关系的是( )
A.在密闭容器中用红磷测定空气中氧气的含量
B.向盛有二氧化锰的烧杯中不断加入过氧化氢溶液
C.等质量氯酸钾制氧气
D.加热高锰酸钾制取氧气时剩余物的质量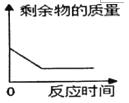
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com