
【题目】相关实验原理与化学反应方程式的书写都正确的是( )
A. 铁丝在氧气中燃烧:4Fe+3O2![]() 2Fe2O3
2Fe2O3
B. 洗去试管壁上附着的铜:Cu+H2SO4=CuSO4+H2↑
C. 用氢氧化钠吸收二氧化硫:2NaOH+SO2=Na2SO4+H2O
D. 工业制取二氧化碳:CaCO3![]() CaO+CO2↑
CaO+CO2↑
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案科目:初中化学 来源: 题型:
【题目】往200克含有稀硝酸和硝酸钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图(假设生成的气体全部逸出),试分析计算:
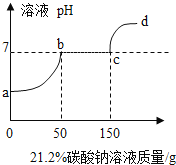
(1)a→b段发生反应的化学方程式为______;
(2)反应中生成的沉淀质量为多少______?
(3)c→d段溶液的pH大于7的原因是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究一氧化碳跟氧化铜反应,某实验小组进行了下列实验:
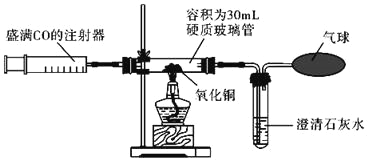
(1)实验操作:
①按如图装好药品、连好仪器,确保装置的气密性良好。
②轻轻推动注射器活塞,向硬质玻璃管中注入_____mL一氧化碳气体,排尽其中空气。
③点燃酒精灯加热氧化铜,继续缓缓推入一氧化碳气体。开始加热后即可观察到的现象是_____,约1分钟后观察到的现象是_____,约3分钟后观察到的现象是_____。
④此时熄灭酒精灯,停止通入一氧化碳气体。
(2)根据上述实验写出一氧化碳跟氧化铜反应的化学方程式_____。
(3)实验结束后,为了防止有毒气体污染环境,处理剩余气体的方法是_____。
(4)玻璃注射器常用规格有5mL、10mL、20mL、50mL、100mL.本实验中应选用的注射器规格是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】由下面粒子结构示意图得出的结论不正确的是 ( )
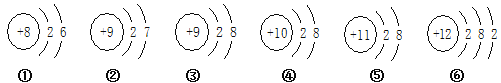
A. ②③属于同种元素B. ①②均易形成阴离子
C. ③④⑤属于离子D. ⑥是镁原子结构示意图
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两物质的溶解度曲线如图所示,请据图回答下列问题。
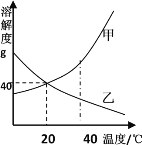
⑴20℃时,甲物质的溶解度是______g;
⑵从甲的饱和溶液中获得甲,可采用______方法。
⑶欲将40℃时乙物质的饱和溶液变为不饱和溶液,可采用的方法是______;(写一种即可)
⑷40℃时,将甲、乙两物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数的大小关系是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】NH4Cl和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |

A. t3应介于40℃~50℃
B. 将t3℃时Na2SO4的饱和溶液降温至t1℃,c点将沿曲线c→b→a运动
C. 甲、乙饱和溶液从t2升温到t3,溶质的质量分数都不变
D. 将d点甲、乙溶液移至c点,可采用的方法只有加入溶质甲、乙,且溶质质量分数增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(一)铁材料的有关知识
(1)人类使用金属先后经历了“青铜”、“铁器”时代,到近代才开始大量使用铝材料.这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是_____.
(2)在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理_____.
(3)钢铁露置在空气中易生锈,写出一种防止钢铁生锈的方法_____.
以下是同学对铁锈的成分、铁锈制草酸亚铁晶体及草酸亚铁晶体热分解的研究.
(二)用上述铁锈制草酸亚铁晶体(FeC2O4·nH2O)
资料:①FeSO4遇到氧气氧化,会转化为Fe2(SO4)3.
②FeSO4的溶解度如下表:
温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
(制备流程)
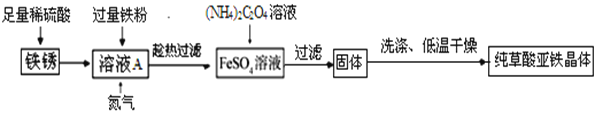
(1)溶液加入过量铁粉,发生的反应有:Fe+Fe2(SO4)3=3FeSO4、_____.充分反应后要趁热过滤的目的是_____.
(2)流程中产生草酸亚铁晶体反应的化学方程式为_____.
(3)制备过程中,溶液中通入氮气的作用是_____.
(三)探究FeC2O4·nH2O热分解的产物及n的值
(实验装置)
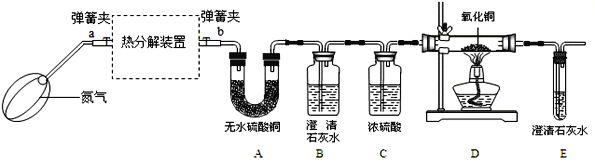
资料:①FeC2O4·nH2O为淡黄色粉末;FeO和Fe3O4都是黑色固体,其中FeO易被氧气氧化.
②FeC2O4·nH2O加热至300℃完全失去结晶水;继续加热至400℃,剩余固体受热分解产生黑色固体、CO2和CO.
(实验分析)
(1)若通过E装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解产生CO,则需在B和C装置之间增加盛有_____(填试剂名称)的洗气瓶.
(2)先鼓入氮气,再加热分解装置的原因是_____.
(3)指出上述实验装置不足之处_____.
(4)取3.60gFeC2O4·nH2O,按上述实验步骤进行实验,测得热分解装置中固体量随温度变化曲线如下图所示:
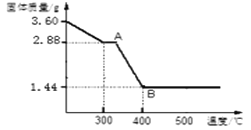
①FeC2O4·nH2O中n的值为_____.
②反应后,热分解装置中残留的黑色物质为_____(填化学式).
③草酸亚铁晶体受热分解的方程式为_____.
④若将图中1.44g固体在空气中充分加热,固体增加0.16g,此固体(铁的氧化物)为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】维生素C(化学式为C6H8O6)是人体必须的营养物质,能提高免疫力,预防癌症,保护牙龈等。下列有关维生素C的说法错误的是
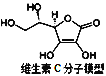
A. 维生素C中碳、氢、氧原子的个数比为3:4:3
B. 维生素C分子中含有20个原子核
C. 维生素C分子中质子数和电子数一定相等
D. 维生素C分子是由三种元素的原子构成的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com