
【题目】在一定条件下,向一密闭的容器内加入A、B、C、D四种物质各20g,充分反应后,测定其质量,得到数据如下:
物质 | A | B | C | D |
反应前质量/g | 20 | 20 | 20 | 20 |
反应后质量/g | 20 | 30 | 未知 | 14 |
(1)反应后C的质量是_____g。
(2)A物质可能是_____(填“反应物”或“生成物”“催化剂”)。
(3)容器中B物质肯定是_____填“单质”或“化合物”)。
(4)容器中发生反应的基本反应类型是_____。
【答案】16 催化剂 化合物 化合反应
【解析】
A物质反应前后质量没有变化,可能是催化剂或没有参加反应,B物质反应后质量增加,为生成物,C物质反应后质量减少,为反应物,D物质反应后质量减少,为反应物,,则反应物C和D生成B。
(1)根据质量守恒定律,反应前反应物的总质量等于生成物的总质量,
![]() ,未知=16,反应后C的质量是16g。
,未知=16,反应后C的质量是16g。
(2)催化剂在反应前后质量和化学性质均不变,A物质反应前后质量没有变化,可能是催化剂。
(3)A物质反应前后质量没有变化,可能是催化剂或没有参加反应,B物质反应后质量增加,为生成物,C物质反应后质量减少,为反应物,D物质反应后质量减少,为反应物,,则反应物C和D生成B,故容器中B物质肯定是化合物。
(4)C和D反应后质量减少,为反应物,B物质反应后质量增加,为生成物,A物质反应前后质量没有变化,可能是催化剂或没有参加反应,故容器中发生反应的基本反应类型是化合反应。


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:初中化学 来源: 题型:
【题目】根据下列元素的原子结构示意图填空.

(1)氧元素和硫元素化学性质相似的原因是它们的原子________相同;
(2)由铝元素和氯元素组成化合物的化学式为________.
(3)下图是某化学反应前后的微观模拟图,请根据图示回答.
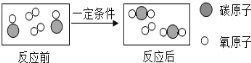
①标出生成物中氧元素的化合价________;
②写出图示反应的化学方程式________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】焦炭(主要成分是碳单质,杂质不与水反应) 与水蒸气在高温条件下反应,能产生一种俗称为水煤气的气体燃料,可能还有H2、CO、CO2.某小组同学设计了如下实验装置并进行实验。实验后发现 A 装置中溶液变浑浊,D 中的固体由黑色变红色,E 中的固体由 白色变蓝色,G 装置中有水流入烧杯。(已知无水硫酸铜遇水蒸气变蓝,碱石灰能吸收二氧化碳和水蒸气,浓硫酸能吸收水蒸气)。
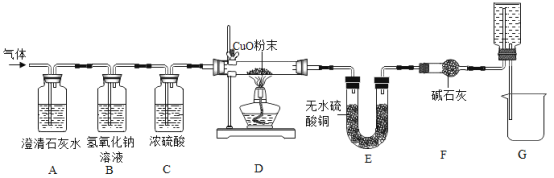
在反应前后对D、E装置进行了质量的测量(各步反应均完全),测量结果如表:
装置及药品 | 反应前 | 反应后 |
D装置中玻璃管与固体的总质量/g | 223.3 | 215.0 |
E装置中U型管与固体的总质量/g | 260.0 | 267.2 |
请分析回答下列问题:
(1)水煤气中一定含有CO2的理由是_____(用化学方程式表示)。
(2)一定能证明水煤气中有氢气存在的实验现象是_____,_____。
(3)G 装置的作用:①“抽气”;②_____。
(4)该小组同学通过数据分析,证明水煤气中存在 CO 气体,请利用上表中的原始数据,列出数据分析过程(只列式不计算)。_____
(5)同学们发现,不通过测量反应前后装置的质量,也可方便的证明 CO 气体的存在。 需增加一个图中的装置_____(填装置序号)来代替装置 F。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】尿素[(NH2)2CO]是农业上重要的氮肥。工业上合成尿素的工艺流程如下:
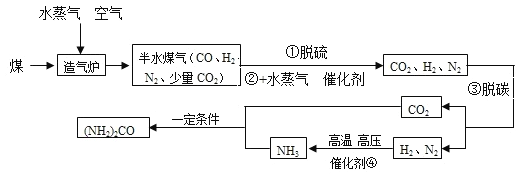
(1)煤是我国目前主要的化石燃料,主要含有_____;煤燃烧时排放出_____和_____等污染物会形成酸雨。
(2)造气炉中发生反应: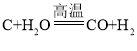 ,
,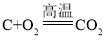 ,上述两个反应中表现还原性的物质是_____(填化学式)。
,上述两个反应中表现还原性的物质是_____(填化学式)。
(3)脱碳过程③是通过一定的工艺流程将CO2与H2、N2分离,此过程发生的是_____(填“物理变化”或“化学变化”)。
(4)反应④的反应基本类型是_____。
(5)写出由CO2和NH3合成尿素[(NH2)2CO]并生成水的反应方程式_____。
(6)氢气是最清洁的能源,工业上可用电解水的方法制取氢气,写出反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
制氢:铁酸锌( ZnFe2O4)可用于循环分解水制氢,其反应可表示为:
![]() ;
;![]()
(1) ZnFe2O4中Fe的化合价为_____。
(2)该循环制氢的过程中,不断被消耗的物质是_____(填化学式)。
(3)氢气作为新能源的优点有_____(任写一点),该循环法制氢的不足之处是_____。
(4)下列说法正确的是_____(填序号)。
A 能源结构向多元、清洁、低碳转型
B 科技进步会促进能源的利用
C 石油和太阳能属于可再生能源
D 生活中的废热可转化为电能
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组欲通过实验测定某种石灰石中碳酸钙的质量分数。取该石灰石样品8.0g,将80mL稀盐酸分四次加入,所得数据如下表(已知该石灰石中的杂质不溶于水,也不与稀盐酸反应):
实验序号 | 1 | 2 | 3 | 4 |
加入稀盐酸的体积(mL) | 20 | 20 | 20 | 20 |
充分反应后剩余固体的质量(g) | 5.5 | m | 1.2 | n |
(1)上表中,m=_____,n=_____。
(2)该石灰石中碳钙的质量分数为_____。
(3)若要制取6.6g二氧化碳,至少需要该石灰石多少克?_____(写出计算过程,结果精确到0.lg)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用如图所示的装置进行实验,验证质量守恒定律。
| 实验1 | 实验2 | ||
实验药品 | 硫酸铜溶液、铁 | 过氧化氢溶液、二氧化锰 | ||
电子秤示数 | 反应前 | m1 | m3 | |
反应后 | m2 | m4 | ||
(1)实验2发生反应的化学方程式为____________________________。
(2)实验2中药品混合后,烧杯内可观察到的现象为___________________。
(3)比较反应前后电子秤示数,描述正确的是__________(填序号)。
Am1=m2 Bm1<m2 Cm3= m4 Dm3> m4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在测定质量守恒定律时,某同学设计了如图A、B两个实验,根据质量守恒定律回答下列问题:
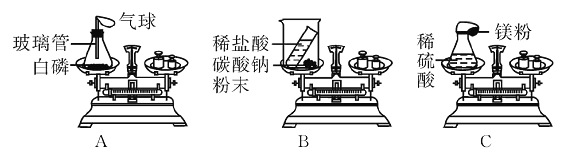
(1)通过实验知道,实验A中反应前后质量总和相等,在该实验中气球变化的现象是________,实验B中测得反应前后质量减小了,质量减小的原因是_____,若要使该实验测得的质量相等,需要进行如何改进_______。
(2)以上两个实验中,满足质量守恒定律的是______。
(3)某学生在课外研究性学习活动课上用如图C所示的装置做实验,瓶内放了足量的稀硫酸,气球内放有一定量的镁粉,将它紧紧栓在瓶口上,放在托盘天平上称量,质量为W1,然后将气球内的镁粉全部倒入瓶内,反应的方程式为(Mg+H2SO4=== MgSO4+H2↑),观察到立即产生大量的气泡,气球逐渐胀大,充分反应后最终再次称量,质量为W2,结果W1>W2(装置不漏气)。反应后称得质量减小的原因是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的运用。
(1)硬水与软水:
我国有些村庄为了获取淡水采用打深井取地下水的方法。检验地下水是硬水还是软水,可以取水样加入少量_____,振荡,若观察到_____(填实验现象),说明是硬水。使用硬水会给生产、生活带来麻烦,生活中常用_____的方法来降低水的硬度。
(2)水的净化:
某自来水厂净水过程如下:

①炭滤池中常用煤粉替代活性炭,这说明煤粉具有的性质是_____。
②下列说法正确的是_____(填字母)
A 加入絮凝剂可使悬浮杂质沉降
B 通过砂滤池可除去某些可溶性杂质
C 用蒸馏的方法可降低自来水的硬度
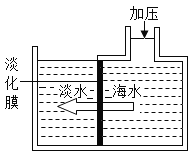
③海水淡化可采用膜分离技术。如图所示,对淡化膜右侧的海水加压,水分子可以通过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。该海水淡化过程属于_____变化。(填“物理"或“化学")
(3)水资源的利用:
水危机日趋严重,节水是每个公民义不容辞的责任,请你结合生活提一条节水建议_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com