
【题目】请结合以下图示,回答问题。
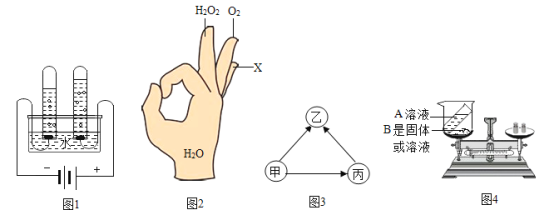
(1)如图1所示,电解水的实验中正极与负极产生气体的质量比为____。
(2)如图2所示,小明用手势OK表示初中常见化学反应中生成水的不同方法,要求手指上的物质分别通过某种基本反应类型直接生成水(如图中的H2O2、O2),X不能选择下列A、B、C、D4种物质中的____(填序号)
ACuO BH2CO3 CC2H5OH DCa(OH)2
(3)如图3所示,“→”表示一种金属能把另一种金属从其盐溶液中置换出来,则甲、乙、丙三种金属的活泼性由强到弱的顺序是____(用“甲、乙、丙”表示)。
(4)如图4所示,某同学用此装置验证质量守恒定律的实验,下列药品不能达到该实验目的的是____(填序号)。
A 火碱和稀盐酸反应 B 铁和稀盐酸反应
C 铁和硝酸锌溶液反应 D 硫酸和氯化钠溶液
【答案】8:1 C 甲>丙>乙 BCD
【解析】
(1)电解水时正极生成氧气,负极生成氢气,根据反应的化学方程式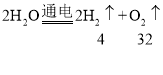 ,可以求出生成氧气和氢气的质量比为:32:4=8:1;
,可以求出生成氧气和氢气的质量比为:32:4=8:1;
(2)A、CuO和酸或者氢气反应都能生成水,和酸反应是复分解反应,和氢气反应是置换反应,都属于基本反应类型,不符合题意;
B、碳酸分解生成水和二氧化碳,该反应属于分解反应,属于基本反应类型,不符合题意;
C、酒精和氧气在点燃的条件下生成二氧化碳和水,不是基本反应类型,符合题意;
D、稀盐酸与氢氧化钙反应生成氯化钙和水,属于复分解反应,属于基本反应类型,不符合题意。故选C。
(3)由图中金属与盐溶液的反应关系可知,金属甲能把金属丙从其盐溶液中置换出来,说明金属甲的活动性比丙强;金属丙能把金属乙从其盐溶液中置换出来,说明金属丙的活动性比乙强;因此三种金属的活动性由弱到强的顺序为:甲>丙>乙。
(4)A、氢氧化钠溶液和稀盐酸反应生成氯化钠和水,可以验证质量守恒定律,不符合题意;
B、铁与稀盐酸反应生成氯化亚铁和氢气,有气体生成应在密闭环境中进行,本装置不可以验证质量守恒定律,符合题意;
C、铁和硝酸锌溶液不反应,不可以验证质量守恒定律,符合题意;
D、硫酸和氯化钠溶液不反应,不可以验证质量守恒定律,符合题意。故选BCD。


科目:初中化学 来源: 题型:
【题目】下列实验方案中,能达到目的的是( )
A.比较金属的活动性强弱:将等质量的铁丝和锌粒放入等浓度的稀盐酸中
B.粗略地测定空气中氧气的含量:用铁丝代替红磷在空气中燃烧
C.制取![]() :将
:将![]() 溶液和
溶液和![]() 溶液混合后过滤
溶液混合后过滤
D.除去![]() 溶液中少量的盐酸:加过量的
溶液中少量的盐酸:加过量的![]() 粉末,充分反应后过滤
粉末,充分反应后过滤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图A、B、C三种固体的溶解度曲线回答;
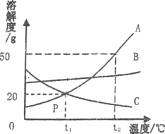
(1)要使C的饱和溶液成为不饱和溶液,可采用_________的方法。(填一种即可)
(2)要除去B中的少量A,可采用_________的方法。
(3)将t2℃时三种物质的饱和溶液分别降温到t1℃,所得溶液中溶质的质量分数由大到小的顺序是_________(填字母)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像中有关量的变化趋势正确的是
A.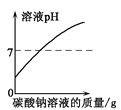 向一定量的盐酸和氯化钡的混合溶液中,逐滴加入碳酸钠溶液至过量
向一定量的盐酸和氯化钡的混合溶液中,逐滴加入碳酸钠溶液至过量
B.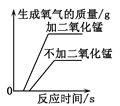 加热等质量的两份氯酸钾,一份加入二氧化锰,一份不加二氧化锰
加热等质量的两份氯酸钾,一份加入二氧化锰,一份不加二氧化锰
C.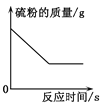 一定量的硫粉与过量的氧气在密闭容器内点燃并充分反应
一定量的硫粉与过量的氧气在密闭容器内点燃并充分反应
D.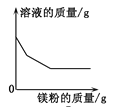 向一定量的氯化亚铁和氯化铜的混合溶液中,逐渐加入镁粉至过量
向一定量的氯化亚铁和氯化铜的混合溶液中,逐渐加入镁粉至过量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是以实验为基础的科学,实验是科学探究的重要手段。
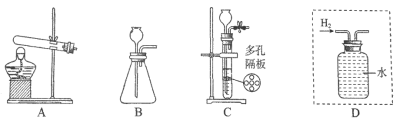
(1)如图是实验室制取气体的常用装置。
①写出一个用A装置制取O2的化学方程式_____。
②B和C装置均可制取CO2,与B装置比较,C装置的优点是什么?_____
③若用D装置采用排水法收集H2,在图中将导管补画完整_____。
(2)如图所示,实验小组用微型实验装置“W”形玻璃管探究燃烧的条件。
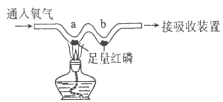
①对比a、b处的实验现象,可知可燃物燃烧的条件之一是什么?_____
②若验证可燃物燃烧的另一个条件,还需补充的实验操作是什么?_____
(3)某趣味实验装置如图所示,其气密性良好。
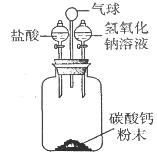
①先向广口瓶中加稀盐酸至碳酸钙粉末恰好全部溶解。关闭活塞,震荡,观察到气球变大。然后再将一定量的氢氧化钠溶液加入广口瓶中,关闭活塞,震荡,观察到气球变小且广口瓶中产生白色沉淀。请写出引起气球变小的反应化学方程式_____。
②反应结束后,小明将废液过滤,并对滤液成分进行探究,取滤液少许于试管中,加入足量稀盐酸,发现有气泡产生。于是小明得出结论:滤液的溶质组成为Na2CO3、NaCl,你认为滤液的溶质组成还可能是什么_____?请写出你的猜想并设计实验证明你的猜想,简要写出实验步骤和现象_____。
(4)某同学为测定一瓶过氧化氢溶液的质量分数,取该溶液34.0 g,加入二氧化锰1.0 g,待完全反应不再有气体逸出时,称得剩余物质的总质量为34.2 g。请计算该过氧化氢溶液中溶质的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示)。小强和小华同学很感兴趣,决定对其成分进行探究。
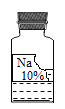
(提出问题)这瓶试剂可能是什么溶液呢?
(交流讨论)根据受损标签的情况判断,这瓶试剂不可能是____。(填序号)
A 酸 B 碱 C 盐
(查阅资料)Ⅰ初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3。
ⅡNa2CO3和NaHCO3的水溶液都呈碱性。
Ⅲ室温(![]() )时,测定四种物质的溶解度数据如下:
)时,测定四种物质的溶解度数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度g | 36 | 109 | 215 | 9.6 |
小华根据试剂瓶标注的质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是___。
(作出猜想)①可能是NaCl;②可能是Na2CO3;③可能是____。
(实验探究)(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH7,则这瓶试剂不可能是____。
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验。
实验步骤 | 实验现象 | 结论及化学方程式 |
①取少量溶液于试管中,滴加____。 | 产生大量气泡 | 反应的化学方程式:___。 |
②把产生的气体通入澄清的石灰水中。 | 澄清的石灰水变浑浊 | 猜想②正确。反应的化学方程式:____。 |
(拓展延伸)请你选择与小强不同类别的试剂,来鉴别NaOH溶液和Na2CO3溶液,你选择的试剂是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了除去粗盐中的杂质得到纯净的氯化钠,进行了下列实验。
I.除去粗盐中难溶性杂质:
(1)实验步骤:①溶解→②__________→③蒸发。(填操作名称)
(2)在以上的三步操作中均会用到一种常见的玻璃仪器是__________。
II.经过上面的操作所得的氯化钠中还混有一些可溶性杂质,为了将混有硫酸钠、氯化钙的氯化钠提纯,某同学设计的实验流程如下:
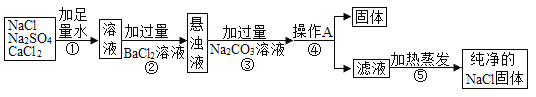
请根据以上流程图中的信息,回答下列问题:
(3)步骤②中发生反应的方程式为_____________;
(4)步骤④中所得固体中含有________________;(填化学式)
(5)此方案并不严谨,应该在步骤⑤加热蒸发之前加入过量的__________(填试剂名称)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室的部分实验装置图,回答有关问题
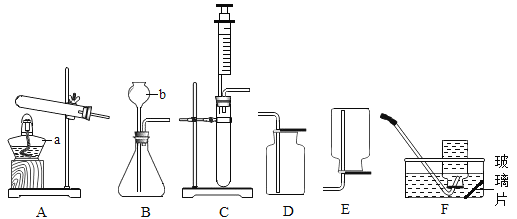
(1)写出仪器名称:a:______ b:______
(2)实验室常用过氧化氢溶液和二氧化锰制取氧气,若要控制反应速率,要收集较为纯净的氧气,应选择的发生和收集装置是______(填字母);写出该反应的化学方程式:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像不能正确反映其对应变化关系的是
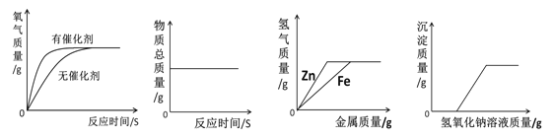
A B C D
A. 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气
B. 一定质量的红磷在密闭容器中燃烧
C. 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
D. 向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com