
【题目】逻辑推理是一种重要的思维方法,以下推理合理的是( )
A.因为碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液
B.因为![]() 和
和![]() 的组成元素相同,所以它们的化学性质相同
的组成元素相同,所以它们的化学性质相同
C.因为蜡烛燃烧生成![]() 和
和![]() ,所以蜡烛组成中一定含有碳、氢元素,可能含氧元素
,所以蜡烛组成中一定含有碳、氢元素,可能含氧元素
D.因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件
科目:初中化学 来源: 题型:
【题目】蜡烛(足量)在如图的密闭装置内燃烧至熄灭,用仪器测出这一过程中瓶内氧气含量的变化如图所示,下列判断的正确是( )
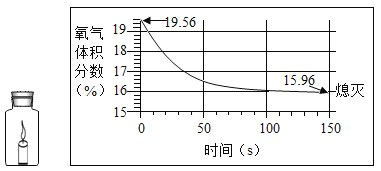
A.该实验说明燃烧只需要氧气
B.蜡烛熄灭的原因是瓶内氧气已经耗尽
C.氧气浓度小于一定值时,蜡烛就无法燃烧
D.蜡烛熄灭后,瓶内只剩二氧化碳气体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】密闭容器内,有甲、乙,丙、丁四种物质,在一定条件下充分混合反应,测得反应前后各物质的质量分数如图所示。下列说法错误的是( )
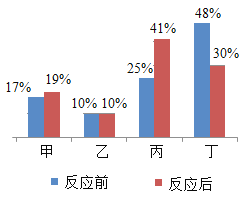
A.反应生成甲和丙的质量比为8:1
B.乙可能是该反应的催化剂
C.该反应是分解反应
D.丁一定是化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水产养殖的速效增氧剂“鱼浮灵”的主要成分是过氧碳酸钠(![]() )。某化学研究小组对“鱼浮灵”的制备、成分测定及增氧原理进行了如下探究。
)。某化学研究小组对“鱼浮灵”的制备、成分测定及增氧原理进行了如下探究。
(查阅资料)①过氧碳酸钠有![]() 和
和![]() 的双重性质;50℃开始分解。
的双重性质;50℃开始分解。
②过氧碳酸钠在异丙醇(有机溶剂)中的溶解度较低。
Ⅰ.“鱼浮灵”的制备。
实验室用![]() 与稳定剂的混合溶液和30%的
与稳定剂的混合溶液和30%的![]() 溶液反应制备过氧碳酸钠,实验装置如图所示。
溶液反应制备过氧碳酸钠,实验装置如图所示。
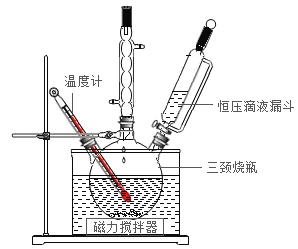
(1)反应温度不能超过20℃的原因是_____。
(2)反应结束后,停止搅拌,向反应液中加入异丙醇,静置过滤、洗涤、干燥,获得过氧碳酸钠固体。加入异丙醇的目的_____。
Ⅱ.“鱼浮灵”的成分测定。
(定性检测)检测过氧碳酸钠溶液中的成分。
(3)请补充完成下列实验报告中的相关内容。
实验序号 | 实验步骤 | 实验现象 | 解释或结论 |
① | 取样,加入 | 木条复燃 | 反应的化学方程式 _____ |
② | _____ | _____ | 溶液中含有 |
(定量研究)测定“鱼浮灵”中过氧碳酸钠的组成。
实验③:称取一定质量的“鱼浮灵”样品于小烧杯中,加适量水溶解,向小烧杯中加入足量![]() ,溶液,过滤、洗涤、干燥,得到碳酸钡(
,溶液,过滤、洗涤、干燥,得到碳酸钡(![]() )固体3.94g。
)固体3.94g。
实验④:另称取相同质量的“鱼浮灵”样品于锥形瓶中,加入足量稀硫酸,再逐滴加入高锰酸钾溶液,充分反应,消耗![]() 的质量为1.896g,该反应的原理是:
的质量为1.896g,该反应的原理是:
![]() 。
。
(4)计算确定过氧碳酸钠(![]() )的化学式_____(写出计算过程)。
)的化学式_____(写出计算过程)。
Ⅲ.“鱼浮灵”的增氧原理。
研究小组通过测定常温下相同时间内水溶液中溶解氧的变化,探究![]() 、
、![]() 对
对![]() 分解速率的影响,设计了对比实验,实验数据记录如下表。
分解速率的影响,设计了对比实验,实验数据记录如下表。
编号 | ① | ② | ③ | ④ | ⑤ |
试剂 |
|
|
|
|
|
pH | 6.96 | 6.01 | 8.14 | 8.15 | 9.26 |
溶解氧( | 5.68 | 6.44 | 9.11 | 9.12 | 10.97 |
(5)由实验②可知,常温下,过氧化氢水溶液呈_____(填“酸性”“中性”或“碱性”)。
(6)过氧碳酸钠可以速效增氧的原理是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
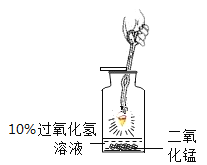
【题目】实验是化学研究的基础,结合下列实验装置及图示回答问题。
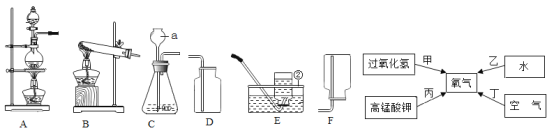
(1)图中a的仪器名称是______。
(2)“绿色化学要求利用化学原理从源头上消除污染,实验室制取氧气的方法中最能体现绿色化追求的途径是_____(填编号),该反应的化学方程式是______。
(3)若用二氧化锰和浓硫酸混合加热制备氧气,应选择的发生装置和收集装置的组合是______(填字母编号).
(4)做铁丝在氧气中燃烧的实验改进如图所示,其优点是实验简便、保证安全和______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线.
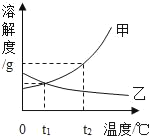
(1)_____℃时,甲、乙两种物质的溶解度相等;
(2)把甲物质的不饱和溶液变为饱和溶液,下列有关说法正确的是_____;(填序号,下同)
A 溶剂的质量一定变小
B 溶质的质量可能不变
C 溶质的质量分数一定变大
D 溶液的质量一定变大
E 该饱和溶液还可以溶解其他物质
(3)通常情况下,在实验室用固体甲配制一定溶质质量分数的甲溶液,需用到的仪器有:托盘天平(带砝码盒)、烧杯和_____.
A 酒精灯 B 药匙 C 玻璃棒 D 漏斗 E 铁架台 F 量筒 G 胶头滴管
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为检验当地石灰石中含碳酸钙的质量分数,在实验直将6g石灰石样品(杂质不参如反应,也不溶解于水)放入盛有19g稀盐酸的烧杯中,恰好完全反应,测得烧杯中物质的总质量为22.8g,求(保留小数点后一位)
(1)生成二氧化碳的质量为_____。
(2)所用稀盐酸的溶质的质量分数?_____
(3)样品中碳酸钙的质量分数。_____
(4)反应后所得溶液的溶质质量分数是多少?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 等质量的![]() 和
和![]() ,氧元素质量比为5:6
,氧元素质量比为5:6
B. 等质量的![]() 和
和![]() ;混合后,氮元素质量分数大于35%
;混合后,氮元素质量分数大于35%
C. 等质量的水和过氧化氢,完全分解后生成氧气的质量比为17:9
D. 等质量、等质量分数的氢氧化钾溶液和稀盐酸,充分反应后,所得溶液呈碱性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com