
【题目】汽车制造是盐城市的支柱经济产业之一,汽车制造过程中要用到大量的铁、铜、铝等金属材料,请按要求填空.
(1)汽车制造中用得最多的金属材料是钢.钢(填“是”或“不是”)纯金属.车体表面喷漆不仅美观,而且可有效防止钢铁与接触而生锈.炼铁的原理是利用一氧化碳与氧化铁反应还原出铁,反应的化学方程式为 .
(2)汽车电路中的导线大都是铜芯的,这主要是利用了铜的性.将赤铜矿(主要成分Cu2O)和辉铜矿(主要成分Cu2S)混合焙烧可得到铜,请将反应的方程式补充完整:2Cu2O+Cu2S ![]() 6Cu+ .
6Cu+ .
(3)铁、铜、铝三种因素在地壳中的含量多少顺序为Al>Fe>Cu,但三种金属被人类发现和利用的时间是铜最早,而铝最晚,这跟它们的有关.铝具有很好的抗腐蚀性能,原因是 .
(4)镁铝合金是汽车制造中的重要材料之一.为测定某镁铝合金(只含镁、铝两种元素)的组成成分,某学习小组取3.9g合金粉末加入100.0g过量的盐酸中,向充分反应后的溶液中加入过量20.0%的氢氧化钠溶液,最终得到沉淀2.9g.
【质疑】通过讨论,大家认为得到的沉淀质量数据可能有问题.按初中化学现有知识计算,沉淀的质量至少为 g.
(5)【探讨】经向老师请教,同学们了解到氢氧化铝沉淀可与氢氧化钠溶液反应,产生可溶性的偏铝酸钠,反应如下:NaOH+Al(OH)3═NaAlO2+2H2O
【计算】若已知产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示,请计算:
①该合金中镁的质量为 g;铝的质量为 g.
②加入的盐酸溶质质量分数为多少?(请写出计算过程)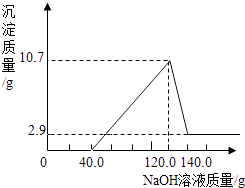
【答案】
(1)不是;水和氧气;Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
(2)导电;SO2↑
(3)金属活动性;铝与氧气反应形成了一层致密的氧化铝薄膜
(4)9.425
(5)1.2;2.7;解:设与1.2g镁反应的盐酸中溶质的质量为p
Mg+ | 2HCl═MgCl2+H2↑ |
24 | 73 |
1.2g | p |
![]() 解得:p=3.65g
解得:p=3.65g
设与2.7g铝反应的盐酸中溶质的质量为q
2Al+6HCl═ | 2AlCl3+3H2↑ |
54 | 219 |
2.7g | q |
![]() 解得:q=10.95g
解得:q=10.95g
设与氢氧化钠反应的盐酸中溶质的质量为n
HCl+ | NaOH=NaCl+H2O |
36.5 | 40 |
n | 40g×20.0% |
![]() 解得:n=7.3g
解得:n=7.3g
加入的盐酸溶质质量分数为: ![]() =21.9%
=21.9%
【解析】解:(1)汽车制造中用得最多的金属材料是钢.钢不是纯金属,是铁的合金.车体表面喷漆不仅美观,而且可有效防止钢铁与水和氧气接触而生锈.炼铁的原理是利用一氧化碳与氧化铁反应还原出铁,反应的化学方程式为:Fe2O3+3CO ![]() 2Fe+3CO2 . (2)汽车电路中的导线大都是铜芯的,这主要是利用了铜的导电性.将赤铜矿(主要成分Cu2O)和辉铜矿(主要成分Cu2S)混合焙烧可得到铜,由反应的方程式及质量守恒定律可知,应填入:SO2↑.(3)铁、铜、铝三种因素在地壳中的含量多少顺序为Al>Fe>Cu,但三种金属被人类发现和利用的时间是铜最早,而铝最晚,这跟它们的金属活动性有关.铝具有很好的抗腐蚀性能,原因是铝与氧气反应形成了一层致密的氧化铝薄膜.
2Fe+3CO2 . (2)汽车电路中的导线大都是铜芯的,这主要是利用了铜的导电性.将赤铜矿(主要成分Cu2O)和辉铜矿(主要成分Cu2S)混合焙烧可得到铜,由反应的方程式及质量守恒定律可知,应填入:SO2↑.(3)铁、铜、铝三种因素在地壳中的含量多少顺序为Al>Fe>Cu,但三种金属被人类发现和利用的时间是铜最早,而铝最晚,这跟它们的金属活动性有关.铝具有很好的抗腐蚀性能,原因是铝与氧气反应形成了一层致密的氧化铝薄膜.
(4)【质疑】
假设镁的质量是3.9g,生成的氢氧化镁的质量是x
Mg~ | Mg(OH)2 |
24 | 58 |
3.9g | x |
![]() 解得:x=9.425g
解得:x=9.425g
假设铝的质量是3.9g,生成的氢氧化铝的质量是y
Al~ | Al(OH)3 |
27 | 78 |
3.9g | y |
![]() 解得:y≈11.27g
解得:y≈11.27g
按初中化学现有知识计算,沉淀的质量至少为9.425g.
【计算】①设该合金中镁的质量为m
Mg~ | Mg(OH)2 |
24 | 58 |
m | 2.9g |
![]() 解得:m=1.2g
解得:m=1.2g
铝的质量为:3.9g﹣1.2g=2.7g
故答为:(1)不是,水和氧气,Fe2O3+3CO ![]() 2Fe+3CO2 . (2)导电,SO2↑;(3)金属活动性,铝与氧气反应形成了一层致密的氧化铝薄膜.(4)【质疑】9.425g.【计算】①1.2;2.7.②21.9%.
2Fe+3CO2 . (2)导电,SO2↑;(3)金属活动性,铝与氧气反应形成了一层致密的氧化铝薄膜.(4)【质疑】9.425g.【计算】①1.2;2.7.②21.9%.
【考点精析】根据题目的已知条件,利用金属的物理性质及用途和金属材料的选择依据的相关知识可以得到问题的答案,需要掌握金属的物理性质: (1)常温下一般为固态(汞为液态),有金属光泽.(2)大多数呈银白色(铜为紫红色,金为黄色)(3)有良好的导热性、导电性、延展性;黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:
【题目】2015年4月28日召开的国务院常务会议确定,加快清洁油品生产供应,力争提前完成成品油质量升级任务,清洁汽油添加剂异辛烷(C8H18),能改善油品质量,促进汽油燃烧,大幅减少车辆污染物排放,有效保护大气环境.请计算:
(1)异辛烷的相对分子质量
(2)异辛烷中碳、氢元素质量比
(3)异辛烷中碳元素的质量分数(保留一位小数)
(4)10吨的异辛烷中含碳元素的质量.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质(不含结晶水)的溶解度曲线如下图所示.下列说法正确的是( ) 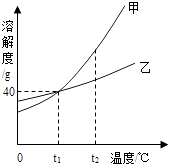
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时,甲、乙两物质的溶解度相等,均为40g
C.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
D.甲的溶解度受温度影响较小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸铜在纺织、印刷等行业有广泛用途.
(1)工业上可用铜屑、空气与稀硫酸在80℃条件下制备硫酸铜. 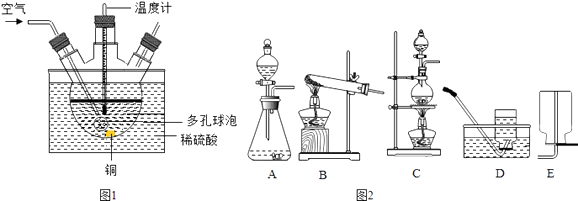
①如图1是实验室模拟工业制备硫酸铜的装置.反应的化学方程式为 , 采用水浴加热的优点是 , 多孔球泡的作用为 .
②工业生产时可用纯氧代替空气.这一措施能加快反应速率外,还具有的优点是③实验室用H2O2溶液和MnO2制备O2 , 反应的化学方程式为 , 在图2中,应选用的发生装置为(填序号,下同),收集装置为 .
(2)以CuSO4为原料制备碱式碳酸铜[Cu2(OH)2CO3]的过程如图3: 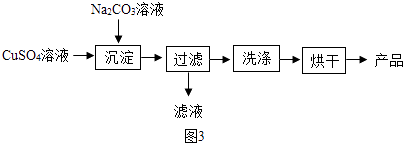
①“沉淀”时的反应为:2CuSO4+2Na2CO3+H2O=Cu2(OH)2CO3↓+2+CO2↑
②检验沉淀是否洗涤干净选用的试剂是(填化学式),烘干时产品中出现少量黑色物质,可能的原因为 .
③若所得产品的产率(产率= ![]() ×100%)偏高,其可能的原因为(填序号)
×100%)偏高,其可能的原因为(填序号)
a.反应物为完全沉淀 b.过滤时滤纸破损
c.Cu2(OH)2CO3未洗涤干净 d.Cu2(OH)2CO3为完全烘干
④“沉淀”时若有少量5Cu(OH)22CuCO3生成,则产品中铜元素的质量分数(填“偏大”“不变”或“偏小”)
(3)T℃时加热32.0g硫酸铜,一段时间后得到15.2gCuO和Cu2O的混合物,计算该混合物中CuO的质量(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示,下列说法正确的是( ) 
A.X的值为22
B.该反应属于置换反应
C.W由碳、氢两种元素组成
D.W中碳、氢元素原子个数比为1:4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D四种物质之间的一步转化关系如图所示(部分反应物、生成物及反应条件围标出),它们均含有同种金属元素.A是大理石的主要成分,B是氧化物,C为碱、D由两种元素组成.下列判断错误的是( ) 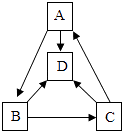
A.A的化学式为CaCO3
B.D物质不属于盐
C.表中未涉及的基本反应类型是置换反应
D.B→C的化学方程式为CaO+H2O═Ca(OH)2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用高锰酸钾制取氧气的主要步骤有:①装药品;②检查装置气密性;③固定装置;④加热;⑤收集气体;⑥撤酒精灯;⑦从水槽中撤出导管。正确的操作顺序为
A.②①③④⑤⑥⑦ B.②①③④⑤⑦⑥
C.①②③④⑤⑦⑥ D.①②③④⑤⑥⑦
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,某同学设计了如下实验方案: 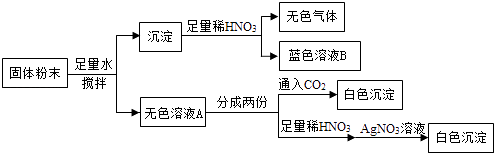 下列判断正确的是( )
下列判断正确的是( )
A.蓝色溶液B中阳离子只有Cu2+
B.无色溶液A中一定有NaOH
C.原固体粉末一定有NaCl
D.原固体粉末一定有CaCO3、NaOH、NaNO3、CuCl2和Ca(NO3)2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业炼铁.
(1)工业炼铁的主要设备是;
(2)工业炼铁的原料包括(填字母):
A.焦炭
B.铁矿石
C.烧碱
D.热空气
(3)下列矿石主要成分为Fe3O4的是(填字母):
A.赤铁矿
B.磁铁矿
C.黄铁矿
(4)写出CO与Fe2O3反应方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com