
【题目】某化学兴趣小组的同学欲在常温、常压下,用一定质量的镁与足量的稀硫酸反应,测定镁的相对原子质量。利用如图所示的装置(盛放镁条的隔板有小孔,图中固定装置已略去)进行实验,充分反应后,测得生成氢气的体积为 V.已知本实验条件下,氢气的密度为ρ。
关于该实验,有如下说法:①连接仪器后,要先检查装置的气密性;②打开分液漏斗的活塞,可观察到乙中稀硫酸进入装置丙中;③装置中的空气对实验结果无影响;④当丙中无气泡产生,冷却至室温后读取量筒戊中水的积,即为反应生成氢气的体积;⑤利用该实验原理,还可以测定铜的相对原子质量。其中正确说法是( )

A. ①②③④B. ①②④C. ①④⑤D. ②③⑤
科目:初中化学 来源: 题型:
【题目】在已平衡的天平两边分别放一个等质量的烧杯,烧杯中装有等质量、等质量分数的足量稀盐酸,在左边烧杯中加入5.6g金属铁,在右边烧杯中加入5.5g镁和铜的混合物,充分反应后天平仍然保持平衡,则右边烧杯中加入的混合物中镁和铜的质量比为( )
A. 36:19 B. 12:43 C. 24:31 D. 13:42
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D四种纯净物之间存在如图所示的转化关系,其中A和B的组成元素相同,C是空气中含量较多,且具有氧化性的一种气体单质。“→”表示相连的物质之间可以转化。请回答。
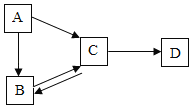
(1)A→C反应的文字表达式为_____。
(2)B→C的化学反应基本类型是_____。
(3)D的化学式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中的①和②是氟元素和钙元素在元素周期表中的信息,A、B、C、D是4种粒子的结构示意图。请完成下列空白。

(1)钙元素的相对原子质量为_______,氟元素的原子序数为_______;D中的x为_______。
(2)①和②是不同种元素,它们的最本质的区别是_______________________________。
(3)A、B、C、D结构示意图中,属于同种元素的粒子是_______(填字母)。
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似_______(填字母)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】掌握化学仪器的用途和特征,从下面的仪器中的序号或字母填空:
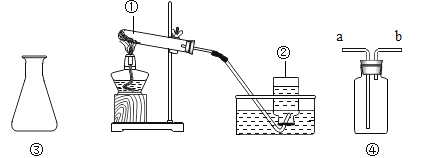
(1)可以直接在酒精灯上加热的仪器是_____;
(2)固体和液体可以反应的仪器是_____;
(3)可以收集气体的装置是_____,如果收集密度比空气大的气体先从_____入,在从_____出。如果收集密度比空气小的气体先从_____入,从_____出。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下:
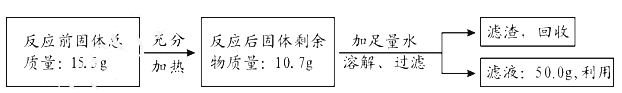
请回答下列问题:
(1)滤液可作化肥使用,你认为它属于_______肥。
(2)该同学制得氧气的质量_______g。
(3)计算滤液中溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为电解水的装置,据实验的有关现象回答:
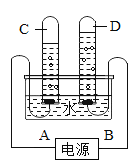
(1)A为电源的_____极(填正或负),D管中气体的检验方法是用_____来检验。
(2)C管中气体与D管中气体体积比为_____,质量比为_____(如D管中气体的密度是C管中气体密度的16倍)。
(3)由实验得出水是由_____组成的。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸钠广泛用于造纸、纺织、玻璃、洗涤剂、肥皂、制革等工业,是一种重要的化工原料。吕布兰、索尔维和侯德榜为碳酸钠的工业化生产作出了巨大贡献。
I、吕布兰法
1789年,法国医生吕布兰 (N.Leblanc,1742﹣1806)以食盐、浓硫酸、木炭和石灰石为原料,开创了规模化工业制取碳酸钠的先河,具体流程如图:
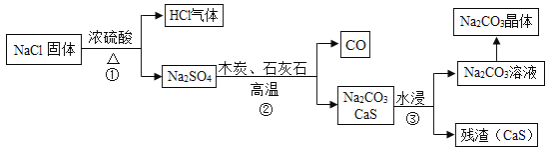
(1)碳酸钠俗称_____。
(2)在高温条件下,②中发生两步反应,其中一步是Na2SO4和木炭生成Na2S和CO,该反应的化学方程式为 ___________。
(3)③中“水浸”时通常需要搅拌,其目的是________。
(4)不断有科学家对吕布兰法进行改进,是因为此法有明显不足,请写出一条不足之处______。
Ⅱ、索尔维法
1892年,比利时工程师索尔维发明氨碱法制碳酸钠,又称索尔维法。原理如下:
NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl
2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
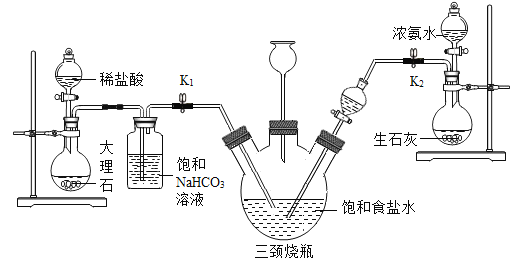
实验操作如下:
①关闭K1,打开K2通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②待三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
剩余固体质量/g | 未记录 | 15.3 | 13.7 | 11.9 | 10.6 | 10.6 |
请回答下列问题:
(5)饱和NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为_____;
(6)三颈烧瓶上连接的长颈漏斗的主要作用是_____
(7)①根据实验记录,计算t2时 NaHCO3固体的分解率 (已分解的 NaHCO3质量与加热前原NaHCO3质量的比值),请写出计算过程_________。
②若加热前NaHCO3固体中还存在少量NaCl,上述计算结果将_____ (填“偏大”、“偏小或“无影响”)。
(8)制碱技术在很长一段时间内把持在英、法等西方国家手中,我国化学工程专家侯德榜先生独立摸索出索尔维法并公布与众,又于1943年创造性地将制碱与制氨两种工艺联合起来,基本消除废弃物的排放,同时生产出碳酸钠和氯化铵两种产品,这就是著名的侯氏制碱法。下列认识或理解正确的是_____
①科学认识是在曲折的、艰辛的积累过程中不断进步的;
②“科技兴邦、实业救国”是侯德榜先生回国研究的巨大动力;
③侯氏制碱法大大提高了原料的利用率,它符合当今“绿色化学”的理念。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在2014年索契冬季奥运会上,中国运动员共获得了九枚奖牌,成为亚洲体坛霸主。
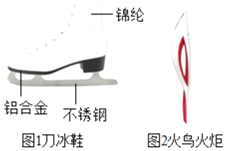
①图1是速度滑冰运动员使用的刀冰鞋,刀冰鞋中含有的金属单质是______(写化学式)。制造刀冰鞋的铝合金材料具有较好的抗腐蚀性,请用化学方程式表示铝在空气中与氧气反应生成致密的氧化膜的过程______。
②图2是2014年索契冬奥会的火炬,火炬外形像神话传说中的火鸟,采集圣火,在太阳光下将火炬燃料喷口伸向凹面镜焦点位置,打开阀门,火炬将被点燃,将燃料喷向凹面镜焦点位置的目的是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com