
【题目】水是人类宝贵的自然资源
(1)为迎接今年9月在天津举行的全运会,市民们积极为“美丽天津,绿色全运”做贡献.琳琳同学对海河的水样进行了相关研究.
①可以采用_____来测定海河水的酸碱度.
②自制简易净水器净化海河水,其中活性炭起到_____和过滤的作用.
③日常生活中为了降低水的硬度,常采用的方法是_____.
(2)二氧化氯(ClO2)可用作自来水的消毒剂,工业上用氯酸钠(NaClO4)和盐酸反应制取二氧化氯,其反应的化学方程式为:2NaClO3+4HCl═2ClO2↑+Cl2↑+2X+2NaCl.其中X的化学式为____;二氧化氯中氯元素的化合价为_____.
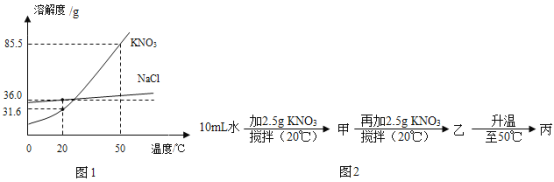
(3)如图为NaCl、KNO3的溶解度曲线(水的密度约为1g/cm3).
①20℃时,KNO3的溶解度是_____.
②茜茜同学利用溶解度曲线进行了图2实验:甲、乙、丙中为饱和溶液的是___(选填“甲”、“乙”或“丙”),甲的溶质的质量分数为___,若将甲溶液稀释到5%,则需加水的质量为___g.
③欲除去KNO3固体中混有的少量NaCl,提纯的方法为_____.
④若将50℃时NaCl、KNO3两种物质的饱和溶液冷却至20℃,该过程中保持不变的是_____(填序号)
A 溶质的质量 B 溶剂的质量 C 溶质的质量分数 D 物质的溶解度
【答案】PH试纸 吸附 煮沸 H2O +4 31.6g 乙 20% 37.5 降温结晶 B
【解析】
(1)①可以采用PH试纸来测定海河水的酸碱度;②根据活性炭有吸附和过滤的作用;③降低水的硬度的方法是:在生活中是加热煮沸,在实验室中是蒸馏;
(2)根据质量守恒定律,等号两边各原子的种类和数目相等分析,根据在二氧化氯中氯元素与氧元素的化合价代数和为零分析;
(3)根据溶解度曲线可知:硝酸钾和氯化钠两种固体物质的溶解度,都是随温度升高而增大,而硝酸钾的溶解度随温度的升高变化比氯化钠大分析;
①观察图像,20℃时,KNO3的溶解度是31.6g;
②根据溶质的质量分数公式计算;
③欲除去KNO3固体中混有的少量NaCl,提纯的方法为降温结晶;
④若将饱和溶液冷却,该过程中保持不变的是溶剂的质量。
(1)根据题目信息可知:可以采用PH试纸来测定海河水的酸碱度,自制简易净水器净化海河水,其中活性炭起到吸附和过滤的作用;降低水的硬度的方法是:在生活中是加热煮沸,在实验室中是蒸馏;故答案为:①PH试纸;②吸附;③煮沸;
(2)根据质量守恒定律,等号两边各原子的种类和数目相等,![]() ,X中有两个H原子和一个O原子;二氧化氯中氯元素的化合价为+4价,因为氧元素的化合价是﹣2价;故答案为:H2O;+4;
,X中有两个H原子和一个O原子;二氧化氯中氯元素的化合价为+4价,因为氧元素的化合价是﹣2价;故答案为:H2O;+4;
(3)20℃时,KNO3的溶解度是31.6g;图2中,甲、乙、丙中为饱和溶液的是乙,并且固体有剩余;水的密度约为1g/cm3,因此水的质量=10mL×1g/mL=10g,甲的溶质的质量分数=![]() =20%;若将甲溶液稀释到5%,则需加水的质量为x,(12.5g+x)×5%=2.5g,x=37.5g;欲除去KNO3固体中混有的少量NaCl,提纯的方法为降温结晶,因为硝酸钾的溶解度受温度的影响比氯化钠大;若将50℃时NaCl、KNO3两种物质的饱和溶液冷却至20℃,该过程中保持不变的是溶剂的质量故答案为:①31.6g;②乙;20%;37.5;③降温结晶;④B;
=20%;若将甲溶液稀释到5%,则需加水的质量为x,(12.5g+x)×5%=2.5g,x=37.5g;欲除去KNO3固体中混有的少量NaCl,提纯的方法为降温结晶,因为硝酸钾的溶解度受温度的影响比氯化钠大;若将50℃时NaCl、KNO3两种物质的饱和溶液冷却至20℃,该过程中保持不变的是溶剂的质量故答案为:①31.6g;②乙;20%;37.5;③降温结晶;④B;


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:初中化学 来源: 题型:
【题目】A-H图是实验室常用来制取气体的装置。

(1)仪器a的名称是______。
(2)利用过氧化氢和二氧化锰制取![]() 发生装置应选仪器______(填序号),反应方程式是______。
发生装置应选仪器______(填序号),反应方程式是______。
(3)用CO还原铁矿石应选用的仪器是______(填序号),加热前应先______,然后用酒精灯加热,实验结束应先______再______。
(4)I图为同学某利用废弃材料设计的家庭小实验,该装置右边部分相当于图A-H中的仪器______(填序号)组合,发生反应的化学方程式是______,该实验左边部分在操作上的优点是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室制取氧气或二氧化碳时经常用到的装置,请回答有关问题。

① 写出仪器a的名称: ;
② 实验室用氯酸钾制取干燥的氧气时,可选用的收集装置是 (填编号) ;
③ 装置B可以用来制取氢气,实验室用锌和稀硫酸制取氢气的反应化学方程式是 ,该反应属于 (填化学反应基本类型);
④ 实验室制取二氧化碳气体时,为了控制反应的发生和停止,可选用下图中的 装置(填编号),选用该发生装置制取气体需满足的一般条件是

⑤ 实验室制取二氧化碳时,所用大理石与100g稀盐酸恰好完全反应(杂质不参与反应),生成8.8g二氧化碳,求大理石中所含碳酸钙的物质的量为 mol?(根据化学方程式列式计算)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种物质的溶解度曲线,据图回答:
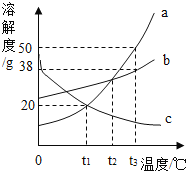
(1)t1℃时a、b、c三种物质的溶解度由大到小的顺序是______(填写序号,下同).
(2)若要将c的饱和溶液变为不饱和溶液,可以采用的方法是 ______ 、____
(3)将t3℃时a、b、c三种物质饱和溶液的温度降低到t1℃时,三种溶液的溶质质量分数大小关系是____________
(4)t2℃时,a和b两种溶液的溶质质量分数 ______________(填”一定“或“不一定”)相等。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是( )
A.质量和质量分数均相等的氢氧化钠溶液与稀硫酸充分反应,所得溶液呈酸性
B.等质量的二氧化硫和三氧化硫,二氧化硫和三氧化硫中硫元素的质量比为4:5
C.硝酸镁样品(含有一种杂质)14.8g,溶于水,与足量的NaOH溶液充分反应生成沉淀5.5g,则样品中可能含有的杂质是MgSO4
D.向一定量的氧化铁与氧化铜的混合物中加入100g质量分数为9.8%稀硫酸,恰好完全反应,则原混合物中氧元素的质量是1.6g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某纯碱样品(含少量氯化钠和13%的不溶性杂质,杂质不参加化学反应)中碳酸钠的含量,取50g样品放入烧杯中,加入137.7g水充分溶解,再向烧杯中加入300g稀盐酸,恰好完全反应,经测定.烧杯内物质的总质量为474.5g(产生的气体全部逸出)请计算:
(1)生成二氧化碳的质量_____;
(2)纯碱样品的质量分数_____;
(3)反应后所得溶液中溶质质量分数_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将100g含有少量碳酸钾的氯化钾样品加入50g盐酸中完全反应且溶解,气体全部逸出,得到145.6g溶液.则:
(1)产生的气体质量为________g.
(2)样品中氯化钾的质量分数_______;
(3)所得溶液中溶质质量分数_______(计算结果精确到0.1%).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常利用下图部分装置制取氧气。
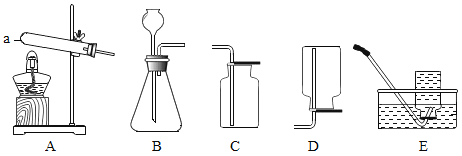
(1)仪器a的名称是_____。
(2)实验室用A装置制备氧气时,反应的化学方程式为_____。
(3)为了获得较干燥的氧气,应选用的收集装置是____(填字母序号)。验满的方法是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取气体时需要的一些装置如图所示,请回答下列问题:
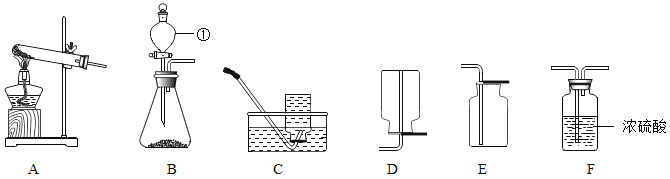
(1)写出标有序号的仪器名称:①_____。
(2)实验室制取氧气和二氧化碳的发生装置都可选用B装置的原因是_____,其中实验室制O2的化学方程式为_____。
(3)若要制取并收集到干燥的氧气,所选择装置的连接顺序为:_____(填字母序号)。
(4)若B装置用于实验室制取二氧化碳,则反应的化学方程式为_____。
(5)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,甲烷密度比空气小,难溶于水,收集装置可以选择_____(填字母序号,一种即可);请写出甲烷完全燃烧的化学方程式_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com