
【题目】25℃时,探究某固体物质的溶解性,实验记录如下表。下列实验结论正确的是
编号 | ① | ② | ③ | ④ |
水的质量/g | 50 | 50 | 50 | 50 |
加入固体质量/g | 5 | 10 | 15 | 20 |
充分溶解后 | 固体完全溶解 | 固体完全溶解 | 剩余少量固体 | 剩余较多固体 |
A.实验①所得溶液溶质质量分数为10%B.实验说明25℃时该物质的溶解度是20
C.实验③④所得溶液溶质质量分数相同D.实验④所得溶液中含溶质20g
科目:初中化学 来源: 题型:
【题目】请结合图回答问题:
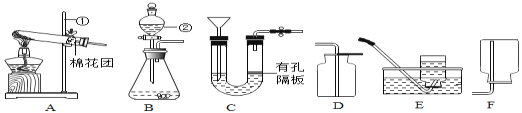
(1)仪器名称:①_________,②__________。
(2)用高锰酸钾制取氧气,可选用的发生装置是_____(选填序号),该反应的化学方程式为_______。用E装置收集氧气完毕后,应先____(选填“a从水中取出导气管”或“b熄灭酒精灯”)。
(3)实验室制取CO2,反应的化学方程式为_________,为方便控制反应的发生和停止,应选择的发生装置是__________(选填序号)。
(4)实验室制备H2 的原料可用__________和稀盐酸,该反应的化学方程式为______。为了控制反应的速度和制得较为纯净的氢气,应选择的发生和收集装置的组合是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C是初中化学中常见物质,A、B都是纯净物,且两种物质由相同的元素组成,C为气体单质,能使带余烬的木条复燃,它们之间有如图2-3-7所示的转化关系(反应条件和部分反应物已略去),请推断并回答:
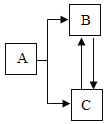
(1)物质A是(物质名称):A_____,B_____,C_____。
(2)写出A生产B和C的方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学家侯德榜在1926年生产出纯度为99%的“红三角”牌纯碱(Na2CO3),为世界制碱工业作出突出的贡献。化学小组用氯化钡(BaCl2)溶液测定某纯碱样品纯度,有关化学反应(杂质不参与反应)原理为Na2CO3 + BaCl2 = BaCO3↓+ 2NaCl 。若该纯碱样品质量2.15 g,充分反应后产生的BaCO3质量为3.94 g。求:
(1)参加反应的Na2CO3的质量_____。
(2)该纯碱样品的纯度为多少?_____(结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】十三五期间,烟台将建设大型海水淡化厂,下图是某设计院设计的综合利用海水的流程图。据图回答问题:
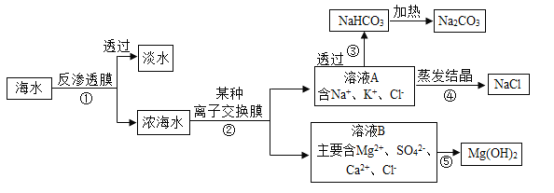
(1)反渗透膜法与滤纸过滤法在原理上都是利用混合体系中各物质的__________不同进行分离的方法。离子交换膜是对特定离子的选择性透过膜,可以使带特定电量的离子透过过程②中“某种离子交换膜”选择透过的离子特点是________。
(2)过程③是氨碱法制纯碱的一个流程,其中碳酸氢钠属于_______(填“酸”、“碱”或“盐”)。
(3)过程④采用蒸发结晶的方法,而不采用冷却热饱和溶液方法,原因是________,实验室在加热蒸发结晶过程中,当蒸发皿_______时,停止加热。
(4)浓海水中SO42-、Ca2+、Mg2+可用离子交换膜直接除去,若用化学沉淀法依次除去SO42-、Ca2+、Mg2+,需要的三种离子分别是_______(写离子符号)。
(5)若有溶质质量分数为10%的氯化钠不饱和溶液100kg,要将其变成20℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法_______。(已知:20℃时氯化钠的溶解度为36g.)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明同学想在实验室完成模拟炼铁的实验,设计下图①→④的思路。已知方框内是初中常见气体制取的发生装置,可供选择的装置见图A或B,提供选择的药品是:氯酸钾晶体、过氧化氢溶液、二氧化锰粉末、稀盐酸、块状石灰石

(1)写出图中标号a、b、c的仪器名称: a是______,b是_______,c是_______;
(2)若用A装置放入①方框内,则X是氧气,写出生成氧气的化学方程式_______;
(3)若用B装置放入①方框内,且能控制反应发生与停止,则X气体______(填能或不能)是氧气,写出生成X气体的化学方程式_____;
(4)③中玻璃管内固体由____色逐渐变成___色,说明氧化铁与一氧化碳反应生成了铁,该化学方程式为______,该反应______(填属于或不属于)置换反应;
(5)④中试管内出现白色浑浊,该化学方程式为_____;④中尾气处理的化学方程式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某硫酸铵(NH4)2SO4 样品(含有少量NH4Cl),为了测定硫酸铵样品中硫酸铵的质量分数,取样品16.0g,加入40.0g水中完全溶解后,向溶液中加入某种质量分数的氯化钡溶液,实验中精确测得产生白色沉淀的质量与加入氯化钡溶液的质量的关系如图所示。试计算:
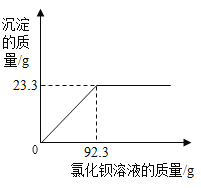
(1)硫酸铵中氢和氧元素的质量比为多少______?
(2)样品中硫酸铵的质量分数是多少______?
(3)当恰好反应时,所得溶液中溶质的质量分数是多少______?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】被誉为“中国天眼”的FAST,是目前世界上最大单口径、最灵敏的射电望远镜,2016年9月在贵州落成。如图所示。请回答下列问题:

(1)选择角钢而不用纯铁做塔架的主要原因是________;
(2)角钢中含有锰(Mn)和硅,锰可以与稀盐酸反应,生成锰的化合物中锰元素显+2价。请写出锰与稀盐酸反应的化学方程式:__________________;
(3)请你写出一条防止铁制材料生锈的具体措施:______。铝有很好的抗腐蚀性,是因为铝在空气中易与氧气反应生成致密的__________(填化学式)薄膜。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组探究气体的制备方法。
[实验可用药品探究]
(1)制取氧气时,甲同学提出,必须要用含有氧元素的物质才有可能制取氧气。他依据的原理是____ 定律
(2)工业上一般选用空气为原料制取氧气,这种方法的优点是___________________。 由于需要高压和低温条件,这种方法不适合于实验室制取氧气。
(3)下列方法中,适合实验室制取氧气的是____________;
①电解水
②加热高锰酸钾
③加热氯酸钾和二氧化锰
④用过氧化氢溶液和二氧化锰
⑤加热氧化汞
(4)[催化剂和催化作用探究]
[探究一] 影响过氧化氢分解速率的因素有哪些?小组同学做了四个实验,实验数据如下:
实验序号 | H2O2溶液的溶质质量的分数% | H2O2溶液的体积/mL | 温度/°C | MnO2的用量/g | 收集O2的体积/mL | 反应时间 |
① | 5 | 1 | 20 | 0.1 | 4 | 16s |
② | 15 | 1 | 20 | 0.1 | 4 | 6s |
③ | 30 | 5 | 35 | 0 | 4 | 98min |
④ | 30 | 5 | 55 | 0 | 4 | 20min |
③④两组实验对比可知:____________________________;
(5)能说明过氧化氢的分解速率与其质量分数有关的实验是____ ( 填实验序号)。
(6) [探究二] 其他金属氧化物能否起到类似MnO2的催化作用?实验方案如下:
I. 用MnO2、CuO、 Fe2O3、 Cr2O3 四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
Ⅱ.取30粒含MnO2的海藻酸钠微球,采用下图装置进行实验。改用其他三种微球,分别重复上述实验,得到下图的锥形瓶内压强随时间变化的曲线图。
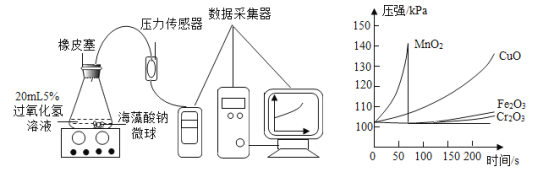
用含MnO2的海藻酸钠微球进行实验, 60 s时压强瞬间回落,其原因是______
A MnO2被反应完
B 开始实验时装置气密性不好
C 橡胶塞被气体冲出
D 数据采集器的电源被切断
(7)从实验曲线看,催化效果较好、反应温和的催化剂是____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com