
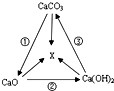
 氢氧化钠与氢氧化钙是初中化学最常见的两种碱,根据你所学知识回答:
氢氧化钠与氢氧化钙是初中化学最常见的两种碱,根据你所学知识回答:分析 (1)根据氢氧化钠和二氧化碳反应生成碳酸钠和水,酚酞遇碱变红色进行分析;
(2)根据氢氧化钠、氢氧化钙都显碱性,都能是指示剂变色,二氧化碳能使澄清石灰水变浑浊,碳酸钠会与氢氧化钙生成碳酸钙沉淀进行分析;
(3)根据氢氧化钙可以用来改良酸性土壤,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,碳酸钙和盐酸反应胡思陈二氧化碳气体进行分析.
解答 解:(1)氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:CO2+2NaOH=Na2CO3+H2O,酚酞遇碱变红色,所以不能用酚酞试液检验NaOH是否变质,理由是:氢氧化钠、碳酸钠都显碱性,都能是酚酞变红色;
(2)氢氧化钠、氢氧化钙都显碱性,都能是指示剂变色,二氧化碳能使澄清石灰水变浑浊,碳酸钠会与氢氧化钙生成碳酸钙沉淀,故选:AC;
(3)氢氧化钙可以用来改良酸性土壤,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,碳酸钙和盐酸反应胡思陈二氧化碳气体,所以取样,加入稀盐酸,观察到固体逐渐溶解,有气泡产生,证明样品中含有石灰石.
故答案为:(1)CO2+2NaOH=Na2CO3+H2O,氢氧化钠、碳酸钠都显碱性,都能是酚酞变红色;
(2)AC;
(3)改良酸性土壤,CaCO3+2HCl=CaCl2+H2O+CO2↑,有气泡产生.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.


科目:初中化学 来源: 题型:实验探究题
| 气体 | X | Y | 二氧化碳 | 水蒸气 |
| 吸入气体 | 78.25% | 21.05% | 0.04% | 0.66% |
| 呼出气体 | 74.88% | 15.26% | 3.68% | 6.18% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 控制变量法是常用的化学学习方法.下面是探究燃烧条件的实验,请你根据图示信息和资料信息回答有关问题.
控制变量法是常用的化学学习方法.下面是探究燃烧条件的实验,请你根据图示信息和资料信息回答有关问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 温度 | 溶解度(g) | ||
| A | B | C | |
| 20 | 16 | 20 | 40 |
| 40 | 30 | 25 | 30 |
| 60 | 53.5 | 30 | 20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com