
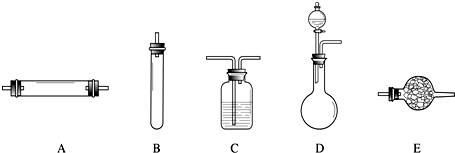
分析 (1)根据反应物状态和反应条件选择发生装置,对比原料及生产过程分析生石灰的作用:生石灰和水反应生成熟石灰,一方面消耗氨水中的水,另一方面放出的热量促使氨水挥发、分解而得到氨气;
(2)根据实验的要求要除去空气中多余的水蒸气、二氧化碳等杂质,可以通过碱性干燥剂完成;
(3)根据反应物及题目的信息结合元素守恒判断生成物写出化学方程式;
(4)根据绿色化学的定义结合反应的原理对比分析优点;
(5)根据方法二得到的氮气不纯进行考虑.
解答 解:(1)用CaO和浓氨水反应,应选固液常温型的发生装置,即D;浓氨水常温下跟生石灰反应生成氨气和氢氧化钙,化学方程式为CaO+NH3•H2O=NH3↑+Ca(OH)2,因为氨水不稳定易挥发,生石灰和水反应生成熟石灰的过程中,生石灰的两个作用是:一方面消耗氨水溶液中的水,另一方面放出的热量促使氨水挥发、分解而得到氨气;
(2)空气中除了氮气、氧气外,还含有二氧化碳、水蒸气等,为保证所得氨气尽可能纯净,要除去空气中多余的水蒸气、二氧化碳等杂质,可以通过碱性干燥剂-碱石灰,既可以吸收二氧化碳又能吸收水;
(3)根据信息反应物是亚硝酸钠(NaNO2)和氯化铵,反应条件是加热,氮元素全部转化为氮气,反应前后元素的种类不变,因此生成物还有氯化钠和水,化学方程式为:NaNO2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+N2↑+2H2O;
(4)从题中信息可知,NH3和CuO生成Cu和N2 而空气和Cu生成CuO,故Cu和CuO可以循环使用,方法三使用有毒的亚硝酸钠,方法一和二避免使用有毒物质而造成污染,因此联合使用方法一和方法二与单独使用方法三相比的优点有:铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染);(5)将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末只是除去了氧气,其中还含有稀有气体等杂质,由于稀有气体的密度比氮气密度大,所以导致氮气密度总是偏大5‰左右.
故答案为:(1)D; 生石灰和水反应放热,促使氨水挥发、分解而得到氨气(或降低氨气的溶解度);生石灰与水反应,减少了溶剂;
(2)E,碱石灰;
(3)NaNO2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+N2↑+2H2O;
(4)铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染);
(5)方法二制得的氮气中含有密度(或相对分子质量)比氮气大的稀有气体,导致密度偏大.
点评 本题是一信息题,考查学生的知识拓展迁移能力,要求学生有良好的分析能力,能会从题干信息中找突破口,根据信息将学过的知识进行迁移.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 混合物的分离 | 分离物质的原理 |
| A. | 分离制氧气后剩余固体中的二氧化锰和氯化钾 | 二氧化锰和氯化钾的溶解性不同 |
| B. | 将石油加热炼制得到汽油、煤油、柴油等产品 | 石油中各成分的沸点不同 |
| C. | 分离硝酸钾和氯化钠组成的混合物 | 溶解度受温度影响不同 |
| D. | 分离液态空气制取氧气 | 利用氮气和氧气的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
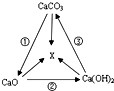 氢氧化钠与氢氧化钙是初中化学最常见的两种碱,根据你所学知识回答:
氢氧化钠与氢氧化钙是初中化学最常见的两种碱,根据你所学知识回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 农民就地焚烧秸秆 | |
| B. | 深埋含镉、汞的废旧电池 | |
| C. | 工业制酒精C2H4+H2O$\frac{\underline{\;催化剂\;}}{\;}$C2H6O | |
| D. | 化工生产中的废气向高空排放 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com