
【题目】食醋是厨房中常用的调味品,它的主要成分是乙酸, 乙酸分子的模型如图所示,其中![]() 代表一个碳原子,
代表一个碳原子,![]() 代表一个氢原子,
代表一个氢原子,![]() 代表一个氧原子。
代表一个氧原子。
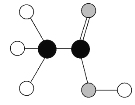
(1)乙酸中碳元素、氢元素、氧元素的质量比是___。
(2)乙酸的相对分子质量为_____。
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案 培优三好生系列答案
培优三好生系列答案科目:初中化学 来源: 题型:
【题目】碳元素是组成许多物质的基本元素。
(1)下列物质的主要成分中(括号所示为主要成分的化学式),能与鸡蛋壳的主要成分反应的是______(填字母序号)。
A  食醋(CH3COOH)
食醋(CH3COOH)
B  食用纯碱(Na2CO3)
食用纯碱(Na2CO3)
C  味精(C5H8NO4Na)
味精(C5H8NO4Na)
(2)化石燃料包括煤、石油和天然气,其中天然气充分燃烧的化学方程式为___________________。
(3)二氧化碳可用于制化肥尿素[CO(NH2)2],其反应的微观示意图如下:
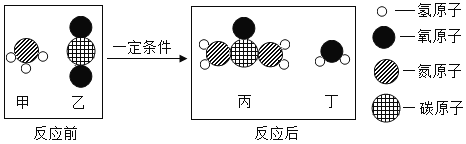
生产尿素的反应中,丙与丁的质量比为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】按下列要求完成化学方程式
(1)木炭在氧气中燃烧______。
(2)过氧化氢溶液与二氧化锰混合______。
(3)氢氧化钠和硫酸溶液反应______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】春节期间我国爆发了新冠肺炎疫情,为了做好疫情防控,公共场所常用“84”消毒液或75%酒精溶液消毒杀菌。
(1)“84”消毒液:主要成分是次氯酸钠(NaClO),其中Cl元素的化合价是_______,它是由2NaOH+Cl2=NaClO+X+H2O反应制得,其中X的化学式是_______。
(2)酒精(C2H5OH):物质分类中属于_______(填“有机物”或“无机物”),其中碳、氢原子物质的量之比是_______,23g酒精中约含_______个氢原子。溶质质量分数为75%消毒酒精中“75%”的含义是_______。
(3)下图是酒精完全燃烧的微观示意图。

酒精燃烧的化学方程式是_______。
已知:“![]() ”的相对原子质量是“
”的相对原子质量是“![]() ”的n倍,该反应中“
”的n倍,该反应中“![]() ”和“
”和“![]() ”的质量比是_______。(用含n的式子表示)
”的质量比是_______。(用含n的式子表示)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的基本工具。按要求回答下面问题:
(1)写出2个二氧化氮分子的符号 ______;
(2)标出Fe2O3中铁元素的化合价___________;
(3)写出CH4中右下角数字“4”的意义_______ ;
(4)写出CO32-中右上角数字“2”的意义_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种物质的溶解度曲线,根据图示回答:

(1)t1℃时30gA物质加入到50g水中,充分溶解后溶质与溶剂的质量比为_______;
(2)A物质饱和溶液中混有少量B物质,可采取_______、过滤、洗涤的方法提纯物质A;
(3)将接近饱和的C溶液转变为饱和溶液,除了可以采取增加溶质的方法外,还有________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】农作物必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等.
(1)从如图可知氧原子的质子数为__,在化学反应中__(填“易得”或“易失”)电子.

(2)KNO3中N的化合价是__.
(3)写出化学符号:
①钙离子____;
②2个磷原子__;
③氨气分子__.
(4)写出草木灰(主要成分是碳酸钾)与盐酸反应的化学方程式:_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧化物、酸、碱、盐都属于化合物。甲、乙、丙、丁、M是初中化学常见的化合物。其中甲、乙、丙、丁分属上述四种不同类别的化合物,M与甲属于同种类别的化合物。它们之间的部分转化关系如图所示(部分反应物、生成物、反应条件己略去。“一”表示物质之间能发生反应,“→”表示物质之间的转化关系)。回答下列问题:

(1)若甲是碳酸钙,则可以用水鉴别乙和丙吗?请写出你判断的理由:_____。
(2)若乙是可用于改良酸性土壤的碱,甲是氧化物,则甲可以是_____(填一种物质),写出甲→M转化的化学方程式_____。
(3)若丁是氢氧化钠,则甲可以通过中和反应转化为M吗?_____(填“可以”或“不可以”);再写出氢氧化钠的一种用途:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业生产的纯碱中常含有少量氯化钠杂质,现称取12 g纯碱样品于烧杯中,加入水使其完全溶解,逐渐加入氯化钙溶液至过量,测得加入氯化钙溶液的质量与生成沉淀的关系如下图所示。(反应的化学方程式:CaCl2 + Na2CO3 == CaCO3↓+ 2NaCl)
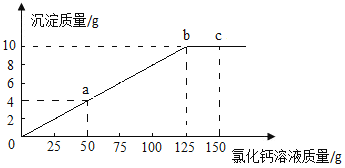
(1)计算样品中碳酸钠的质量分数(要求写出计算过程,精确到0.1%)。
(2)若要计算氯化钙溶液中溶质的质量分数,可使用上图中 点的一组数据(填标号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com