

 ��
�� ���� �ٸ��ݹ��̵ı仯Ҫ�ؽ��з�����
�ڸ��ݸ������������Ƶ����ʵ����Ͷ�Ӧ�Ļ�ѧ����ʽ����HCl�����ʵ������Ȼ��Ƶ�������
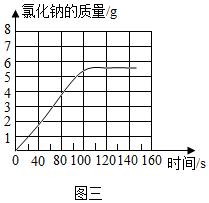
�۸��ݢڼ�����Ȼ��� �������Ƴ���Ӧ�ı仯���ߣ�
��� �⣺
��ͼ���Կ����ڹ�����pH�ɿ�ʼ�Ĵ���7���ӽ�7������7�������С��7��˵���кͷ�Ӧ����������ͬһ�����й�ע������һ���������¶ȣ��������ߺͣ�˵���кͷ�Ӧ�Ƿ��ȵģ�����Ӧ��ɺ�����������ᣬ�൱��ϡ������Һ���¶��������ͣ����������������Һ�е����������ɵ��Ȼ��ƺ�ʣ���HCl���˴�û���ر�Ҫ��д��ѧʽ�������ƾ��ɣ�
����0.1mol����������ǡ����ȫ��Ӧ��HCl�����ʵ���Ϊx�����ɵ��Ȼ��Ƶ�����Ϊy
NaOH+HCl=NaCl+H2O
1mol 1mol 58.5g
0.1mol x y
$\frac{1mol}{0.1mol}$=$\frac{1mol}{x}$=$\frac{58.5g}{y}$
x=0.1mol
y=5.85g
���Թ������Ȼ��Ƶ�������0��ʼ��������5.85g��Ȼ�������ӣ�
��ͼΪ��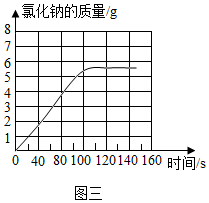
�ʴ�Ϊ��
����Һ��pH�����½�ֱ��С��7�����ȣ�NaCl��HCl��
��0.1mol��
�� ��
��
���� ������е������ʵ����������Ļ�ϼ��㣬ע�������ȷ����Ҫ��������㣮������ͬʱ�漰�����������ʵ����������ʱ�����ݺ͵�λ��Ҫ��ѭ����һ�£����Ҷ�Ӧ��


 ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д� �ݾ�ѵ������ϵ�д�
�ݾ�ѵ������ϵ�д� С����ȫ�ܼ��ϵ�д�
С����ȫ�ܼ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
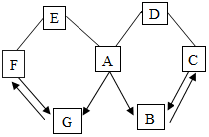 ��ͼ��ʾA��G�dz��л�ѧ�г��������ʣ�ͼ�С�������ʾת����ϵ����-����ʾ��ܷ�Ӧ����֪Aʱ����θҺ�к��е��ᣬG����������壬B��C��D��E��F���������DΪ��ɫ��ĩ����ش�
��ͼ��ʾA��G�dz��л�ѧ�г��������ʣ�ͼ�С�������ʾת����ϵ����-����ʾ��ܷ�Ӧ����֪Aʱ����θҺ�к��е��ᣬG����������壬B��C��D��E��F���������DΪ��ɫ��ĩ����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 A��B��C��D��EΪ���л�ѧ�������������ʣ�����֮�������ͼ��ʾ�Ĺ�ϵ����������ʾ���ʾ�һ����Ӧ��ת��Ϊ��һ�����ʣ���-����ʾ�����������ܷ�����ѧ��Ӧ�����ַ�Ӧ������P��Ӧ��������ȥ������ش��������⣺
A��B��C��D��EΪ���л�ѧ�������������ʣ�����֮�������ͼ��ʾ�Ĺ�ϵ����������ʾ���ʾ�һ����Ӧ��ת��Ϊ��һ�����ʣ���-����ʾ�����������ܷ�����ѧ��Ӧ�����ַ�Ӧ������P��Ӧ��������ȥ������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X�Ļ�ѧʽΪH2 | |
| B�� | ���Ļ��ϼ���0����+3 | |
| C�� | �÷�Ӧ�������ڸ��ֽⷴӦ | |
| D�� | �ɲ�������ȡCO2��ͬ�ķ���װ����ȡX |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʢ��Ũ������Լ�ƿ����ƿ�ڳ��ְ��� | |
| B�� | Ũ�����մ��Ƥ���ϣ������ô�����ˮ��ϴ��Ȼ����Ϳ��3%-5%������������Һ | |
| C�� | ʵ������ϡ����Ϳ�״ʯ��ʯ��ȡ������̼ | |
| D�� | ����������������ʡ�ũҩ��Ⱦ���Լ�ұ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO��NH2��2 | B�� | Ca��H2PO4��2 | C�� | KNO3 | D�� | NH4HCO3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com