
| ||
| ||
| 100 |
| 15g |
| 56 |
| x |


科目:初中化学 来源: 题型:
| A、稀有气体元素的原子都处于稳定结构,不易发生化学反应,故它们的化学性质比较稳定 |
| B、处于稳定结构的粒子,一定是稀有气体元素的原子 |
| C、原子核外的电子是分层排布的 |
| D、金属元素原子在反应易失去最外层电子,而非金属元素的原子的最外层则易夺取电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:
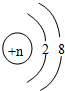 来表示阳离子、阴离子、原子,则n对应的三个数据准确的是( )
来表示阳离子、阴离子、原子,则n对应的三个数据准确的是( )| A、9、11、10 |
| B、11、9、10 |
| C、12、11、10 |
| D、12、8、10 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 元素周期表的排列体现元素性质的规律性,如:同一纵行的元素最高正价相同,同类物质化学性质相似.图示是碳、硅元素在周期表中的相对位置,回答:
元素周期表的排列体现元素性质的规律性,如:同一纵行的元素最高正价相同,同类物质化学性质相似.图示是碳、硅元素在周期表中的相对位置,回答:| 元素 | 氧化物 | 酸 | 钠盐 |
| C | CO2 | H2CO3 | Na2CO3 |
| Si | SiO2 | Na2SiO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验编号 | 实验药品 | 分解温度(℃) |
| ① | 氯酸钾 | 580 |
| ② | 氯酸钾、二氧化锰(质量比1:1) | 350 |
| ③ | 氯酸钾、氧化铜(质量比1:1) | 370 |
| ④ | 氯酸钾、三氧化二铁(质量比1:1) | 390 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com