
【题目】已知甲、乙、丙、丁分别是初中化学中常见的四种不同类别的物质,相邻两种物质可发生化学反应,生成A、B、C、D四种物质(部分生成物已略)。其中乙是应用最广的金属,丙是蓝色溶液,丁中含有钠离子,B是气体,D是不溶性碱。
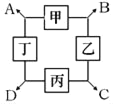
(1)写出乙的化学式_____;
(2)若C是一种盐,则其溶液的颜色为_____;
(3)甲所属的物质类型为_____(填“酸”“碱”“盐”或“氧化物”);
(4)若丙由三种元素组成,试写出丙与丁反应的化学方程式_____;
【答案】Fe 浅绿色 酸 CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
【解析】
乙是应用最广泛的金属,所以乙是铁;丙是蓝色溶液,所以丙中含有铜离子,可以是硫酸铜;丁中含有钠离子,能与丙(硫酸铜)反应生成D, D是不溶性碱,所以D是氢氧化铜,丁是氢氧化钠;乙(铁)和甲反应会生成气体B,所以甲是酸,可以是盐酸,B是氢气。
(1)由分析可知,乙为铁,其化学式是Fe,故填Fe;
(2)铁和硫酸铜反应生成硫酸亚铁和铜,C是一种盐,则C为硫酸亚铁,其溶液的颜色为浅绿色,故填浅绿色。
(3)由分析可知,甲可以是盐酸,其所属的物质类型为酸,故填酸。
(4)若丙由三种元素组成,丙与丁的反应是氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,故反应的化学方程式写为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4。


科目:初中化学 来源: 题型:
【题目】用铝土矿(主要含SiO2、Al2O3和少量Fe2O3等)制取铝硅合金材料有干法、湿法等方法,其中干法制备的工艺流程如图所示。
(已知:I.SiO2不溶于水、不与硫酸反应。Ⅱ.转化率是反应物转化为生成物的百分率。)
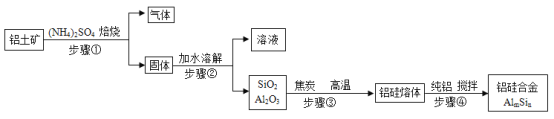
(1)铝硅合金的硬度比纯铝的硬度_______。
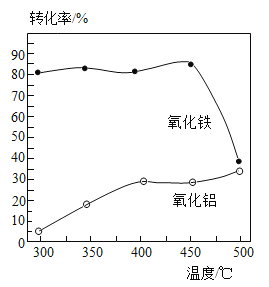
(2)步骤①中焙烧除铁的反应为:4(NH4)2SO4+Fe2O3![]() 2NH4Fe(SO4)2+3H2O+6NH3↑(Al2O3部分发生类似反应,SiO2不发生类似反应)。已知Fe2O3、Al2O3转化为硫酸盐的转化率与温度的关系如图所示,则焙烧除铁最适宜的温度为_______℃。
2NH4Fe(SO4)2+3H2O+6NH3↑(Al2O3部分发生类似反应,SiO2不发生类似反应)。已知Fe2O3、Al2O3转化为硫酸盐的转化率与温度的关系如图所示,则焙烧除铁最适宜的温度为_______℃。
(3)步骤②中包括加水溶解、_______、洗涤等操作。
(4)步骤③中利用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3.写出高温下Al4C3与Al2O3反应生成A1和CO的化学方程式:_______。
(5)若用湿法处理铝土矿,加过量的硫酸浸取,所得溶液中的阳离子有_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Na2CO3、CaCO3、KHCO3、MgCO3分别和盐酸反应,下列分析不正确的是( )
A. 当Na2CO3和CaCO3的质量相等,盐酸足量时,CaCO3生成的CO2气体质量较多
B. 当CaCO3、KHCO3、MgCO3足量,盐酸等质量等浓度时,生成CO2气体的质量相等
C. 当CaCO3和KHCO3的质量相等,盐酸足量时,生成CO2气体的质量相等
D. 当Na2CO3、CaCO3、MgCO3足量,盐酸等质量等浓度时,生成CO2气体的质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以软锰矿粉(主要含MnO2,还有少量Fe2O3)为原料制取MnCO3的流程如图1.
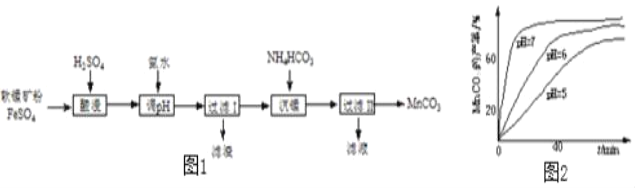
(1)“酸浸”时发生的反应有2FeSO4+MnO2+2H2SO4=_____+MnSO4+2H2O和_____。
(2)“过滤Ⅰ”所得滤渣的主要成分是_____。
(3)“沉锰”时测得MnCO3的产率与溶液pH、反应时间t的关系如图2,反应要控制pH=_____,其理由是_____、_____。
(4)“过滤Ⅱ”所得滤液中溶质的主要成分是_____。
(5)为测定某软锰矿中MnO2的质量分数,称取2.0 g软锰矿样品,加入3.35 g草酸钠(Na2C2O4)固体,再加足量稀硫酸(杂质不参加反应),充分反应后,过量的Na2C2O4用31.6 g/L KMnO4溶液进行反应,当滴入10.0 mL KMnO4溶液时恰好完全反应。
已知:①MnO2+Na2C2O4+2H2SO4=MnSO4 +2CO2↑+2H2O+Na2SO4 ;②2KMnO4+5Na2C2O4+8H2SO4=2MnSO4+5Na2SO4+K2SO4+10CO2↑+8H2O.
求该软锰矿中MnO2的质量分数。_____(相对分子质量:KMnO4 158;Na2C2O4 134;MnO2 87)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学在探究金属的有关性质时,进行了如图所示实验:在A实验结束后将两支试管内的物质倒入一洁净烧杯中,一段时间后过滤。为确定过滤后得到的滤渣和滤液的成分,同学们进行了如下实验。

实验一:滤渣的成分是什么?
(1)甲同学取少量滤渣于试管中,加入稀硫酸,无气泡产生,证明滤渣里不含_____。乙同学通过物理方法也得到了同样的结论,请简述方法和现象_____。
实验二:滤液里的溶质有哪些?
(2)同学们认为一定有硫酸亚铁,为确定可能含有的其他溶质,同学们进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
取少量滤液,向其中加入少量铁粉 | _____ | 滤液里的溶质还有硫酸和硫酸铜 |
请写出铁与硫酸铜反应的化学方程式:_____。
(3)有同学提出可以直接观察滤液的颜色判断滤液中是否含有硫酸铜,同学们对硫酸铜溶液为什么呈蓝色很感兴趣,决定探究硫酸铜溶液中哪种粒子使溶液呈蓝色。设计的实验方案如下:
实验操作 | 实验现象 | 实验结论 |
①取少量_____溶液,观察颜色 | 溶液呈无色 | 硫酸根离子不能使溶液呈蓝色 |
②取少量硫酸铜溶液,观察颜色 | 溶液呈蓝色 | 铜离子使溶液呈蓝色 |
(4)除了(3)中实验方案外,你还能设计其他方案探究硫酸铜溶液中到底是哪种粒子使溶液呈蓝色吗?实验所需的药品和仪器任选,请简述实验操作和实验现象。
实验搡作 | 实验现象 |
_____ | _____ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是由氢、氧两种元素组成的化合物。这一结论是科学家们在大量实验的基础上得出的。
(1)实验室中常用二氧化锰和双氧水反应来制备氧气。请从如图1的装置中选择并组装一套制取干燥氧气的装置,正确的连接顺序为___(用接口处字母填写)。
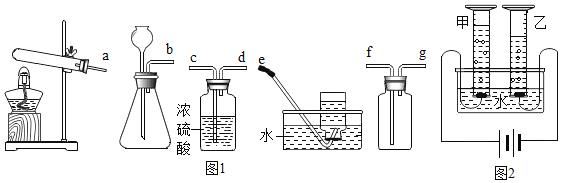
(2)研究氢气的燃烧实验是人们认识水组成的开始。
①氢气在点燃前一定要___。
②氢气在空气中燃烧时,若在火焰上方罩一冷而干燥的小烧杯,可观察到的现象是___。在相同条件下,欲使1L氢气完全燃烧,所需空气至少约为___L。
(3)科学家们又用“电解法”证明了水的组成(装置如图2所示,电极不与水及生成的气体反应)。电解时,水中需加入少量的NaOH,其作用是__。通电一段时间后,发现甲、乙两量简中收集的气体体积比略小于1:2,其原因可能是__(写出一条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】1kg不同燃料燃烧产生CO2和SO2的质量如表所示。
燃料 | 燃烧产物质量/g | |
CO2 | SO2 | |
汽油 | 2900 | 5.0 |
天然气 | 2500 | 0.1 |
煤 | 2500 | 11.0 |
①其中较清洁的燃料是______,使用______做燃料时最易形成酸雨。
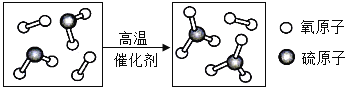
②酸雨形成过程中某一步反应的微观示意图如下图所示。则该反应的化学方程式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组对“NaOH溶液与盐酸是否恰好完全反应”进行探究,请你参与他们的探究活动,并回答有关问题。
(实验探究)
(1)方案一:甲同学按如图所示的方法先向试管中加入约2mLNaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为_____色,证明NaOH溶液与稀盐酸恰好完全反应。
![]()
①请指出如图操作中的错误_____。
②写出NaOH溶液与稀盐酸反应的化学方程式_____。
(2)方案二:乙同学按照下面的方案进行实验证明盐酸与氢氧化钠恰好完全反应。
实验步骤 | 实验现象 | 结论 |
取2mLNaOH溶液于试管中,滴入一定量的稀盐酸,再滴加无色酚酞试液,充分振荡 | 没有明显现象 | 二者恰好完全反应,溶液显中性 |
(实验反思)
①方案一在滴入稀盐酸的过程中,若观察到曾有少量气泡出现,请分析产生气泡的原因可能是_____(写出化学方程式)。
②有同学提出方案二不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是_____。为此,还需要选择_____(填一种试剂),再进行实验即可。
(3)某化学兴趣小组为了测定某工厂废水中硫酸的含量,取100g废水于烧杯中,加入80g质量分数为10%的氢氧化钠溶液,恰好完全反应(废水中无不溶物,其它成分不参与反应),请计算:废水中硫酸的质量分数。_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com