
科目: 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
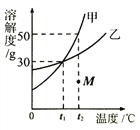
A. 将甲、乙的饱和溶液从t2℃分别降温到t1℃,析出晶体的质量甲一定大于乙
B. t1℃时甲、乙的饱和溶液中溶质质量分数相等
C. t2℃时将40g甲溶于100g水中,形成饱和溶液
D. 将M点的甲溶液变成饱和溶液常采取的方法是加水
查看答案和解析>>
科目: 来源: 题型:
【题目】某化工厂排放的废水中含有碳酸钾和氢氧化钾,化学兴趣小组为探究废水中碳酸钾的含量,提取50g废水样品于集气瓶中,逐滴加入9.8%的稀硫酸,反应过程中产生二氧化碳的质量与加入稀硫酸的质量如下图,请计算。
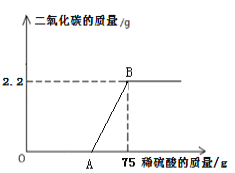
(1)生成二氧化碳的质量为 g;
(2)该废水中碳酸钾的质量分数(写出计算过程);
(3)反应后生成硫酸钾的质量为 g。
查看答案和解析>>
科目: 来源: 题型:
【题目】(9分)实验室现有氯酸钾、二氧化锰、石灰石、稀盐酸、火柴及如下图仪器: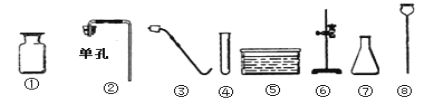
(1)仪器⑦的名称为 ;
(2)若补充一种仪器 (填名称),并利用上述部分仪器和药品可制取氧气;用排水法收集氧气时,待气泡 时,开始收集气体,制取该气体的化学方程式为 ;
(3)若要制取二氧化碳,选择的仪器为 (填序号);
(4)为检查装置的气密性,保持装置内温度不变,将导管的末端伸入装有水的烧杯中。若装置的气密性良好,烧杯内导管处的现象(画圈部分)是
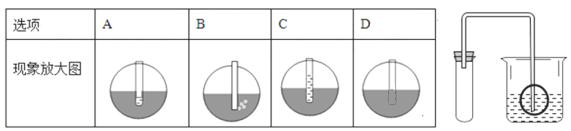
查看答案和解析>>
科目: 来源: 题型:
【题目】(8分)A~E是初中常见的物质,它们的转化关系如图所示(图中“→”代表转化关系,“——”表示相互反应)。其中A和B都属于盐,且B可用于补钙,C是氧化物,E是最常用的溶剂。请回答下列问题:
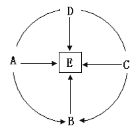
(1)物质E的化学式为 ;
(2)物质C的一种用途为 ;
(3)A与D反应的基本类型为 ;
(4)反应C→B的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为A、B、C三种固体物质的溶解度曲线,根据图示完成下列问题:

(1) ℃时,A、B两种物质的溶解度相等。
(2)t2℃时,向70gA物质中加入100g水,充分溶解后,所得溶液 (填“是”或“不是”)饱和溶液,该溶液的溶质质量分数是 ;
(3)用一定的方法,将某温度下C的不饱和溶液变为饱和溶液,下列说法正确的是 。
a.溶剂的质量可能不变
b.溶质质量分数一定变大
c.溶液的质量可能不变
d.溶质的质量一定变大
查看答案和解析>>
科目: 来源: 题型:
【题目】(7分)2014年11月1日,“嫦娥五号”T1试验器携带玉雕、音乐芯片、港式月饼等成功返回。请回答下列问题:
(1)玉雕是用玉石雕刻而成的玉器。某种玉石的主要成份是NaAlSi2O6。NaAlSi2O6中硅元素和氧元素的原子个数比为 ;硅元素的质量分数为 (精确到0.1%);
(2)音乐芯片主要是由高纯硅制成。工业上用石英(主要成分为SiO2)制备粗硅的化学方程式为:SiO2+2C![]() Si+2R↑,则R的化学式为 ;
Si+2R↑,则R的化学式为 ;
(3)港式月饼的制作常用面粉、冰糖、精炼油、火腿等物质,其中富含糖类的有 ;
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是小梅配制100g溶质质量分数为12%的NaCl溶液的实验操作示意图:
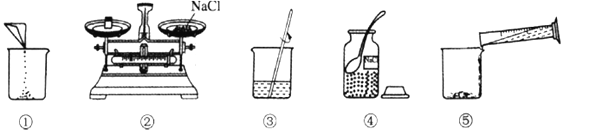
(1)上图中的玻璃仪器分别为广口瓶、量筒、烧杯和___________ 。
(2)配制时应选择_________ ml (10ml、50ml 、100ml)的量筒量取所需要的水。
(3)指出图中的一处错误操作________________________________________________
(4)用上述图示的序号表示配制溶液的操作顺序________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是A、B、C三种物质的溶解度曲线,据图回答:
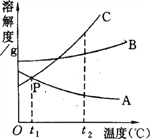
(1)P点表示t1℃时____________物质的溶解度相等。
(2)t1℃时,将一定量B的饱和溶液升温至t2℃,溶质的质量将___________(填“变大、变小”或“不变”)
(3)t2℃时,三种物质的溶解度由大到小的顺序是________________ 。
(4)t1℃时A的溶解度_________t2℃时A的溶解度;(填“大于”、“小于”或“等于”)
(5)使一定量接近饱和的A物质溶液变为饱和溶液采用的一种方法是____________________
(6)如果C中混有少量的B,想要得到纯净的C,方法是 _______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如右图所示,下列叙述正确的是
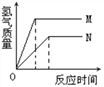
A. M、N两种金属中较活泼的是N
B. 生成H2的质量M<N
C. 相对原子质量较大的是N
D. 产生H2的速率N>M
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸是一种重要的化工原料,也是实验室中常用的化学试剂,下面是对硫酸的组成、性质、制取、用途等方面的探究,请你共同参与并回答有关问题
探究一、检测硫酸溶液中所含的离子
以下试剂能用来检测硫酸溶液中所含的阴阳离子的组合是____________(填序号)
①石蕊试液 氯化钡溶液 ②PH试纸、硝酸钡溶液 ③石蕊试液 稀盐酸、氯化钡溶液 ④硝酸钡溶液、稀硝酸 ⑤氯化钡溶液稀硝酸
探究二、硫酸的性质
由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异:
(1)探究浓硫酸的某些特征作了如下一些实验:
①用小木棍蘸取少量浓硫酸,放置一会后,可观察到________________
②兴趣小组把98%的浓硫酸10ml和63.3%的硫酸溶液(用10ml98%的浓硫酸与10ml水配成)约20ml分别放入两个相同的小烧杯中,称量、观察、记录、分析;根据室温环境下实验的数据绘成的曲线如图1;
由如图1曲线你能得到的实验结论有哪些?(写两点)_________________________
(2)浓硫酸的稀释;实验室用98%的浓硫酸(密度1.84g/cm3)配制100g溶质质量分数为20%的稀硫酸,需要水的体积为__________ml(精确到0.1);浓硫酸稀释过程如图2所示,b中盛放的物质是__________(填物质名称),a的作用是______________。
(3)探究稀硫酸的化学性质;
如图选择不同类别的物质与稀硫酸反应发生了如下颜色变化;
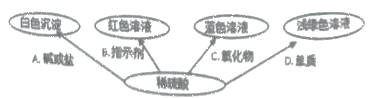
①请在编号C处填一种物质,则C是________________________________(写化学式)
②请写出B体现了稀硫酸的性质是__________________
③请写出符合编号A的一个化学反应方程式__________________
探究三、硫酸的工业制法
工业上黄铁矿为原料生产硫酸的工艺流程如图所示;
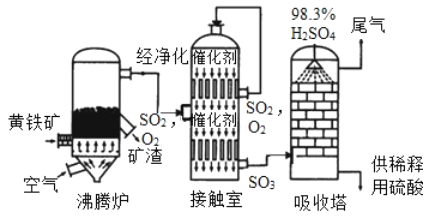
(1)接触室中发生的化学方程式为____________________________________________________ 硫酸是一种重要的化工产品,用途十分广泛,请写出稀硫酸的一种用途_____________________
(2)依据生产硫酸的工艺流程图,下列说法正确的是_____________填字母序号)
为使黄铁矿充分燃烧,需将其粉碎
催化剂能够提高SO2的反应速率和产量
吸收塔中得到的产品为混合物
沸腾炉排除的矿渣可供炼铁
(3)探究某黄铁矿中FeSO2的含量:
同学们进行了如下实验探究(假设每步反应均完全)。
【查阅资料】
①4FeS2+11O2![]() 2Fe2O3+8SO2 ②Na2SO3+H2O2=Na2SO4+H2O
2Fe2O3+8SO2 ②Na2SO3+H2O2=Na2SO4+H2O
【实验探究】
I称取1.60g黄铁矿样品放入如图所示装置(夹持装置省略)的石英管中,从a处不断地缓缓通入空气、高温灼烧石英管中的黄铁矿样品至完全反应。

II反应结束后,将乙瓶中的溶液进行如图处理
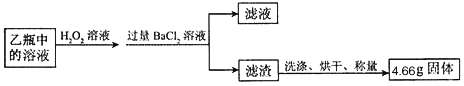
【问题讨论】
①I中装置甲瓶内盛放的试剂是氢氧化钠溶液,其作用是____________________;II中滤液所含的溶质一定有__________________________________。
【含量测定】
②II中最终得到的4.66g固体是_______填物质的化学式);
③计算该黄铁矿中FeS2的质量分数为______________;
【交流反思】
④如果缺少甲装置,则最终测得FeS2的质量分数将会__________________填“偏大”“偏小”“不变”
⑤如何证明II中所加BaCl2溶液已过量(请简要写出操作方法及现象_________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com