
科目: 来源: 题型:
【题目】有一包固体粉末,可能含有铜、氧化铁、氯化钠、硫酸钠、硫酸铜中的一种或几种,为确定其成分进行了如下实验,现象如图所示(部分生成物未标出)。
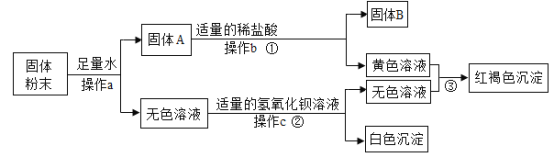
根据实验过程中的现象判断:
(1)固体B的成分是_____(填化学式);操作a、b、c为同一操作,其名称是_____,该操作需要的玻璃仪器烧杯、漏斗、_____。
(2)固体粉末中一定不含有的物质是____(填化学式,下同),可能含有的物质是_____;
(3)写出反应③的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年11月,我省“温汤佬富硒盐皮蛋”荣获首届“中国金牌旅游小吃”。如图是硒原子的结构示意图和元素周期表中的信息,请回答:
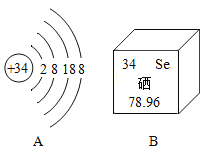
(1)硒具有防癌、抗癌作用,是人体必需的_____(填“常量”或“微量”)元素;
(2)硒原子核内有_____个质子。
(3)图A表示的粒子符号是,图B中78.96表示的是_____;
(4)市场上的加硒盐是在碘盐的基础上添加了一定量的亚硒酸钠制成的。亚硒酸钠(Na2SeO3)中硒的化合价是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】从C、H、O、Al、N五种元素中,选择适当的元素符号用化学用语填空。
(1)最简单的有机物_____。
(2)污染空气的气体_____(填一种即可)。
(3)两个氮分子_____。
(4)氧化铝中铝元素的化合价_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】若分别将100gt3°C时甲、乙、丙的饱和溶液降温至t1°C,对所得的三种溶液的说法正确的是_____。
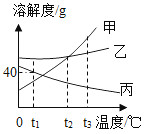
A. 甲、乙、丙都是饱和溶液
B. 所含溶剂质量:甲<乙<丙
C. 溶质质量分数:乙>甲=丙
D. 溶液质量:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下,测得反应前后各物质的质量分数如图所示,下列说法正确的是_____。
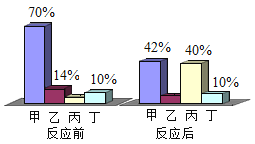
A. 丙可能是单质
B. 丁一定是该反应的催化剂
C. 该反应是化合反应
D. 该反应中乙、丙的质量比为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个图象中,能正确表示对应变化关系的是( )
A. 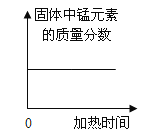 加热一定量的高锰酸钾固体
加热一定量的高锰酸钾固体
B. 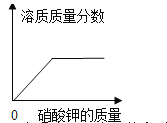 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
C. 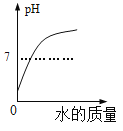 向一定量稀盐酸中加水稀释
向一定量稀盐酸中加水稀释
D. 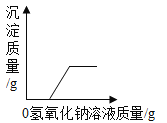 向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液
向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景。其反应的微观示意图为下列有关说法正确的( )
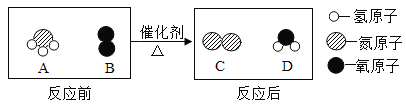
A. 反应前后分子个数不变
B. 反应前后原子数目发生改变
C. 反应中C、D分子个数比为1:1
D. 该反应为置换反应
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钙(CaO2)是一种白色无毒的固体,微溶于水,溶于酸,能杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等方面。以下是一种制备过氧化钙的实验方法:
(Ⅰ)氨气的制备
(查阅资料)
①实验室常用加热氯化铵和熟石灰固体混合物的方法制取氨气;
②氨气极易溶于水,所得溶液称为氨水。
③碱石灰的主要成分是氧化钙和氢氧化钠的混合物。
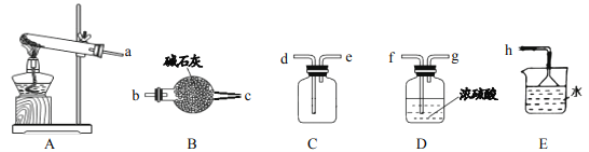
(1)实验室制取氨气的化学方程式_____。
(2)如需收集一瓶干燥的氨气,请选择上图中合适的装置,装置连接顺序为:a→_____→_____→_____→_____→h(按气流方向,用小写字母填空)。
(Ⅱ)碳酸钙的制备

(1)铁的氧化物主要成分为氧化铁,写出氧化铁和盐酸反应的化学方程式_____。
(2)步骤①加入双氧水的目的是使溶液中的Fe2+转化为Fe3+,加入氨水使铁离子形成沉淀,则滤渣的主要成分为_____(填化学式),小火煮沸的作用是使沉淀颗粒长大,有利于_____。
(Ⅲ)过氧化钙的制备
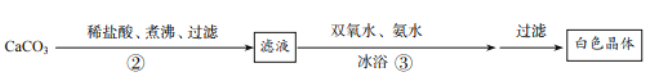
(1)步骤②的具体操作为逐滴加入稀盐酸直至过量。将溶液煮沸的作用是_____。
(2)步骤③是氯化钙和过氧化氢反应制取过氧化钙,则反应的化学方程式为_____,加入氨水的目的是_____,该反应需要在冰浴下进行,原因是_____。
(3)某同学认为,将石灰石煅烧后,直接加入双氧水反应,过滤后即可得到过氧化钙产品,使用该制备工艺的主要缺点是_____。
(4)已知CaO2在350℃迅速分解生成CaO和O2。下图是实验室测定产品中CaO2含量的装置(夹持装置省略)。
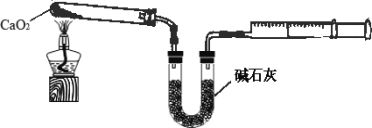
若所取产品质量是0.5g,测得气体体积为60.0mL(该温度下氧气密度为1.6g/L),则产品中CaO2的质量分数为多少_____(写出计算过程)?
查看答案和解析>>
科目: 来源: 题型:
【题目】磷酸铁锂(LiFePO4)电池具有稳定性高、安全、对环境友好等优良性能,是目前最具有发展前景的锂电池正极材料。实验室可利用绿矾(FeSO4·7H2O)和磷酸(H3PO4)为原料制备LiFePO4,其流程如下图所示。已知磷酸铁(FePO4)是一种难溶于水的白色固体。
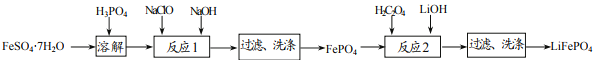
试回答下列问题:
(1)NaClO中氯元素的化合价为_____价。
(2)“溶解”步骤时H3PO4不宜过量太多的原因是_____。
(3)过滤操作中用到的玻璃仪器有:烧杯、玻璃棒和_____。
(4)取反应1最后一次洗涤后的滤液,依次滴加硝酸银溶液和稀硝酸,有白色沉淀生成,则滤液中肯定含有的物质是_____。
(5)请你完成“反应2”总反应的化学方程式。
2LiOH+6H2C2O4+2FePO4=2LiFePO4+7CO2↑+5_____+7H2O(在空格中填写正确的化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com