
科目: 来源: 题型:
【题目】为探究铁生锈的条件,某化学社团设计了如下实验:取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,装置如图所示,进行下列实验,实验要保证有足够长的时间来观察现象.
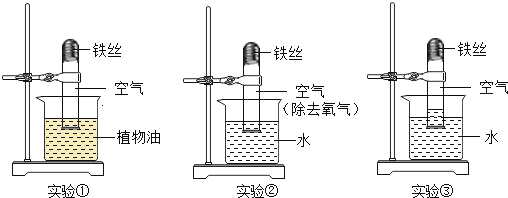
(1)铁生锈实际上是铁与空气中的_____(填名称)发生反应的结果.
(2)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的_____.
(3)该实验创新之处在于:可根据铁丝表面的铁锈和_____两种现象来判断铁丝反应进行的情况.
查看答案和解析>>
科目: 来源: 题型:
【题目】某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰好完全反应时:
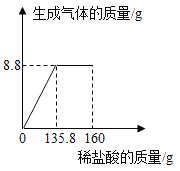
(1)产生的二氧化碳的质量是 克。
(2)此时所得到的溶液中溶质的质量分数(写出必要的计算过程,结果保留到0.1%)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(9分)某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数.
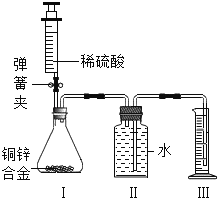
探究过程如下:
①连接实验装置并检查装置气密性.
②向装置Ⅰ中的锥形瓶加入2.0g的铜锌合金样品粉末,由注射器缓缓注入稀硫酸,待到锥形瓶中不再产生气体时,准确读取注射器内读数,减少10.5mL稀硫酸,同时立即夹紧弹簧夹,移出装置Ⅲ中的导管,准确读取量筒内水的体积为214.0mL.(注:样品中的杂质不参加反应)
③装置Ⅰ中剩余固体物质经过适当处理后,准确称量其质量1.4g.
④该小组的三位同学利用实验过程测得不同数据,计算铜锌合金样品中锌的质量分数.
甲同学利用装置Ⅰ中反应前后固体的质量进行计算;
乙同学利用装置Ⅰ中加入稀硫酸的量进行计算;
丙同学利用装置Ⅲ中量取水的体积进行计算,并查得:在标准状况下,氢气的密度为0.09g/L.
回答下列问题:
(1)装置Ⅰ中反应的化学方程式为 ,实验过程中须加入稀硫酸至不再产生气体,目的是 .
(2)步骤③中称量剩余固体之前的正确操作是 、洗涤、干燥.
(3)根据实验测定的数据,上述三位同学中 (填“甲”、“乙”或“丙”)同学无法进行计算样品中锌的质量分数.
(4)化学小组同学发现:按照丙同学的方案进行计算,致使实验结果出现较大偏差.以下因素可能造成偏差的有 (填标号).
A.移出装置Ⅲ时,导管内留存了一部分水
B.实验测量前,没有排除装置Ⅰ中的空气
C.数据处理时,未排除加入稀硫酸所占的体积.
查看答案和解析>>
科目: 来源: 题型:
【题目】(10分)南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源。
(1)海水制盐。从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加稍过量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发。正确的操作顺序是 (填字母)。加Na2CO3溶液的作用是除去 。
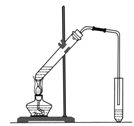
(2)海水淡化。下图是一个简易的蒸馏法淡化海水的装置。证明得到的水是淡水的方法是 。
(3)海水制镁。从海水中提取金属镁的过程如下图所示:
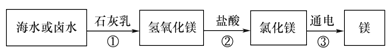
在上述转化过程中发生中和反应的是 (填反应顺序号)。海水中本身就含有氯化镁,则①、②两步的作用是 。
(4)海水“制碱”。氨碱法制纯碱是先通过化学反应生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱。
①氨碱法制纯碱中生成NaHCO3和NH4Cl的化学方程式为 ;
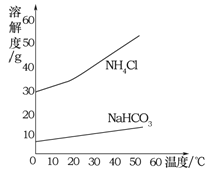
②反应中生成NaHCO3和NH4Cl的质量比为84∶53.5,NaHCO3和NH4Cl的溶解度曲线如图所示。请分析NaHCO3结晶析出而NH4Cl没有结晶析出的原因是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如右下图所示。下列有关说法不正确的是

A.该图像表示的是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好完全反应时。溶液的pH等于7
C.当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D.滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
查看答案和解析>>
科目: 来源: 题型:
【题目】“国庆”假期,小周对“活泼金属与硫酸溶液反应快慢的影响因素”进行了探究。
(提出问题)活泼金属与硫酸溶液反应的快慢受哪些因素的影响呢?
(猜想与假设)a.可能与硫酸溶液的质量分数有关;
b.可能与金属的形状有关;
c.可能与金属的种类有关。
(设计并实验)小周用不同质量分数的硫酸溶液和不同形状的锌进行如下实验:
实验编号 | 硫酸溶液的质量分数(均取20mL) | 锌的形状 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
① | 5% | 锌粒 | 15.6 |
② | 5% | 锌片 | 25.9 |
③ | 10% | 锌粒 | 32.7 |
④ | 10% | 锌片 | 40.9 |
(1)小周用如图装置收集并测量氢气的体积,氢气应从_____管通入。(填e或f或g)
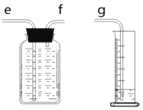
(2)(收集证据)要比较不同质量分数的硫酸溶液与锌反应快慢的影响,可以选择的实验编号是_____。
(得出结论)……
(反思与评价)你认为本实验设计存在哪些不足之处_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】有些化学反应观察不到明显的现象,但通常伴随能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀硫酸混合前后温度有变化,则可以证明发生了化学变化。小周将不同浓度的稀硫酸和NaOH溶液各10克混合,并用灵敏温度计测定同一室温下溶液混合前后温度的变化值(实验装置放置于隔热良好的环境),记录数据见下表。
编号 | 稀硫酸(%) | NaOH溶液(%) | 温度变化/.C |
1 | 9.8 | 4.0 | 3.8 |
2 | 9.8 | 8.0 | 7.6 |
3 | 19.6 | 16.0 | 15.2 |
反应的方程式为:2NaOH+H2SO4═Na2SO4+2H2O
(1)编号1实验反应后,溶液中的溶质是_____。(写化学式)
(2)求编号3实验反应后溶液中溶质质量分数。_____________(计算结果精确至0.1%)
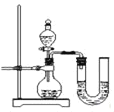
(3)小周在没有使用温度计的情况下,通过如图所示装置也完成了实验,小周判断的依据是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】小周在适宜的条件下,利用 KNO3 晶体和溶质质量分数为 20%的 KNO3 溶液,配制一定溶质质量分数的 KNO3 溶液。取 40克 KNO3 晶体置于烧杯中,并依次加入溶质质量分数为 20%的KNO3 溶液并充分搅拌溶解,其过程如图所示:

(1)在配制过程各阶段的溶液中属于饱和溶液的有_____。(填烧杯序号)
(2)计算④号烧杯中溶液的溶质质量分数(结果精确到0.1%)____________。
(3)已知KNO3晶体的溶解度随温度的升高而增大,在不考虑水分蒸发的情况下,在配制过程中,下列操作会导致④号烧杯中溶液的溶质质量分数偏大的有_____。
A 所用 KNO3 晶体混有少量泥沙 B 配制过程中环境温度升高
C 用砝码生锈的天平称取 40克K NO3 晶体 D 溶解时没有用玻璃棒搅拌
查看答案和解析>>
科目: 来源: 题型:
【题目】金属活动性顺序有重要的应用。铝、铜、铁为日常生活中常见的金属,某化学小组的同学在探究铝、铜、铁三种金属的有关性质时,进行了如图所示的实验:
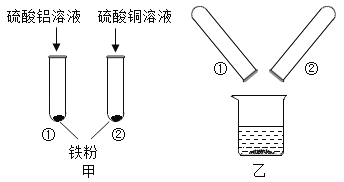
(1)在甲实验②号试管中能观察到的实验现象是_____。
(2)将甲实验结束后①②试管内的物质倒入烧杯中,一段时间后对烧杯中的物质进行过滤,滤液中的溶质一定有_____。
(3)若要验证铝、铁、铜金属活动性顺序,还可以用一种试剂直接与上述金属反应就能达到目的,该试剂可以是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】“对比实验”是科学学习中重要的思维方法。某科学学习小组在实验室做了如图所示的对比实验,请回答下列问题:
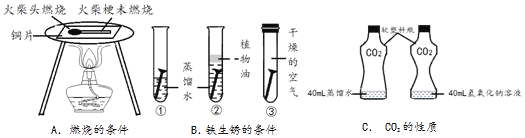
(1)实验A发现火柴头燃烧了,火柴梗没燃烧,说明可燃物燃烧的条件之一是_____,实验结束后发现铜片变黑了,写出黑色物质的化学式_____。
(2)一段时间后,观察到实验B试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是_____。
(3)实验C能证明CO2能与NaOH溶液发生反应的证据是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com