
科目: 来源: 题型:
【题目】某粗盐中除NaCl以外还含有少量杂质MgCl2,为了测定粗盐中MgCl2的质量分数。取固体样品50.0g完全溶解于150.0g水中,并向其中逐渐加入一定浓度的NaOH溶液,实验过程中生成沉淀的质量与加入NaOH溶液的质量的关系如图所示:

注:发生反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl
请根据相关信息完成下列计算:
(1)反应完全时,生成氢氧化镁的质量为_____g;
(2)在粗盐中氯化镁的质量分数;_____
(3)恰好完全反应时得到的溶液中溶质的质量分数。_____
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组的同学要从BaCl2、NaCl混合溶液中得到较纯净的BaCl2和NaCl晶体,为此进行下列实验设计和操作,请回答下列问题。
(提出问题)如何分离BaCl2和NaCl,并得到两种晶体?
(设计方案并实验)
张南同学的实验方案:取一部分混合液于试管中,先向其中加入适量的Na2SO4溶液,过滤,向滤渣中加入适量稀盐酸,将滤液蒸发结晶。
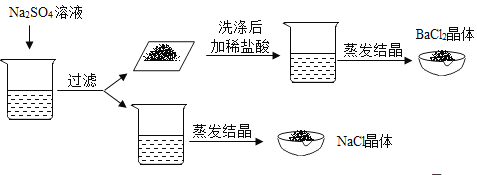
小岗同学的实验方案:取一部分混合液于试管中,先向其中加入过量的Na2CO3溶液,过滤,向滤渣中加入过量稀盐酸,将滤液蒸发结晶。
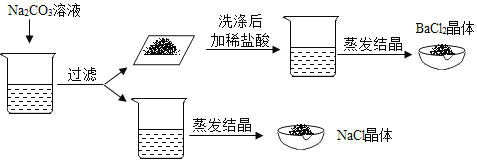
(填写实验报告)
(1)请写出张南同学加入Na2SO4溶液后反应的化学方程式___
(2)小岗同学向滤渣中再加入过量稀盐酸的实验现象是___;
(交流与评价)
(3)小岗同学认为张南同学实验方案不合理,理由是___
(4)小岗同学的实验中加入过量的Na2CO3溶液后,所得溶液中的离子有___(填离子符号) 张南同学认为加入过量稀盐酸可以把碳酸钠杂质去掉,这样做会使所得的氯化钠溶液含有杂质离子,所以方案不合理,但小岗同学认为只要把滤液进行蒸发结晶就不会影响实验结果,在进行蒸发操作时,当___,停止加热。
(反思与总结)
(5)小岗同学在进行操作时所用试剂都是过量的,但后来得到物质确是纯净的,由此我们得出的经验是:如果我们前面加入试剂不能控制适量,那么可以通过___除去干扰离子,而不产生杂质离子或引入干扰离子。
查看答案和解析>>
科目: 来源: 题型:
【题目】人类对物质结构、原子结构的认识永无止境。
(1)最早提出如图1所示原子模型的科学家是______。
(2)α离子轰击金箔后的运动轨迹如图2所示,大多数α粒子不改变原来的运动方向,顺利穿过金箔,说明______,能证明原子核带正电的现象是______;极少数α粒子被反弹回来说明______。
(3)正电子、负质子都属于反粒子,它们与普通的电子、质子的质量与电量均相等,而电性相反,科学家设想在宇宙的某些部分可能存在完全由反粒子构成的反物质,请你推测反氢原子的结构;反氢分子中反氢原子的相对原子质量为______,反氢原子失去一个电子后形成的离子符号是______。

查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下面短文。
酵母与泡打粉:生活中制作糕点、馒头时一般都要添加酵母或泡打粉进行发酵。在面团发酵初期,面团中的氧气和其他养分供应充足,酵母的生命活动非常旺盛,进行着有氧呼吸,淀粉水解成麦芽糖。接着面粉中原有的微量蔗糖及新产生的麦芽糖水解生成葡萄糖与果糖,最后被酵母氧化成二氧化碳和水。面团中的氧气有限,酵母的有氧呼吸逐渐转为无氧呼吸,生成的二氧化碳在面筋的网络中出不去,加热蒸烤时,二氧化碳受热膨胀,使糕点变得松软。用酵母做的食品松软可口,有特殊风味,易于消化。酵母本身含有丰富的蛋白质及维生素B,可以增加营养价值,因此面点大都用酵母发酵。糖和油对酵母菌有抑制作用。用酵母发酵耗费的时间长,而且发酵时间与温度相关(如图)。因此,也有用泡打粉来代替酵母制作糕点的。泡打粉一般是碳酸氢钠与酒石酸的混合物,通常为碳酸盐与固态酸。将泡打粉调和在面团中,碳酸氢钠与酒石酸遇水以及碳酸氢钠受热时都会产生出二氧化碳气体,使面点成为疏松、多孔的海绵状。泡打粉使用时不受发酵时间限制,随时可用,对多油多糖的面团也照样起发泡疏松的作用。缺点是它的碱性会破坏面团中的维生素,降低营养价值,若混合不均匀反而会导致面制品中有的地方碱太多发黄而不能吃。
依据文章内容回答下列问题。
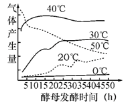
(1)用酵母和泡打粉都能使制作的面食疏松多孔,是因为_____________________________。
(2)在5-10h内,酵母发酵的最佳温度是___________。
(3)酵母本身营养丰富是因为_________________________。
(4)NaHCO3的俗称是__________________。
(5)下列有关酵母和泡打粉的说法中,正确的是___________。
A 酵母发酵的过程中既有有氧呼吸也有无氧呼吸
B 消化功能较弱的人宜食用酵母发酵制作的面食
C 泡打粉的发酵效果与面团中含糖、含油多少无关
D 酵母可以直接使面团中的淀粉转化为二氧化碳和水
查看答案和解析>>
科目: 来源: 题型:
【题目】化学实验小组同学在实验室用过氧化氢溶液制氧气。
(1)用过氧化氢和二氧化锰反应的化学方程式为:__________________________。
(2)同学们发现反应时有白雾产生,用如下两个装置来找原因,其目的是:___________。
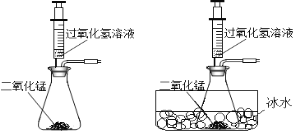
同时又展开了下列思考与探究:
(3)催化剂MnO2的用量对反应速率是否有影响呢?
他们做了这样一组实验:每次均用30mL10%的H2O2溶液,采用不同质量MnO2粉末做催化剂,测定各次收集到500mL氧气所用的时间,结果如下:(其它实验条件均相同)
实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
MnO2粉末用量(克) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
所用时间(秒) | 17 | 8 | 6 | 3 | 2 | 2 | 2 | 2 | 2 | 2 |
请根据表中数据回答,MnO2粉末的用量对反应速率的影响是___________。
(4)H2O2溶液的溶质质量分数对反应速率是否有影响呢?小组同学又做了一组实验:
每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验。记录数据如下:(实验均在20℃室温下进行,其它实验条件均相同)
实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
MnO2粉末用量(克) | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
收集到540mL气体时所用时间(秒) | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
分析表中数据可得出的结论是___________。
(3)实验反思:MnO2颗粒的大小对反应速率是否有影响?请设计实验证明(语言叙述,不用画装置图)___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】中国首款完全自主知识产权民用客机C919飞机的钛合金用量达9.3%。工业上利用钛白粉制备海绵钛的工艺流程如下:
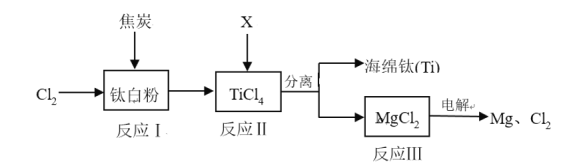
(1)反应Ⅱ发生置换反应生成海锦钛,则物质X的化学式为___________。
(2)反应Ⅲ属于基本反应类型中的__________反应。
(3)该工艺流程中,可以循环使用的物质有__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组用下图装置进行两个实验。已知:白磷的着火点是40℃。
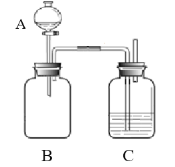
(1)实验一:证明可燃物燃烧条件。A中放有过氧化氢溶液,B中放有一定量二氧化锰;C中放有约半瓶80℃热水,C中左侧长导管出气口处放一块白磷。打开分液漏斗活塞后观察到C中白磷燃烧。该实验证明可燃物燃烧的条件之一是______。该实验C中水的作用是_________。
(2)实验二:证明二氧化碳与氢氧化钠发生化学反应。B中充满二氧化碳,C中液体是足量稀盐酸,打开分液漏斗的活塞,将A中氢氧化钠溶液加入到广口瓶中,关闭活塞,实验过程中可观察到明显的实验现象,产生该现象的原因是________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究铁、铜、银三种金属的活动性顺序,设计了A、B两个方案。
方案A | 方案B |
|
|
(1)能验证三种金属活动性顺序的方案是________(填“A”或“B”)。
(2)方案B中,证明铁的活动性比铜强的现象是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用如图装置制取二氧化碳并完成部分性质实验
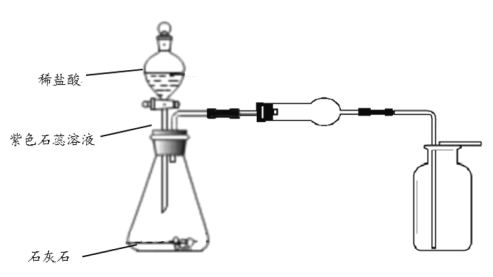
(1)Ⅰ处锥形瓶中发生反应的化学方程式为__________________________________。
(2)写出Ⅱ处干燥管中的实验现象_________________________________________。
(3)Ⅲ处如何证明二氧化碳气体已经充满整个集气瓶?____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用如下图装置测定空气中氧气含量(夹持装置已略去),左侧直玻璃管中液面以上平分为5份。
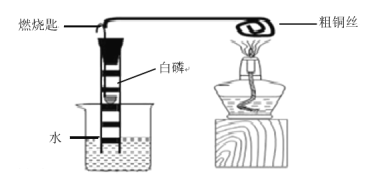
(1)加热铜丝可以引燃白磷,利用的是铜有良好的_______性。
(2)能证明空气中氧气含量的现象是________________________。
(3)用白磷能测定空气中氧气含量的原因是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com