
科目: 来源: 题型:
【题目】化学实验课上,教师让同学们用实验台上五瓶无标签的无色溶液,探究酸碱盐之间的反应。五瓶无标签的无色溶液是:Na2CO3 溶液、NaCl 溶液、NaOH 溶液、Ca(OH)2 溶液、稀盐酸。
(1)甲同学用 A、B、C、D、E 给五瓶无标签的无色溶液编号,做两两混合实验,E与其他四种物质混合的实验现象记录如表:
A | B | C | D | |
E | 无现象 | 白色沉淀 | 无色气泡 | 无现象 |
由此实验确定 E 是_____(写化学式),还能确定_____,不能确定的无色溶液可用_____试剂鉴别。
(2)乙同学探究酸碱盐之间反应的实验如图所示。
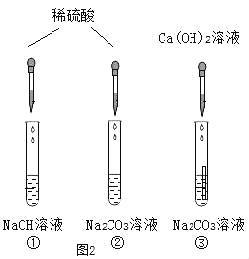
实验①中观察不到明显现象,不能判断反应有没有发生,乙同学是如何改进该实验的?_____,当观察到_____时,说明恰好完全反应,写出反应的化学方程式_____。根据②③实验,结合①的改进实验,可得出酸碱盐之间如果发生反应,要有_____生成。
(3)实验后,丙同学将①②③实验中的废液全部倒入同一只烧杯中,观察到先有气泡产生,后有白色沉淀,过滤得到无色溶液。则无色溶液中一定含有的溶质是_____;可能含有的溶质是_____;为确定可能含有的溶质,简单的实验方案设计是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学兴趣小组用 X 气体与氧化铜反应制取铜的实验装置如图所示,请回答有关问题。

(1)实验开始时,先通一会儿 X 气体,再加热的目的是_____。
(2)实验进行一段时间后,A 玻璃管内观察到的黑色固体变红色,B 干燥管中无明显现象,C 中澄清石灰水变浑浊,则 X 气体为_____;写出 A 玻璃管内发生反应的化学方程式_____。
(3)若用氢气与氧化铜反应,则 B 干燥管中可观察到的现象是_____;用金属锌粒与稀硫酸反应制取氢气,你选择的实验装置(填编号)与理由是_____。
(4)实验过程中,X 气体和氧化铜反应不仅能生成铜,还可能生成中间产物氧化亚铜(化学式为 Cu2O)。如果要对反应后 A 处残留固体的组成进行探究,则残留固体可能的组成有_____种。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学兴趣小组同学,利用木炭粉还原氧化铜实验后的混合粉末(其中含有铜、氧化铜、少量木炭粉) 回收铜,实验流程设计如图所示。
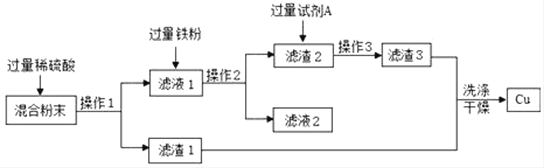
请回答下列问题:
(1)在操作 1、操作 2、操作 3 中,必须用到的玻璃仪器有:烧杯、玻璃棒、_____,其中玻璃棒的作用是_____。
(2)滤液 1 中加入过量铁粉所发生的化学方程式是_____,加入试剂 A 的作用是_____。
(3)按照实验流程操作回收到的 Cu 不纯的原因是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】“卓筒井”是手工制盐的活化石,是我国古代劳动人民勤劳、智慧的象征。其工艺流程包括下面五个步骤:钻井→汲卤→晒卤→滤卤→煎盐。请回答下列问题:
(1)上述步骤中,_____与实验室过滤的原理一样,“煎盐”和实验室_____结晶的原理相同。
(2)“汲卤”获得卤水主要成分是氯化钠与氯化钾,卤水中氯化钠的质量分数大约为 7%~10%,“晒卤”目的是_____;“煎盐”得到的食盐中含有氯化钾,实验室可用_____检验,操作方法是_____。
(3)下列数据是氯化钠和氯化钾固体在不同温度时的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 g/100g 水 | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 | |
根据表中数据可得出:40℃时,氯化钠溶解度_____氯化钾溶解度(填:大于、小于、等于); 氯化钠与氯化钾溶解度相同的温度范围是_____;20℃时,100g 卤水氯化钠的质量分数为 9%,含氯化钾 1.00g,蒸发掉水大于_____g,开始有氯化钠析出。
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值。下列叙述中正确的是( )
A. 分子总数为NA 的NO2和CO2混合气体中含有的氧原子数为4NA
B. 常温常压下,92gNO2和N2O4混合气体中含有的原子数为6NA
C. 1mol SO3中含有的分子数目为4NA
D. 含有3.01×1023个原子的氮气中,N2的分子数为0.5NA
查看答案和解析>>
科目: 来源: 题型:
【题目】20℃时,将等质量的甲、乙两种不与水反应的固体物质(不含结晶水),分别加入到盛有100g 水的烧杯中,充分搅拌后现象如图1,加热到 50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3.则下列说法中错误的是( )
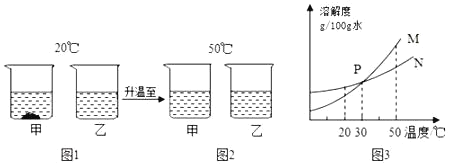
A. 图1中乙的溶液可能是不饱和溶液
B. 图2中两溶液溶质质量分数一定相等
C. 图3中 M表示的是甲的溶解度曲线
D. 图2中两溶液降温至30℃都会析出晶体
查看答案和解析>>
科目: 来源: 题型:
【题目】已知甲、乙两种物质在光照条件下能发生化学反应生成丙和丁,其微观示意图如图(说明:一种小球代表一种原子),则下列说法正确的是( )
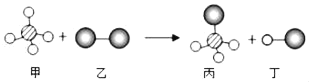
A. 图示中的反应物、生成物都是化合物
B. 根据反应条件推测,该化学变化还伴随着能量变化
C. 该反应原子种类与分子种类都不变,因此符合质量守恒定律
D. 图示中的反应物、生成物质量比为 1:1:1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】钢铁工业是一个国家工业化发展的支柱产业,如图是实验室和工业冶炼铁的示意图,某学校采用“问题探究式”课堂教学,从而解决问题,请你参与完成下列问题:
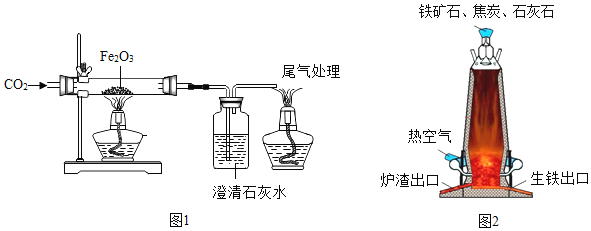
(1)实验时若先给氧化铁加热,再通一氧化碳可能产生的后果是_____;
(2)应对尾气处理的主要原因是_____;
(3)小明同学认为尾气可先储存在瓶内,然后再处理,如图3是他设计的贮气瓶。

①a、b两管应如何伸入,请将图补充完整_____;
②尾气应从_____(填“a”或“b”)端管口通入(其他装置略)。
(4)小刚同学提出质疑:CO能否使澄清石灰水变浑浊?因此,他设计在CO通入Fe2O3之前,应先通入澄清石灰水,以排除CO与澄清石灰水的反应,试对此作出评价。你认为小刚同学的设计是否有必要:_____,理由是_____。
(5)工业炼铁中焦碳的作用是_____。
(6)现将50吨含氧化铁80%的铁矿石与足量一氧化碳充分反应后,理论上可得到铁的质量多少_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】硝酸见光易发生如下分解反应:4HNO3![]() 2X+4NO2↑+O2↑。
2X+4NO2↑+O2↑。
①X的化学式为_____。
②NO2中N元素的化合价为_____。
③硝酸应_____保存。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com